Химические свойства аминов
| Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов: |
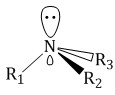
| Аммиак:NH3 | Первичный амин R–:NH2 |
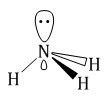
| 
|
| Поэтому амины и аммиак обладают свойствами оснований. |
Основные свойства аминов
| Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми. |
Это объясняется тем, что радикалы СН3–, С2Н5– увеличивают электронную плотность на атоме азота:
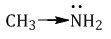 Это приводит к усилению основных свойств.
Это приводит к усилению основных свойств.
| Основные свойства аминов возрастают в ряду: |

Взаимодействие с водой
В водном растворе амины обратимо реагируют с водой. Среда водного раствора аминов — слабощелочная:
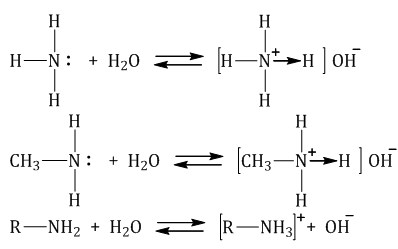
Взаимодействие с кислотами
Амины реагируют с кислотами, как минеральными, так и карбоновыми, и аминокислотами, образуя соли (или амиды в случае карбоновых кислот):
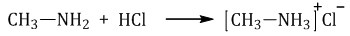
При взаимодействии аминов с многоосновными кислотами возможно образование кислых солей:
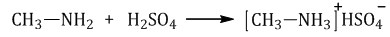
Взаимодействие с солями
Амины способны осаждать гидроксиды тяжелых металлов из водных растворов.
| Например, при взаимодействии с хлоридом железа (II) образуется осадок гидроксида железа (II): |

Окисление аминов
Амины сгорают в кислороде, образуя азот, углекислый газ и воду. Например, уравнение сгорания этиламина:

Особенности анилина
Анилин С6H5-NH2 – это ароматический амин.
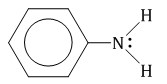
| Анилин – бесцветная маслянистая жидкость с характерным запахом. На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. В воде практически не растворяется. |
При 18 оС в 100 мл воды растворяется 3,6г анилина. Раствор анилина не изменяет окраску индикаторов.
Видеоопыт изучения среды раствора анилина можно посмотреть здесь.
| Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. |
Бензольное кольцо уменьшает основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком:
Анилин не реагирует с водой, но реагирует с сильными кислотами, образуя соли:
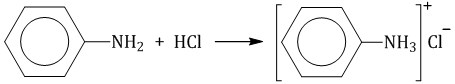
· Бензольное кольцо в анилине становится более активным в реакциях замещения, чем у бензола.
Реакция с галогенами идёт без катализатора во все три орто- и пара- положения.
| Качественная реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок ↓). |
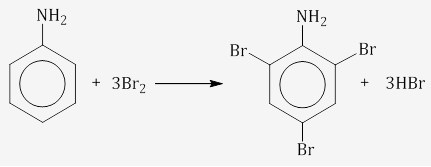
Получение аминов
Восстановление нитросоединений
Первичные амины можно получить восстановлением нитросоединений.
· Гидрирование водородом:
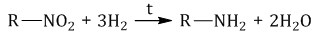
· Восстановление сульфидом аммония (реакция Зинина):

· Алюминий или цинк в щелочной среде.
Алюминий и цинк реагируют с щелочами с образованием гидроксокомплексов.
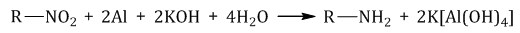
В щелочной и нейтральной среде получаются амины.
Восстановлением нитробензола получают анилин.
· Металлами в кислой среде – железом, оловом или цинком в соляной кислоте.
При этом образуются не сами амины, а соли аминов:

Амины из раствора соли выделяют с помощью щелочи:

Домашнее задание
- Почему амины называют органическими основаниями? УСТНО Запишите уравнения реакций: 1. метиламина с серной кислотой; 2. анилина с соляной кислотой
- Как свойства анилина подтверждают положение теории химического строения о взаимном влиянии атомов в молекуле. УСТНО
- Запишите уравнения реакции бромирования 1. бензола, 2. анилина 3. Почему реакцию бромирования анилина называют качественной реакцией на анилин?
Критерии оценки: Каждое задание из пяти 1.1, 1.2, 3.1, 3.2, 3.3 оценивается в один балл.