Очень часто диагноз Д(-)ГУС необходимо дифференцировать от тромботической тромбоцитопенической пурпуры (ТТП) Мошковица. ТТП является редким нарушением коагуляционного гемостаза, ассоциированного с дефицитом (<5%) или подавлением активности энзима ADAMTS13, инактивирующего фактор Виллебранда и также известного как «протеаза, разрушающая фактор Виллебранда». Дефицит или подавление активности ADAMTS13 вызывает формирование тромбоцитарных микротромбов в капиллярном русле, вызывая гемолиз и повреждение органов и систем: нарушения сознания, неврологическую симптоматику, ОПН, лихорадку, петехиальную сыпь, экхимозы, обусловленные тромбоцитопенией, микроангиопатическую гемолитическую анемию. ГУС и ТТП имеют схожую клиническую картину, хотя считается, что неврологическая симптоматика обычно более выражена при ТТП. Летальность при ТТП составляет 5-10%.
Лечение
Специфической терапии ГУС не существует. Лечение пациентов с Д(+)ГУС заключается в проведении заместительной почечной терапии (ЗПТ) в тех случаях, когда она показана с целью поддержания гомеостаза и обеспечения жизненно важных функций. Параллельно проводится посиндромная терапия, включающая регуляцию водно-электролитного баланса, коррекцию анемии (трансфузии эритроцитов). Применение СЗП также не является доказано необходимым, а трансфузия тромбоцитарной массы оправдано только при наличии клиники кровотечения.
2. Устанавливается мочевой катетер с контролем жидкостного баланса каждые 4-6 часа. Желателен «легкий» отрицательный баланс. Рекомендуемый объем инфузионной терапии рассчитывается как «объем диуреза + 10 мл\кг в сут».
3. Лазикс (фуросемид) от 1 до 5-10 мг\кг\сут дробно или микроструйно. При отсутствии эффекта препарат должен быть отменен.
|
|
4. Гиперкалиемия: при выявлении на ЭКГ признаков угрожающей гиперкалиемии (высокий зубец Т, расширение QRS, широкий зубец Р, наличие эктопического ритма) проводятся экстренные консервативные мероприятия: в/в введение:
· NaHCO3 из расчета 1 мэкв/кг в течение 10 мин;
· 10% глюконат кальция 0.5 мл/кг в течение 5-10 минут;
· 10% раствор глюкозы 10 мл/кг или 4 мл/кг 20% глюкозы с инсулином из расчета 0.3 ЕД на 1 грамм глюкозы в течение 20 минут.
· ß2-агонисты (сальбутамол) в\в или ингаляционно; снижает уровень К+ на 0.6 ммоль\л на 4-5 часов.
5. Гемотрансфузии для лечения анемии. При снижении Hb<60 г\л показано переливание эритроцитарной массы(5-10 мл\кг за 4-8 часов).
6. Для коррекции артериальной гипертонии используется нифедипин 0,25-0,5, мах до 1 мг\кг peros, 0,5-1 мкг\кг\мин в\в.
7. При наличии судорожного синдрома: в\вдиазепам (0,2-0,4 до 1 мг\кг разовая доза), мидазолам (0,2-0,3 мг\кг, разовая доза)
8. При наличии ОПН показано проведение почечно-заместительной терапии (перитонеальный диализ, продленная вено-венозная гемодиафильтрация).
Показания к проведению диализа:
a. Мочевина>22-25 ммоль\л, при повышении креатинина до 250 - 300 (максимально 400) мкмоль/л или его быстром приросте (на 44 и более мкмоль\л\сут),
Некоррегируемыегиперкалиемия, ацидоз, гиперфосфатемия
b. Массивная перегрузка жидкостью
c. Тяжелая неврологическая симптоматика
d. Анурия (<0,3 мл\кг\час), несмотря на терапию лазиксом
9. Интубация и ИВЛ при оценке по шкале ком Глазго <8, наличии острой неврологической симптоматики, при наличии дыхательной недостаточности.
|
|
10. Терапия отека мозга (см. гл.17. раздел 17.5. «Отек мозга»)
Лечебные мероприятия при ТТП.
Плазмаферез для удаления ингибиторов ADAMTS13 c заменой плазмы пациента СЗП или криопреципитатом. Рекомендуется терапия СЗП 10-20, до 40 мл\кг\сут на протяжении длительного времени. Многие авторы доказывают необходимость ежедневногоплазмафереза длительное время
Первым и единственным препаратом, зарегистрированным для лечения атипичного ГУС является ЭКУЛИЗУМАБ (Солирис) – рекомбинантное гуманизированноемоноклональное антитело, которое связывается с белком С5 комплимента, что приводит к блокированию его активации и расщеплению на С5а и С5b, предотвращая образование терминального комплекса комплимента C5b-9 и подавляет активацию комплимент-опосредованного лизиса клеток. Таким образом ЭКУЛИЗУМАБ препятствует вызываемому комплиментом внутрисосудистому гемолизу. Ранее препарат использовался у больных пароксизмальной ночной гемоглобинурией. С 2011 года в США и странах Евросоюза СОЛИРИС одобрен для использования у пациентов с атипичным ГУС для подавления комплимент-обусловленной тромботической микроангиопатии. СОЛИРИС не показан для лечения пациентов с ГУС, обусловленномшига-токсином Е.coli. Однако во время эпидемии E. coli O104:H4 в Европе в 2011 году, насчитывающей 4321 пострадавших, из них 852 с ГУС (в 3 раза больше, чем обычно), с 50 летальными исходами (из них у 32 с ГУС) у нескольких детей в крайне тяжелом состоянии, не отвечающих на традиционное лечение (гемодиализ, плазмаобмен), с выраженными неврологическими осложнениями была проведена терапия СОЛИРИСОМ. В течение 24 часов отмечалось значительное улучшение по неврологическому статусу, быстрая нормализация числа тромбоцитов и уровня ЛДГ. Через 6 мес у всех данных пациентов констатировано полное восстановление. Было показано, что шига-токсин может также вызывать прямую активацию комплимента, в силу чего возможно и у пациентов c шига-токсин-обусловленным ГУС также рационально проведение терапии, направленной на блокирование комплимента. В данном направлении идут клинические исследования.
|
|
Методики применения СОЛИРИСА при атипичном ГУС
| Вес | Индукция | Поддерживающая доза |
| Пациентам старше 18 лет | ||
| По 900 мг 1 раз в неделю в течение первых 4 недель | 1200 мг на 5 неделе, затем 1200 мг каждые 2 недели | |
| Пациентам <18 лет рассчитывается с учетом массы тела по схеме: | ||
| 40 кг и более | По 900 мг 1 раз в неделю в течение первых 4 недель | 1200 мг на 5 неделе, затем 1200 мг каждые 2 недели |
| 30-40 кг | По 600 мг 1 раз в неделю в течение первых 2 недель | 900 мг на 3 неделе, затем 900 мг каждые 2 недели |
| 20-30 кг | По 600 мг 1 раз в неделю в течение 2 недель | 600 мг на 3 неделе, затем 600 мг каждые 2 недели |
| 10-20 кг | По 600 мг 1 раз в неделю | 300 мг на 2 неделе, затем 300 мг каждые 2 недели |
| 5-10 кг | 300 мг 1 раз в неделю | 300 мг на 2 неделе, затем 300 мг каждые 3 недели |
Ввиду своего механизма действия препарат СОЛИРИС повышает предрасположенность больного к менингококковой инфекции (Neisseriameningitidis). Поэтому минимум за 2 недели до начала лечения СОЛИРИСОМ необходимо проведение вакцинации тетравалентной вакциной против менингококка. (В Германии во время эпидемии вакцинация начиналась на фоне терапии СОЛИРИСОМ.)
У пациентов, где этиологическим фактором выступает Streptococcuspneumoniae,необходимо максимально избегать переливания препаратов плазмы, а эритроциты и тромбоциты должны быть «отмыты» для удаления анти-Т-иммуноглобулина.
При наличии неврологических симптомов при атипичном ГУС рекомендуется проведение обменногоплазмафереза. В то же время в проспективных клинических исследованиях не было доказано эффективности и безопасности проведения замены плазмы, 59% пациентов погибают или полностью утрачивают функцию почек даже после проведения плазмаобмена/инфузии плазмы в результате прогрессирования заболевания.
Осложнения
Полиорганная недостаточность
Прогноз
Летальность в острую фазу составляет 5-10% и как правило, обусловлена церебральными и кишечными осложнениями.У 85% детей отмечается полное выздоровление. Хроническая почечная недостаточность развивается у 4-10%, резидуальные неврологические нарушения отмечаются у 5% пациентов.
Конечным результатом Д(-)ГУС в большинстве случаев являются резидуальные нарушения функции почек с исходом в терминальную хроническую почечную недостаточность. Более 50% пациентов с атипичным ГУС погибают, нуждаются в диализе или страдают от почечной недостаточности уже в течение 1 года от установления диагноза.
Литература
1. Рациональная фармакотерапия детских заболеваний. Руководство для практикующих врачей. Под редакцией А.А.Баранова, Н.Н.Володина, Г.А.Самсыгиной, М., Литтера, 2007.
2. T.Nicolai “Pädiatrische Notfall-und Intensivmedizin”, Springer, 2012.
3. P. Barry, K. Morris, T. Ali “Paediatric Intensive Care”, Oxford, 2010.
4. Noris M, Remuzzi G: Atypical hemolytic-uremic syndrome. N Engl J Med 2009 361:1676-87
5. Soliris (eculizumab) full prescribing information. 2011. Cheshire, CT: AlexionPharmaceuticals.
6. Eculizumab in Severe Shiga-Toxin–Associated HUS. N Engl J Med 2011; 364:2561-2563
7. Атипичный гемолитико-уремический синдром (а-ГУС): катастрофические последствия. AlexionPharmaceuticals, 2011.
8. Попа А.В., Лифшиц В.И., Эмирова Х.М. и соав. Современные представления об атипичном гемолитико-уремическом синдроме (NON-Stx-HUS) // Педиатрия. - 2011. - Т. 90, № 4. - С. 134-140
9. Hirt-Minkowski P., Dickernmann M., Schifferli J.A. Atypical Hemolytic Uremic Syndrome: Update on the Complement System and What Is New. Nephron ClinPract., 2012; V.114, N.4: 219-235.
10. M.Beed, R.Sherman, R.Mahajan Emergencies in Critical Care. Oxford University press, 2009.
20.2.Синдром диссеминированного внутрисосудистого свертывания крови (Хамин И.Г.)
Определение
Синдром диссеминированного внутрисосудистого свертывания крови (ДВС) ‒ неспецифический общепатологический процесс нарушениясистемы гемостаза.
Термин «Синдром диссеминированного внутрисосудистого свертывания крови» (ДВС) предложен в 1950 г. Дональдом МакКеем.
Распространенность
Диссеминированное внутрисосудистое свертывание крови часто возникает у детей в критических состояниях.В настоящее время описано более 150 заболеваний, сопровождающихся развитием ДВС.
Этиология
Причинами ДВС могут быть инфекционно-воспалительных заболевания, обильные кровотечения, шоковые состояния, внутрисосудистый гемолиз при переливании несовместимой крови, длительное лечение препаратами, повышающими свертываемость крови, осложнение злокачественных образований. В 60% случаев причиной острого ДВС является сепсис.
Табл. 1. Этиологическая классификация острого ДВС-синдрома
| Инфекционно-септический: Бактериальные инфекции (особенно Грам-отрицательные, менингококкцемия.Это наиболее частые причины в детской интенсивной терапии). Вирусные (например, вирусные геморрагические лихорадки) Другие инфекции:малярия, риккетсиозы | Онкология (контакт с онкологическими прокоагулянтами, тканевым фактором, фактором некроза опухолей, клеточными протеазами): солидные опухоли, лейкозы; В процессе интенсивной химиотерапии. |
| Травматический и при деструкциях тканей: Механическая травма (краш-синдром, массивная травма, проникающие повреждения, ЧМТ), при травматичных оперативных вмешательствах; термальные повреждения (ожоги, обморожения); Гипертермия; Жировая эмболия; при некрозе тканей и органов (асфиксия, гипоксия, острая дистрофия печени, фульминантный некроз печени, синдром Рея, некротический панкреатит, острый инфаркт миокарда, опухолевый распад, ишемия органов и др); при остром внутрисосудистом гемолизе, в том числе при переливаниях несовместимой крови, гемолитико-уремическом синдроме (ГУС); синдроме массивных гемотрансфузий; при острой лучевой болезни. | ДВС у новорожденных: Инфекции Асфиксия в родах Болезнь гиалиновых мембран Аспирационный синдром, апноэ, ателектаз, пневмония Легочное кровотечение Переохлаждение Глубокая недоношенность Тромбозы крупных сосудов Фульминантная пурпура Некротизирующий энтероколит Новообразования у плода и лейкозы Повреждение головного мозга (некрозы и кровоизлияния) Фетальный эритробластоз Поражения печени Врожденное нарушение толерантности к фруктозе |
| Другие расстройства: Цирроз печени РДСВ Инфузия концентратов протромбинового комплекса Воспалительные заболевания кишечника Саркоидоз, амилоидоз Гомозиготный дефицит протеинов С и S | Иммунологические нарушения (активация комплемента, экспозиция тканевого фактора): Анафилактические реакции Аллергические реакции Острые гемолитические посттрансфузионные реакции Гепарин-индуцированная тромбоцитопения Реакция отторжения трансплантата (РТПХ) Болезнь Кавасаки |
| Шоковый: (Геморрагический, гиповолемический, анафилактический, при всех терминальных состояниях). | Акушерский и гинекологический. при эмболии околоплодными водами (особенно инфицированными); при ранней отслойке и предлежанииплаценты; при атонии и массаже матки; при внутриутробной гибели плода и его ретенции; при преэклампсии и эклампсии Индуцированные аборты |
| Прямая активация ферментов: Панкреатит Укусы ядовитых змей |
Патогенез
Поступление в кровоток активаторов свертывания крови и агрегации тромбоцитов, ведет к повышенному образованию тромбина. Избыток тромбина вызывает превращение фибриногена в фибрин, полимеризация которого сопровождается образованием тромбов в микроциркуляторном русле с потреблением тромбоцитов и факторов свертывания крови. Блок микроциркуляции в органах-мишенях ведет к гипоксии, дистрофии и глубокой дисфункции этих органов, что сопровождается развитиеминтоксикации организма продуктами тканевого распада, вторичной эндогенной бактериемии, тяжелого тромбо-геморрагического синдрома. Одновременно тромбин активирует превращение плазминогена в плазмин, с истощением плазменных протеолитических систем. Плазмин вызывает растворение фибрина с образованием продуктов деградации фибрина, которые ингибируя полимеризацию фибрина, увеличивают геморрагический синдром.
«Если система гемостаза и организм в целом способны скомпенсировать действие инициаторов свертывания, то имеет место гиперкоагуляция и ограниченное тромбообразование. Если развивается декомпенсация, то это состояние можно трактовать как ДВС-синдром».
Клиника
Касаясь клинической картины ДВС-синдрома, необходимо отметить, что она складывается из симптомов основного заболевания, индуцирующего развитие ДВС, и непосредственно его проявлений..
Различают острый, подострый и хронический ДВС-синдром.
Острый ДВС (включая молниеносную (катастрофическую) форму) характеризуется комплексом аномалий, включающих нарушение микроциркуляции, повреждение сосудистой стенки, тромбоцитопению, тромбоцитопатию, анизоцитоз и гемолиз эритроцитов, нейтрофильную реакцию, гиперкоагуляцию и геморрагический синдром на фоне коагулопатии и тромбоцитопатии потребления, нарушения в системах фибринолиза, антикоагулянтов, калликреин-кининовой и других протеолитических систем. Доминирует геморрагический синдром (петехии, экхимозы, кровоточивость из мест инъекций, со слизистых оболочек, гастроинтестинальное, легочное кровотечения, интракраниальное кровоизлияние). В течении острого ДВС различают несколько стадий:
1. Стадия гиперкоагуляции и гиперагрегации (кратковременная, трудно диагностируемая). Отмечается тромбирование пунктируемых вен и игл при заборе крови на анализы, быстрое свертывание крови в пробирках, несмотря на смешивание ее с цитратом, появление немотивированных тромбозов и признаков органной недостаточности (например, снижение диуреза вследствие нарушения микроциркуляции в почках как ранний признак развивающейся почечной недостаточности).
2. Стадия коагулопатии и тромбоцитопатии потребления с активацией фибринолитической системы (появления множественных кровоизлияний в местах инъекций, пальпации, ниже места наложения манжеты для измерения АД, длительное кровотечение из мест инъекций, операционных ран; носовые и желудочно-кишечные кровотечения, плохая свертываемость вытекающей крови (малые, быстро лизирующиеся сгустки, полная несвертываемость). Одновременно возникают признаки полиорганной недостаточности (неэффективное дыхание, цианоз, снижение диуреза, нарушения сознания и тд)
3. Стадия генерализациифибринолиза
4. Стадия восстановления.
Табл.2. Изменение показателей гемостаза в зависимости от стадии ДВС (по Е.П.Иванову, 1991)
| Показатель | Норма | I стадия | II стадия | III стадия | IV стадия |
| Тромбоциты | 200-300 х 109/л | <100 | .>200 | ||
| Время свертывания | 6-8 мин | 12-20 | 7-10 | ||
| Аутокоагулограмма | 9-11 сек | 7-9 | 10-12 | 15-20 | 9-12 |
| Фибриноген | 2-4г/л | 2-3 | 1,5 | 3-6 | |
| Протромбиновое время | 15-20 мин | 15-22 | |||
| Антитромбин III в %% | 80-120 | 80-90 | 75-80 | 30-60 | 70-100 |
| Этаноловая проба | отр. | + | ++ | ± | ± |
| Протаминовая проба | отр | ++ | + | ± | ± |
| ПДФ-продукты деградации фибриногена в мкг/л | >20 | >15 | >10 | >15 | |
| Ретракция сгустка в %% | 60-75 |
Подострый ДВС характеризуется длительным периодом гиперкоагуляции и\или гиперагрегации тромбоцитов. Представляет собой вялотекущее, скорее хроническое течение. Лабораторно отмечается тромбоцитопения, нормальное или несколько удлиненное ПВ, укорочение АЧТВ, нормальный или несколько сниженный фибриноген, повышение уровня продуктов деградации фибрина (ПДФ).
Под хроническим ДВС понимаютдлительную волнообразно-текущую фибринацию, которая сопровождается персистирующейтромбинемией, выраженной дисфункцией органов-мишеней при минимальной и зачастую моноорганной геморрагической симптоматике с одновременным возникновением тромбозов магистральных вен, склонностью к тромбоэмболии. Геморрагический синдром не выражен.
Для ДВС характерен ряд глубоких органных нарушений, обозначаемых в литературе, как «субсиндромы». Данные нарушения являются вторичными, поскольку в основе лежит отложение фибрина в микрососудистом русле органов. Среди важнейших «субсиндромов» выделяют:
1. Трансформация асептического ДВС-синдрома в септический (инфицирование мест повреждения тканей, нарушение барьерной функции слизистой оболочки кишечника и транслокацией его микрофлоры в кровь): повышение температуры тела с ознобами, нарастание лейкоцитоза, сдвиг лейкоцитарной формулы влево, увеличение СОЭ, повышение в сыворотке крови острофазных белков (С-реактивного) и интерлейкинов.
2. Тромбоцитопения и тромбоцитопатия потребления
3. Субсиндром легочной (дыхательной) недостаточности (диспноэ, гипоксия, цианоз).
4. Субсиндром острой почечной (олигурия, ОПН) и/или гепаторенальной недостаточности
5. Субсиндромы поражения и недостаточности других органов — надпочечников (нестабильная гемодинамика), мозга (нарушения сознания: делириум, кома), сердца и др.
Сочетание «субсиндромов» формирует синдром полиорганной недостаточности.
Диагностика
Лабораторные характеристики:
В общем анализе крови: тромбоцитопения (<100 х 109/l) часто <50 х 109/l). Возможно снижение Hb. В мазке крови присутствую: фрагментированные эритроциты (шизоциты; 50% при остром ДВС, до 90% - при хроническом), сниженное количество тромбоцитов. Лейкоцитоз со сдвигом влево.
АЧТВ удлиненно. Протромбиное время: удлиненно. Снижение фибриногена (<1 g/L). Продукты деградации фибрина: >40 мкг/мл. Появление Д-димеров.
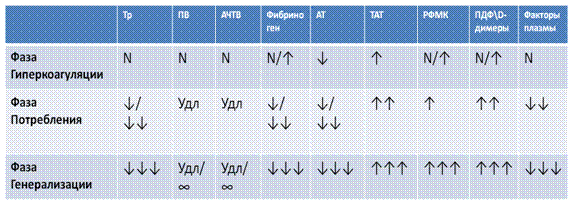
Табл. 3. Динамика изменения показателей свертывающей системы крови при ДВС-синдроме