Задание: 1)Прочитать текст «Строение атома. Изотопы»
Тема: Строения атомов. Изотопы.
Понятие “атом” возникло еще в античном мире для обозначения частиц вещества. В переводе с греческого “атом” означает “неделимый”. Так ли это?
Действительно, атом делим. В центре атома находятся ядро, вокруг которого на большой скорости постоянно движутся электроны. Ядро имеет положительный заряд, а заряд электрона равен -1. Оказывается, ядро атома тоже состоит из частиц. Это протоны, имеющие заряд +1 и массу равную единице (массе атома водорода) – р+ и нейтроны, которые нейтральны, т.е. заряда не имеет, но их масса равна массе протона – n0.
Атом
Ядро Электроны
Протон Нейтрон
Характеристика составных частей атома
| Название частиц | Обозначение | Заряд | Масса |
| Электрон | ℮ | - | 0.000549 |
| Протон | p(Z) | + | 1,007276 |
| Нейтрон | n (N) | 1,008665 |
Информацию о строении атома мы можем найти в периодической таблице.
Заряд ядра, число электронов, число протонов = порядковому номеру в периодической таблице. Порядковый номер – номер, под которым находится данный элемент.
А как определить число нейтронов, если они не имеют заряда, но имеют массу, равную 1?
Число нейтронов рассчитываем: N = Аr – Z, где Аr – относительная атомная масса (массовое число), а Z – порядковый номер элемента или заряд его ядра.
Пример: Элемент: В Cl
Заряд ядра: +5 +17
Число протонов: 5 17
Число электронов: 5 17
Число нейтронов: 11-5=6 35-17=18
Итак, ядро состоит из протонов и нейтронов, массы которых равны 1, тогда массовое число должно быть целым числом. Но в периодической системе практически нет элементов с целочисленным значением относительной атомной массы. Дело в том, что состав атомных ядер может изменяться. Что произойдет, если мы увеличим число протонов в ядре? (Увеличится заряд ядра => получится новый химический элемент.) Такие процессы называются ядерными и происходят, например, на Солнце. В результате ядерных реакций выделяется огромное количество энергии, благодаря которой и существует жизнь на Земле. Человек тоже научился осуществлять такие процессы, например, в ядерных реакторах.
А если изменить число протонов в ядре? (Заряд ядра не изменяется, т.е. это тот же химический элемент, а изменяется только массовое число.)
Разновидности атомов химического элемента с одинаковым зарядом ядра, но разным массовым числом называют изотопы. (С греческого isos – равный, topos – место, т.е. равноместные или занимающие одну клетку в периодической системе.)
Химические элементы, встречающиеся в природе, являются смесью изотопов. Изотопы записываются следующим образом: 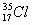 и
и 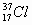 , где нижний индекс – это заряд ядра, а верхний – массовое число(Ar)
, где нижний индекс – это заряд ядра, а верхний – массовое число(Ar)
Например: водород (Н)
1Н 2Н 3Н
Протий Дейтерий Тритий
Заряд ядра: +1 +2 +3
Число протонов: 1 1 1
Число электронов: 1 1 1
Число нейтронов: 0 1 2
Химические свойства изотопов большинства химических элементов одинаковы, несмотря на разную относительную атомную массу. Т.е. свойства элементов зависят не столько от Ar, сколько от заряда ядра. Поэтому современная формулировка периодического закона следующая: свойства простых тел, а так же форма и свойства соединений находятся в периодической зависимости от заряда ядра атома.
Теперь можно дать современное, более точное и научное определение химическому элементу. Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
2) Выполнить упражнения:
А.Определите заряд ядра, число электронов, протонов и нейтронов у химических элементов под номерами: а) 19, б) 5, в) 86, г) 38, д) 44, е) 63.
Б) Сколько протонов, нейтронов и электронов в изотопе: а) 35Cl, б) 25 Mg, в) 65Cu.
!!!! Выполненные упражнения прислать 21 апреля до 14.00