Внутреннюю энергию можно изменить двумя способами.

Если работа совершается над телом, его внутренняя энергия увеличивается.
Вну́тренняя эне́ргия тела (обозначается как E или U) — это сумма энергий молекулярных взаимодействий и тепловых движений молекулы. Внутренняя энергия является однозначной функцией состояния системы. Это означает, что всякий раз, когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе из одного состояния в другое будет всегда равно разности между ее значениями в конечном и начальном состояниях, независимо от пути, по которому совершался переход.
Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:
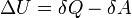
где
-
 — подведённая к телу теплота, измеренная в джоулях
— подведённая к телу теплота, измеренная в джоулях -
 [1] — работа, совершаемая телом против внешних сил, измеренная в джоулях
[1] — работа, совершаемая телом против внешних сил, измеренная в джоулях
Эта формула является математическим выражением первого начала термодинамики
Для квазистатических процессов выполняется следующее соотношение:

где
 — температура, измеренная в кельвинах
— температура, измеренная в кельвинах
 — энтропия, измеренная в джоулях/кельвин
— энтропия, измеренная в джоулях/кельвин
 — давление, измеренное в паскалях
— давление, измеренное в паскалях
 — химический потенциал
— химический потенциал
 — количество частиц в систем
— количество частиц в систем
Теплота сгорания топлива. Условное топливо. Количество воздуха необходимое для горения топлива.
О качестве топлива судят по его теплоте сгорания. Для характеристики твердых и жидких видов топлива служит показатель удельной теплоты сгорания, который представляет собой количество теплоты, выделяемое при полном сгорании единицы массы (кДж/кг). Для газообразных видов топлива применяется показатель объемной теплоты сгорания, представляющий собой количество теплоты выделяемое при сгорании единицы объема (кДж/м3). Кроме того, газообразное топливо в ряде случаев оценивают по количеству теплоты, выделяемой при полном сгорании одного моля газ (кДж/моль).
Теплоту сгорания определяют не только теоретически, но и опытным путем, сжигая определенное количество топлива в специальных приборах, называемых калориметрами. Теплоту сгорания оценивают по повышению температуры воды в колориметре. Результаты, полученные этим методом, близки к значениям, рассчитанным по элементарному составу топлива.
Вопрос 14 Изменение внутренней энергии при нагревании и охлаждении. Работа газа при изменении обьема.
Внутренняя энергия тела зависит от средней кинетической энергии его молекул, а эта энергия, в свою очередь, зависит от температуры. Поэтому, изменяя температуру тела, мы изменяем и его внутреннюю энергию.При нагревании тела его внутренняя энергия увеличивается, при охлаждении уменьшается.
Внутреннюю энергию тела можно изменить и без совершения работы. Так, например, ее можно увеличить, нагрев на плите чайник с водой или опустив ложку в стакан с горячим чаем. Нагревается камин, в котором разведен огонь, крыша дома, освещаемая солнцем, и т. д. Повышение температуры тел во всех этих случаях означает увеличение их внутренней энергии, но это увеличение происходит без совершения работы.
Изменение внутренней энергии тела без совершения работы называется теплообменом. Теплообмен возникает между телами (или частями одного и того же тела), имеющими разную температуру.
Как, например, происходит теплообмен при контакте холодной ложки с горячей водой? Сначала средняя скорость и кинетическая энергия молекул горячей воды превышают среднюю скорость и кинетическую энергию частиц металла, из которого изготовлена ложка. Но в тех местах, где ложка соприкасается с водой, молекулы горячей воды начинают передавать часть своей кинетической энергии частицам ложки, и те начинают двигаться быстрее. Кинетическая энергия молекул воды при этом уменьшается, а кинетическая энергия частиц ложки увеличивается. Вместе с энергией изменяется и температура: вода постепенно остывает, а ложка нагревается. Изменение их температуры происходит до тех пор, пока она и у воды, и у ложки не станет одинаковой.
Часть внутренней энергии, переданной от одного тела к другому при теплообмене, обозначают буквой и называютколичеством теплоты.
Q - количество теплоты.
Количество теплоты не следует путать с температурой. Температура измеряется в градусах, а количество теплоты (как и любая другая энергия) - в джоулях.
При контакте тел с разной температурой более горячее тело отдает некоторое количество теплоты, а более холодное тело его получает.
Работа при изобарном расширении газа. Одним из основных термодинамических процессов, совершающихся в большинстве тепловых машин, является процесс расширения газа с совершением работы. Легко определить работу, совершаемую при изобарном расширении газа.
Если при изобарном расширении газа от объема V1 до объема V2 происходит перемещение поршня в цилиндре на расстояние l (рис. 106), то работа A', совершенная газом, равна

, где p — давление газа,  — изменение его объема.
— изменение его объема.
Работа при произвольном процессе расширения газа. Произвольный процесс расширения газа от объема V1 до объема V2 можно представить как совокупность чередующихся изобарных и изохорных процессов.
Работа при изотермическом расширении газа. Сравнивая площади фигур под участками изотермы и изобары, можно сделать вывод, что расширение газа от объема V1 до объема V2 при одинаковом начальном значении давления газа сопровождается в случае изобарного расширения совершением большей работы.
Работа при сжатии газа. При расширении газа направление вектора силы давления газа совпадает с направлением вектора перемещения, поэтому работа A', совершенная газом, положительна (A' > 0), а работа А внешних сил отрицательна: A = -A' < 0.
При сжатии газа направление вектора внешней силы совпадает с направлением перемещения, поэтому работа А внешних сил положительна (A > 0), а работа A', совершенная газом, отрицательна (A' < 0).
Адиабатный процесс. Кроме изобарного, изохорного и изотермического процессов, в термодинамике часто рассматриваются адиабатные процессы.
Адиабатным процессом называется процесс, происходящий в термодинамической системе при отсутствии теплообмена с окружающими телами, т. е. при условии Q = 0.
Вопрос 15 Условия равновесия тела. Момент силы. Виды равновесия.
Равновесие, или баланс, некоторого числа связанных явлений в естественных и гуманитарных науках.
Система считается находящейся в положении равновесия, если все воздействия на эту систему компенсируются другими или отсутствуют вообще. Сходное понятие — устойчивость. Равновесие может быть устойчивым, неустойчивым или безразличным.
Характерные примеры равновесия:
1. Механическое равновесие, также известно как статическое равновесие, — состояние тела, находящегося в покое, или движущегося равномерно, в котором сумма сил и моментов, действующих на него, равна нулю.
2. Химическое равновесие — положение, в котором химическая реакция протекает в той же степени, как и обратная реакция, и в результате не происходит изменения количества каждого компонента.
3. Физический баланс людей и животных, который поддерживается за счёт понимания его необходимости и в некоторых случаях — при помощи искусственного поддержания этого баланса[источник не указан 948 дней].
4. Термодинамическое равновесие — состояние системы, в котором его внутренние процессы не приводят к изменениям макроскопических параметров (таких, как температура и давление).
Р авенство нулю алгебраической суммы моментов сил не означает также, что при этом тело обязательно находится в покое. На протяжении нескольких миллиардов лет с постоянным периодом продолжается вращение Земли вокруг оси именно потому, что алгебраическая сумма моментов сил, действующих на Землю со стороны других тел, очень мала. По той же причине продолжает вращение с постоянной частотой раскрученное велосипедное колесо, и только внешние силы останавливают это вращение.
Виды равновесия. В практике большую роль играет не только выполнение условия равновесия тел, но и качественная характеристика равновесия, называемая устойчивостью. Различают три вида равновесия тел: устойчивое, неустойчивое и безразличное. Равновесие называется устойчивым, если после небольших внешних воздействий тело возвращается в исходное состояние равновесия. Это происходит, если при небольшом смещении тела в любом направлении от первоначального положения равнодействующая сил, действующих на тело, становится отличной от нуля и направлена к положению равновесия. В устойчивом равновесии находится, например, шар на дне углубления.
Общее условие равновесия тела. Объединяя два вывода, можно сформулировать общее условие равновесия тела: тело находится в равновесии, если равны нулю геометрическая сумма векторов всех приложенных к нему сил и алгебраическая сумма моментов этих сил относительно оси вращения.
Вопрос 16 Парообразование и конденсация. Испарение. Кипение жидкости. Зависимость кипения жидкости от давления.
Парообразование — свойство капельных жидкостей изменять свое агрегатное состояние и превращаться в пар. Парообразование, происходящее лишь на поверхности капельной жидкости, называется испарением. Парообразование по всему объему жидкости называется кипением; оно происходит при определенной температуре, зависящей от давления. Давление, при котором жидкость закипает при данной температуре, называется давлением насыщенных паров pнп, его значение зависит от рода жидкости и ее температуры.
Испаре́ние — процесс перехода вещества из жидкого состояния в газообразное (пар). Процесс испарения является обратным процессу конденсации (переход из парообразного состояния в жидкое. Испарение(парообразование), переход вещества из конденсированной (твердой или жидкой) фазы в газообразную (пар); фазовый переход первого рода.
Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость. В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, то есть когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Число молекул, вылетающих с единицы площади поверхности жидкости за одну секунду, зависит от температуры жидкости. Число молекул, возвращающихся из пара в жидкость, зависит от концентрации молекул пара и от средней скорости их теплового движения, которая определяется температурой пара.
Кипе́ние — процесс парообразования в жидкости (переход вещества из жидкого в газообразное состояние), с возникновением границ разделения фаз. Температура кипения при атмосферном давлении приводится обычно как одна из основных физико-химических характеристик химически чистого вещества.
Кипение различают по типу:
1. кипение при свободной конвекции в большом объеме;
2. кипение при вынужденной конвекции;
3. а так же по отношению средней температуры жидкости к температуре насыщения:
4. кипение жидкости, недогретой до температуры насыщения (поверхностное кипение);
5. кипение жидкости, догретой до температуры насыщения
Пузырьковый
Кипение, при котором пар образуется в виде периодическизарождающихся и растущих пузырей, называется пузырьковым кипением. При медленном пузырьковом кипении в жидкости (а точнее, как правило на стенках или на дне сосуда) появляются пузырьки, наполненные паром. За счёт интенсивного испарения жидкости внутрь пузырьков, они растут, всплывают, и пар высвобождается в паровую фазу над жидкостью. При этом в пристеночном слое жидкость находится в слегка перегретом состоянии, т. е. её температура превышает номинальную температуру кипения. В обычных условиях эта разница невелика (порядка одного градуса).
Плёночный
При увеличении теплового потока до некоторой критической величины отдельные пузырьки сливаются, образуя у стенки сосуда сплошной паровой слой, периодически прорывающийся в объём жидкости. Такой режим называется плёночным.