Диаграмма фазового равновесия для рассматриваемого случая приведена на рис. 8.
Выше линии NEBKMR сплавы находятся в области однородной жидкой фазы. В области KmBMnK сплавы состоят из двух жидких фаз Ж’ и Ж”, концентрация которых определяется линиями KmB и KnM. Кривая BmKnM является линией предельного насыщения, или линией расслаивания.
При температуре BMC происходит монотектическое превращение:
 ,
,
т.е. жидкая фаза концентрации точки М превращается в смесь жидкой фазы концентрации точки В и твёрдой фазы β концентрации точки С.

Рис. 7
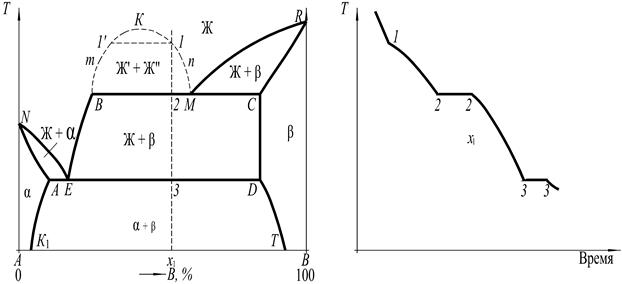
Рис. 8
По правилу фаз в случае монотектического превращения число степеней свободы равно нулю:
С = К – Ф + 1 = 2 – 3 + 1 = 0,
т.е. температура и концентрации фаз в течение всего превращения остаются неизменными.
Рассмотри процессы фазовых переходов при охлаждении сплава состава X 1. В интервале температур T 1- Т 2 из однородной жидкой фазы выделяется жидкая фаза Ж’, концентрация которой изменяется по линии 1’- В. Концентрация жидкой фазы Ж” изменяется по линии 1-М:
 .
.
При температуре Т 2 происходит монотектическое превращение:
 .
.
В интервале температур Т2 - Т 3 происходит кристаллизация твёрдого раствора:
 .
.
При Т 3 происходит эвтектическое превращение:
 .
.
Ниже Т 3 идут следующие превращения:

5. Анализ фазовых превращений в двойных сплавах с наличием
химического соединения
Два компонента могут вступать в химическое взаимодействие друг с другом, образуя химическое соединение. Если химическое соединение устойчиво при всех температурах до температуры его плавления, то такое соединение называется конгруэнтноплавящимся.
Диаграмма фазового равновесия для этого случая с образованием твёрдых растворов α и β на основе компонентов и твёрдого раствора γ на основе химического соединения АmBn представлена на рис. 9.
Для сплава состава Х 2 концентрации компонентов в системе соответствуют химическому соединению. Максимум на кривой ликвидус для сплава Х 2 может быть острым при малой склонности химического соединения к диссоциации АmBn ↔ mA + nB вблизи температуры плавления или пологим при большой степени диссоциации.
Устойчивые химические соединения ведут себя как компоненты, и диаграмма фазового равновесия может рассматриваться как составленная из двух диаграмм с наличием следующих эвтектических превращений:
 ;
;
 .
.
В качестве примера ниже дана схема фазовых переходов для сплава состава Х 1:
 ;
;
 ;
;
 ;
;
 .
.

Рис. 9
В случае образования неустойчивого (инконгруэнтно плавящегося) соединения и ограниченной растворимости в твёрдом состоянии диаграмма фазового равновесия имеет вид, представленный на рис. 10. Твёрдый раствор γ на основе химического соединения АmBn при нагреве устойчив только до температуры ТРОМ, при которой происходит распад:
 .
.
При охлаждении твёрдый раствор γ образуется в результате перитектического превращения:
 .
.
Ниже рассмотрены фазовые переходы при охлаждении сплава состава Х 1:
 ;
;
 ;
;
 ;
;
 ;
;

Рис. 10
6. Анализ фазовых превращений в двойных сплавах при
наличии полиморфных превращений у отдельных компонентов и в случаях перитектоидного и эвтектоидного превращений
Некоторые металлы обладают полиморфизмом, т.е. способностью находиться в различных модификациях, отличающихся строением кристаллической решетки. Каждая кристаллическая модификация устойчива в определенной температурной области. Наличие полиморфизма у отдельных компонентов отражается на диаграммах фазового равновесия. На рис. 11 показана одна из возможных диаграмм фазового равновесия для случая растворимости в твёрдом состоянии при наличии полиморфных превращений у одного из компонентов при температурах ТМ и ТС.
Рассмотрим фазовые переходы, происходящие при охлаждении сплава состава X 1. Кристаллизация твёрдого раствора γ происходит в интервале температур Т 1 и Т 2:
 .
.
В интервале температур Т 3- Т 4 происходит фазовый переход (перекристаллизация в твёрдом состоянии) твёрдого раствора γ на основе одной из модификаций компонента в твёрдый раствор β на основе другой модификации компонента:
 .
.
Аналогичная фазовая перекристаллизация происходит в интервале температур Т 5- Т 6:
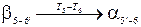 .
.

Рис. 11
В некоторых системах в твёрдом состоянии происходят перитектоидные и эвтектоидные превращения. На рис. 12 представлена диаграмма фазового равновесия с наличием перитектического превращения при температуре ТРМС, т.е. твёрдая фаза γ концентрации точки перитектики Р взаимодействует с твёрдой фазой β концентрации точки С, образуя новую твёрдую фазу α концентрации точки М.
Рис. 12
Рассмотрим фазовые превращения при охлаждении сплава Х 1:
 ;
;
 ;
;

 ;
;
 .
.
На рис. 13 показана одна из возможных диаграмм фазового равновесия с наличием эвтектоидного превращения при температуре ТАЕС:
 ,
,
т.е. твёрдая фаза β концентрации точки Е превращается в смесь, состоящую из кристаллов α и γ твёрдых фаз.

Рис. 13
Рассмотрим фазовые превращения на примере сплава Х 1:
 ;
;
 ;
;
 ;
;
 .
.