Современная промышленность немыслима без использования свойств вакуума. Это особенно относится к работе элекровакуумных приборов (электроннолучевых трубок, магнетронов и др.). Вакуумная техника используется при производстве чистых и сверхчистых материалов. Свойства вакуума используются в технологических процессах, в частности при сушке пищевых продуктов методом сублимационной и вакуумной сушки. Вакуум используют при автоматизации производственных процессов для удержания (присоса) изделий.
ПРОЦЕСС КИПЕНИЯ
Парообразованием называется процесс превращения вещества из жидкого состояния в газообразное. Испарение – это парообразование, происходящее при любой температуре со свободной поверхности жидкости или твёрдого тела.При некоторой температуре, зависящей от физических свойств жидкости и давления, наступает процесс парообразования как со свободной поверхности жидкости, так и по всему её объёму, который называется кипением. Переход вещества из газообразного состояния в жидкое или твёрдое называется конденсацией. Процессы парообразования и конденсации происходят при постоянной температуре, если давление не изменяется. Насыщенным называют пар, соприкасающийся с жидкостью и находящийся в термическом и динамическом равновесии с ней, когда число молекул, покидающих в единицу времени жидкость, равно числу молекул, конденсирующихся на её поверхности. С увеличением температуры жидкости увеличивается число молекул в паровом пространстве, что приводит к росту давления и плотности пара. Одновременно увеличивается скорость конденсации. При новом установившемся значении температуры устанавливается новое состояние равновесия. Давление насыщенного пара является монотонно возрастающей функцией температуры. Сухим насыщенным называют насыщенный пар, в котором отсутствуют взвешенные частицы жидкой фазы. Влажным насыщенным называют насыщенный пар, в котором содержатся взвешенные высокодисперсные частицы жидкой фазы. Массовая доля сухого насыщенного пара во влажном называется степенью сухости пара х, а (1-х) – степенью влажности. Если сухому насыщенному пару при постоянном давлении сообщить некоторое количество теплоты, то его температура будет больше температуры насыщения. Такой пар называется перегретым.
Теплотой жидкости называют количество теплоты, необходимое для нагревания 1кг жидкости от Т=273К до температуры насыщения Тн. Теплотой парообразования называют количество теплоты, необходимое для превращения 1 кг жидкости при температуре кипения в сухой насыщенный пар при постоянных температуре и давлении. Теплота парообразования однозначно определяется давлением и температурой и уменьшается с их ростом до нуля в критической точке. Она расходуется на работу по преодолению сил молекулярного сцепления при переходе молекул из жидкой фазы в паровую (Р) и на внешнюю работу расширения Ф = Р (v’’- v’), где v’’, v’ – удельные объёмы пара и воды. Тогда можно записать: r = (Р+Ф), где r – теплота парообразования. Обычно Р и Ф называют внутренней и внешней теплотой парообразования. Зависимость Р = Р(Т) при фазовом превращении вещества определяется уравнением Клапейрона-Клаузиуса:
dP/dT = r/Tн(v’’- v’ ),
где Tн – температура насыщения,
dP/dT – производная от давления по температуре, взятая на кривой ОК фазового перехода в координатах Р-Т (рис.1.),
Г - газообразная фаза; Ж - жидкая фаза; ОК – парообразование (конденсация); ОА – плавление (отвердевание); ОВ – сублимация (десублимация). Удельный объём сухого насыщенного пара v’’ экспериментальным путём определить трудно из-за неустойчивости состояния пара, поэтому его рассчитывают по уравнению Клапейрона-Клаузиуса, определив из эксперимента другие величины [ r, v’, P=f(Tн) ].
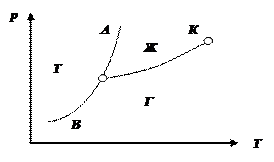 |
Рис.1. Диаграмма Р -Т состояния вещества.
Перегретый пар и в ещё большей степени насыщенный отличаются по свойствам от идеальных газов.
Уравнения состояния для паров сложны и не применяются в практических расчётах. Поэтому используют таблицы и диаграммы, составленные на основании опытных и теоретических данных.В таблицах термодинамических свойств воды и водяного пара (в книге Александрова А.А. и др. «Теплофизические свойства рабочих веществ теплоэнергетики». М: Издательский дом МЭИ, 2009) приведены термодинамические параметры кипящей воды и сухого насыщенного пара (удельный объём v, энтальпия h, теплота парообразования r, энтропия s).
ДИАГРАММЫp-v и Т-v ДЛЯ ВОДЫИ ВОДЯНОГО ПАРА.
Процесс нагревания и испарения воды при различных давлениях, в том числе и ниже атмосферного, показан на «диаграммах p-v и Т-v для воды и водяного пара», изображённых на рис. 2.
На рис. 2 показана диаграмма p-v воды и водяного пара, на которой рассмотрена изобара ad. Точка а соответствует состоянию воды при температуре 00С. В результате изобарного процесса ab подвода теплоты температура воды повышается, а удельный объем увеличивается. При температуре, соответствующей выбранному давлению, в точке b вода закипает.
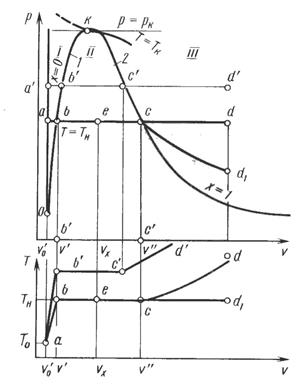
Рис.2. Диаграммы p-v и T-v для воды и водяного пара
Кипение воды сопровождается бурным парообразованием по всему объему жидкости. Процесс парообразования идет на участке изобары bc при постоянной температуре, т.е. участок bc одновременно является изотермой и изобарой. Полное испарение воды произойдет в точке с, где степень сухости пара равна единице, а в точке b степень сухости пара равняется нулю. При большем давлении описанный процесс может быть представлен зависимостью a’d’.
Область I соответствует нагреваемой воде, область II – насыщенному пару, область Ш – перегретому пару. Эти области разделяет нижняя пограничная кривая1, где степень сухости равна нулю, и верхняя пограничная кривая 2, где степень сухости пара равна единице. Между кривыми 1 и 2 располагается область влажного насыщенного пара, в которой в равновесии находятся две фазы – жидкость и пар.
Критическая точка К – конечная точка фазового перехода жидкость – пар. При температурах выше критической существование вещества в двухфазном состоянии невозможно. Параметры критической точки: давление pk = 22,064 МПа; удельный объем vk = 0,03106 м3/ кг; абсолютная температура Tk = 647,096 К (373,946 С).