Однако данные Marusawa H. C соавт. о наличии интегрированной в геном клетки вирусной ДНК у больных хроническим гепатитом и у некоторых переболевших острым гепатитом В, у которых произошла элиминация HBsAg при наличии анти-HBc-антител и даже изолированных анти-HBs-антител, ставят под сомнения существующие представления.
С гепатитом В может ассоциироваться еще один тип патологии – гепатит D. Он вызывается РНК-содержащим вирусом, репликация которого невозможна без наличия ВГВ-инфекции. Именно это определяет существование двух форм гепатита D – коинфекции (при одновременном инфцировании HBV и ВГD) и суперинфекции (инфицирование ВГD- носителя HBV). Клинически гепатит D протекает тяжелее, чем В, и именно он в значительной степени определяет летальность при последнем.
Культуральные свойства. ВГВ не культивируется на куриных эмбрионах, не обладает гемолитической и гемагглютинирующей активностью. Культивируется только в культуре клеток, полученной из ткани первичного рака печени в виде персистирующей инфекции, без оказания цитопатического и цитолитического действий и с малым накоплением вирионов. К вирусу чувствительны приматы: гориллы, шимпанзе, африканские зеленые мартышки.
Иммунитет. Будет рассмотрен на следующем занятии.
Профилактика. С 1986 г. в практику мирового здравоохранения для профилактики гепатита В введена рекомбинантная вакцина.
Вирус гепатита С относится к семейству Flaviviridae, роду Hepacivirus. По мнению многих авторов, гепатит С в настоящее время является центральной проблемой вирусных гепатитов. Кроме того его возбудитель представляет одну из основных причин цирроза печени и гепатоцеллюлярной карциномы.
Вирус является патогенным только для человека.
Он реплицируется преимущественно в гепатоцитах, но не обладает прямым цитопатическим свойством, способствуя формированию персистентной инфекции. Помимо заболеваний печени HCV-инфекция может вызывать и различные внепеченочные проявления, включая смешанную криоглобулинемию, гломерулонефрит, кожные высыпания, поражения глаз и В-клеточную лимфому.
К настоящему времени вирусом гепатита С инфицировано около 170 млн. человек в мире, в том числе 250000-350000 ежегодно умирают от HCV-обусловленных заболеваний. В области лечения и профилактики осложнений гепатита С большая роль отводится противовирусной терапии, эффективность которой достигает 40-50% [78].
Массовое распространение инфекции, чрезвычайная способность к
хронизации (до 90% случаев острого гепатита заканчиваются развитием хронического), высокая изменчивость вируса, и, как следствие, отсутствие сильного специфического иммунитета и доступной модели для изучения инфекции, а также непреодолимые на сегодняшний день трудности в создании вакцины против гепатита С определяют актуальность проблемы.
HCV классифицирован как представитель семейства Flaviviridae, род Hepacivirus, и содержит однонитчатую линейную «+»-нитевую РНК. К настоящему времени идентифицировано, как минимум, 6 генотипов HCV, обозначаемых римскими цифрами от I до VI (по H.Okamoto) или арабскими (по P.Simonds), а также 5 генотипов, выделенных в Юго-Восточной Азии. Кроме того внутри каждого типа существует множество субтипов (более 100) с уровнем гомологии между различными представителями 72-86%, а различия в последовательностях в пределах 1-14% определяют существование множественных вариантов (квазивидов). Присутствие в организме инфицированного человека одновременно миллионов квазивидов объясняет беспрерывное появление новых антигенных вариантов и «ускользание» вируса от иммунного надзора. Генотипы 1а и 1b являются наиболее распространенными и труднее всего поддаются лечению. Генотипы 2 и 4 распространены преимущественно в Центральной и Западной Африке, генотипы 3 и 6 – в Китае, Юго-Восточной Азии и Индии, где встречается также огромное количество подтипов этих вирусов.
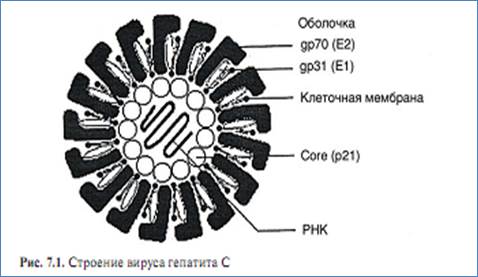
Вирион HCV имеет икосаэдрический тип симметрии и сформирован из однонитчатой «+»-нитевой РНК, упакованной в капсид.
Структурные протеины HCV представлены ядерным (core) протеином, который способен взаимодействовать с множеством протеинов клетки-хозяина и вмешиваться в транскрипцию генов, липидный метаболизм, апоптоз и запускать различные патологические процессы, а также оболочечными Е1- и Е2-протеинами, с антигенной лабильностью которого преимущественно ассоциируется изменчивость вируса. По данным Zibert A. (1997), антитела против пептидов, кодируемых гипервариабельной зоной HVR1 участка генома, ответственного за синтез белка Е2, блокируют взаимодействие HCV с клеткой.
Неструктурные протеины (р7, NS2, NS3, NS4A, NS4B, NS5A, NS5B), в основном, являются ферментами и необходимы для репликации вируса. Из них NS5B (центральный компонент HCV-репликазы) рассматривается как важная цель противовирусных интервенций.
Репликативный цикл HCV (рис. 24) начинается с адсорбции вируса на специфических рецепторах клеток. Предполагается, что в формирование рецепторного комплекса вовлечены тетраспанин CD81, “scavenger”-рецептор BI (SR-BI), молекулы адгезии DC-SIGN и L-SIGN, а также липопротеиновый рецептор низкой плотности (LDL). Теоретически данные молекулы могут стать одними из мишеней для противовирусных средств при гепатите С.
Собственно репликация вируса к настоящему времени изучена относительно плохо вследствие отсутствия вплоть до недавнего времени высокочувствительных клеточных структур, однако предполагается, что репликативный цикл типичен для флавивирусов.
В качестве потенциальных мишеней рассматриваются также белки NS3 (мультифункциональный протеин семейства сериновых протеаз, имеющий несколько функционально активных доменов) и NS5A (фосфорилированный Zn-содержащий металлопротеин), участвующий в регуляции синтеза интерферона. Несмотря на то, что роль NS5A в репродукции вируса окончательно не определена, имеются предположения о том, что он ингибирует один или несколько клеточных белков, участвующих в начальных стадиях противовирусного действия интерферона.

Репликативный цикл вируса гепатита С.
Резистентность к терапии интерферонами ассоциируется с оболочечным белком Е2, неструктурными протеинами NS 3/4A и NS5A, однако специфические мутации определены только для последнего. Конформация NS3, связанной с кофактором NS4A (ответственным за протеолитическую активность фермента), интенсивно изучалась в целях создания препарата, способного воздействовать на эту мишень. Тем не менее, малые размеры активного сайта связывания субстрата сделали эту задачу по разработке этого препарата более сложной, чем в случае с ВИЧ. Наиболее перспективными ингибиторами протеазы HCV являются цилупревир, телапревир, боцепревир и др.
Культуральные свойства. ВГС не культивируется на куриных эмбрионах, не обладает гемолитической и гемагглютинирующей активностью. Экспериментальной моделью является шимпанзе. Трудно адаптируется к культивированию в культуре клеток.
Резистентность. Относительно нестабилен при хранении при комнатной температуре. ВГС чувствителен к эфиру, детергентам, формальдегиду, УФ-лучам; нагревание при 60?С инактивирует вирус в течение 10 ч, при 100?С в течение 2 мин.
Эпидемиология. Заражение ВГС аналогично заражению ВГВ. Однако для заражения ВГС требуется большая заражающая доза, чем при гепатите В. Наиболее часто ВГС передается при переливаниях крови (2/3 случаев), половым путем, при использовании загрязненных инструментов. Трансплацентарная передача возможна только в случае высокой вирусемии. Вирус широко распространен. В мире более 1/3 населения инфицировано ВГС.
Клиническая картина. Инкубационный период 6-8 нед. Клиническое течение острого гепатита С более легкое, чем гепатита В. Часто встречаются безжелтушные формы, выявить заболевание при которых можно по повышению активности аланинаминотрансаминазы в крови. Однако в 60% случаев процесс переходит в хроническое состояние с развитием цирроза и первичного рака печени. Переход в хроническое состояние в 50% случаев связан, с одной стороны, с отсутствием выраженного CD4-клеточного иммунного ответа, а также возможностью вируса избегать нейтрализующего действия антител вследствие большой изменчивости генома. Предполагается, что ВГС представляет собой персистирующую вирусную инфекцию, при которой вирус персистирует в лимфатических узлах. При ослаблении CD4-иммунного ответа происходит реактивация вируса. Выраженный CD4-иммунньIЙ ответ, направленный против эпитопа на NS3-белке, обусловливает выздоровление.
Профилактика и лечение. Для неспецифической профилактики проводят те же мероприятия, что и при гепатите В. Для лечения применяют интерферон и рибовирин. Специфическая профилактика не разработана.
Вирус гепатита Е
Вирус гепатита Е (HEV) вызывает гепатит Е - инфекцию с фекально-оральным механизмом передачи. Вирус был открыт в 1983 г. советским ученым акад. М.С. Балаяном в опытах самозаражения экстрактами фекалий 9 больных гепатитом ни А, ни В. Вирус принадлежит к отдельному роду Hepevirus. Заболевание особенно распространено в странах Средней Азии.
Структура. Вирус не имеет липидной оболочки. Нуклеокапсид сферической формы размером 27-34 нм. Геном вируса представлен однонитевой плюс-РНК, которая кодирует РНК-зависимую РНК-полимеразу, папаиноподобную протеазу и трансмембранный белок, обеспечивающий проникновение вируса в клетку.
Эпидемиология и клиническая картина. Источник инфекции - больные люди. Главный путь передачи инфекции водный. Инкубационный период от 2 до 6 нед. Заболевание сопровождается умеренным поражением печени, интоксикацией и желтухой. Про- гноз, как правило, благоприятный, за исключением беременных, у которых смертность от гепатита Е составляет 16-20%. В последнее время вирус гепатита Е был выделен у некоторых животных (свиней, оленей, крупного рогатого скота, птиц и др.), что предполагает возможность передачи вируса от животных человеку.
Иммунитет. После перенесенного заболевания формируется стойкий иммунитет.
Микробиологическая диагностика. Применяют серологический метод. В сыворотке и плазме крови определяют IgG- и IgM- антитела к вирусу. Кроме того, методом ПЦР определяют вирусную РНК в сыворотке крови во время острой фазы инфекции.
Лечение и профилактика. Лечение симптоматическое. Беременным вводят специфический иммуноглобулин. Неспецифическая профилактика направлена на улучшение санитарно-гигиенических условий и снабжение качественной питьевой водой. Создана неживая цельновирионная вакцина. Испытываются живая и генно- инженерная вакцины.
Вирус гепатита G
Малоизученный вирус, предположительно относящийся к семейству Flaviviridae, роду Hepacivirus. Для его репликации требуется ВГС. Считается, что вирус гепатита G обладает лимфотропностью, вызывает персистирующие формы инфекции.