Гидроксикарбонильными называют соединения, содержащие в молекуле одновременно гидроксильную и альдегидную (или кетон- ную) группы.
В соответствии с этим различают гидроксиальдегиды и гидроксикетоны.
Наиболее известными представителями этих классов соединений являются глицериновый альдегид и дигидроксиацетон, играющие в виде фосфатов большую роль в биохимических процессах.
Глицериновый альдегид (глицеральдегид). Использование глицеринового альдегида в качестве конфигурационного стандарта рассмотрено выше.
Внутримолекулярная циклизация. Для гидроксикарбонильных соединений с достаточно удаленными друг от друга функциональными группами возможна внутримолекулярная циклизация (моносахариды). Образованием циклических полуацеталей объясняется таутомерия углеводов.

Гидроксикислоты
Гидроксикислотами называют соединения, содержащие в молекуле одновременно гидроксильную и карбоксильную группы. В алифатическом ряду по взаимному расположению функциональных групп различают α-, β-, γ- и т. д. гидроксикислоты. Буквой греческого алфавита указывают положение другой функциональной группы относительно карбоксильной, при этом отсчет ведется от ближайшего к карбоксильной группе атома углерода, т. е. от атома С-2. Отметим, что в заместительной номенклатуре для замещенных карбоновых кислот локанты α-, β-, γ- и т. д. не употребляются.
Кислотно-основные свойства. В гетерофункциональных соединениях в зависимости от природы функциональных групп и их местоположения в молекуле возможно усиление или, наоборот, ослабление некоторых свойств, характерных для монофункциональных соединений. Например, кислотность гидроксикислот выше, чем незамещенных кислот.
α -Гидроксикислоты. У α-гидроксикислот функциональные группы близки, но внутримолекулярного взаимодействия между ними не происходит из-за неустойчивости трехчленных циклов, которые могли бы при этом образоваться. При нагревании α-гидроксикислоты претерпевают межмоле- кулярную циклизацию с образованием продуктов, называемых соответственно лактидами.
Молочная кислота известна как продукт молочнокислого брожения лактозы, содержащейся в молоке, и других углеводов, входящих в состав овощей и плодов.
В организме L-(+)-молочная кислота является одним из продуктов превращения глюкозы (гликолиза). Она накапливается в мышцах при интенсивной работе, вследствие чего в них возникает характерная боль. Причина накопления молочной кислоты – недостаток кислорода, что вызывает восстановление пировиноградной кислоты с участием НАДН в молочную.

Во время отдыха запасы кислорода возобновляются, и молочная кислота окисляется снова в пировиноградную кислоту.
β -Гидроксикислоты. Характерное общее свойство этих гетерофункциональных кислот заключается в способности к элиминированию молекулы воды с образованием α,β-ненасыщенных кислот.

Реакции элиминирования протекают в мягких условиях. Это объясняется высокой протонной подвижностью α-атома водорода, обусловленной электронным влиянием двух электроноакцепторных
групп (Х и СООН).

γ -Гидроксикислоты. Эти кислоты, как и кислоты с δ-расположением функциональных групп, при нагревании претерпевают внутримолекулярную циклизацию. Из гидроксикислот при этом образуются циклические сложные эфиры - лактоны. Лактоны легко образуются уже при незначительном нагревании, а также в кислой среде.
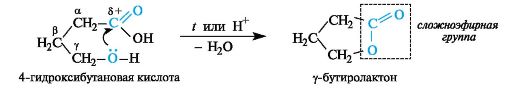
4-Гидроксимасляная кислота (традиционно называемая γ-гидроксимасляной кислотой, ГОМК) применяется в виде натриевой соли как снотворное средство, а также в анестезиологии.
Многоосновные гидроксикислоты. Рассматриваемые в этом разделе яблочная, лимонная, изолимонная кислоты, а также щавелевоуксусная кислоты являются участниками цикла трикарбоновых кислот, называемого также циклом лимонной кислоты, или циклом Кребса. Это универсальный этап окислительного катаболизма углеводов и других соединений в присутствии кислорода.
Яблочная кислота в значительных количествах содержится в незрелых яблоках, рябине, фруктовых соках. В организме L-яблочная кислота образуется путем гидратации фумаровой кислоты.

Лимонная кислота содержится в плодах цитрусовых (лимоны, апельсины), винограде, крыжовнике, а также в листьях табака.
При дегидратации лимонной кислоты как β-гидроксикарбоновой кислоты получается цисаконитовая кислота, которая далее гидратируется с образованием изолимонной кислоты.

Винные кислоты - представители дигидроксидикарбоновых кислот, содержат два асимметрических атома углерода и поэтому должны были бы существовать в виде четырех стереоизомеров, но в действительности известны три стереоизомера.
D -(+)-Bинная кислота, или обыкновенная винная кислота, известна под названием виннокаменной кислоты. Она содержится в винограде, рябине. Кислая калиевая соль трудно растворима в воде. L-(-)-Винная кислота в очень небольшом количестве содержится в виноградных винах.
Мезовинная кислота в природе не встречается; она частично образуется при длительном нагревании в щелочном растворе любого из ее стереоизомеров.

Оксокислоты
Оксокислотами называют соединения, содержащие в молекуле одновременно карбоксильную и альдегидную (или кетонную) группы.
В соответствии с этим различают альдегидокислоты и кетонокислоты.
Простейшей альдегидокислотой является глиоксалевая (глиоксиловая) кислота, которая обычно существует в виде гидрата (НО)2СНСООН. Она содержится в недозрелых фруктах, но по мере созревания ее количество уменьшается.
Пировиноградная кислота является одним из промежуточных продуктов молочнокислого и спиртового брожения углеводов. Своим названием пировиноградная кислота обязана тому, что впервые была выделена при пиролизе виноградной кислоты. Пировиноградная кислота декарбоксилируется при нагревании с разбавленной и декарбонилируется (отщепляет СО) - с концентрированной серной кислотой.

Щавелевоуксусная кислота одновременно является α- и β-оксокислотой. Она образуется при окислении яблочной кислоты.

Ацетоуксусная кислота - представитель β-оксокислот. В свободном состоянии представляет сиропообразную жидкость, медленно выделяющую диоксид углерода.

Как продукт окисления 3-гидроксимасляной кислоты наряду с продуктами ее превращений накапливается в организме больных сахарным диабетом (так называемые ацетоновые, или кетоновые тела.

Ацетоуксусный эфир - жидкость с приятным фруктовым запахом. Ацетоуксусный эфир представляет собой смесь двух изомеров - кетона (92,5%) и енола (7,5 %), находящихся в таутомерном равновесии.

Бензойная кислота. Применяется в виде натриевой соли как отхаркивающее средство. В свободном виде бензойная кислота встречается в некоторых смолах и бальзамах, а также в клюкве, бруснике, но чаще содержится в связанном виде, например в виде N-бензоильного производного аминоуксусной кислоты, называемого гиппуровой кислотой. Эта кислота образуется в печени из бензойной и аминоуксусной (глицин) кислот и выводится с мочой. В клинической практике по количеству гиппуровой кислоты в моче больных (после приема бензоата натрия) судят об эффективности обезвреживающей функции печени.

и-Аминофенол и его производные. Как гетерофункциональное соединение п -аминофенол может образовывать производные по каждой функциональной группе в отдельности и одновременно по двум функциональным группам. Сам п-аминофенол ядовит; интерес для медицины представляет его производное - парацетамол, оказывающий анальгетическое (обезболивающее) и жаропонижающее действие.

п-Аминобензойная кислота (ПАБК) и ее производные. Эфиры ароматических аминокислот способны в той или иной степени вызывать местную анестезию. Особенно заметно это свойство у пара -производных. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (2-диэтиламиноэтиловый эфир ПАБК). Новокаин применяют в виде соли (гидрохлорида), что связано с необходимостью повышения его растворимости в воде.

Салициловая кислота и ее производные. Салициловая кислота- о-гидроксибензойная кислота- относится к группе фенолокислот. Как соединение с орто- расположением функциональных групп она декарбоксилируется при нагревании с образованием фенола. Салициловая кислота проявляет антиревматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рKа 3,0) вызывает раздражение желудочно-кишечного тракта и поэтому применяется только наружно. Внутрь применяют ее производные - соли или эфиры.
Салициловая кислота способна образовывать производные по каждой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по карбоксильной группе - метилсалицилат, фенилсалицилат (салол), а также по гидроксильной группе - ацетилсалициловая кислота (аспирин).
Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике.
Из других производных салициловой кислоты большое значение имеет п -аминосалициловая кислота (ПАСК) как противотуберкулезное средство. ПАСК является антагонистом п -аминобензойной кислоты, необходимой для нормальной жизнедеятельности микроорганизмов.

Сульфаниловая кислота и ее производные. Сульфаниловая (п-аминобензолсульфоновая) кислота существует в виде диполярного иона.

Амид сульфаниловой кислоты (сульфаниламид), известный как стрептоцид, является родоначальником группы лекарственных средств, обладающих антибактериальной активностью и называемых сульфаниламидами.
