O
|
|

 H2N – CH2 – C
H2N – CH2 – C
|
OH
 | |||||
 | |||||
 | |||||
ВНИМАНИЕ ИНФОРМАЦИЯ!
Способность алифатических аминокислот образовывать соли с солями тяжелых металлов используется для идентификации аминокислот (качественная реакция). При взаимодействии аминокислот с сульфатом меди в щелочной среде образуются соли меди, в которых ион меди связан дополнительными валентностями с атомами азота, образуя комплексный ион темно-синего цвета.

Провели качественную реакцию на алифатические аминокислоты с сульфатом меди в щелочной среде (реакция основана на способности образовывать комплексные соединения хелатного типа за счет карбоксильной и a-аминогруппы с катионом Cu2+).
Реакция с нингидрином является качественной на аминокислоты алифатического ряда:
 | |||||
 | |||||
| |||||


|
|
NH2
Аминокислота Нингидрин
|





|
 |
+ R – C = O + CO2 + 3 H2O
|
H
Дикетогидриндилиден-
дикетогидриндамин
(сине-фиолетовый)
Наиболее важная реакция аминокислот – полимеризация. Она лежит в основе образования белков, происходит в живых организмах, катализируется ферментами.
Аминогруппа одной молекулы вступает во взаимодействие с карбоксильной группой другой молекулы.

(амидная связь)
СПЕЦИФИЧЕСКИЕ РЕАКЦИИ АМИНОКИСЛОТ (отношение к нагреванию):
Наличие в молекулах аминокислот двух различных функциональных групп приводит к появлению ряда специфических свойств, которые в общих чертах сходны со свойствами гидроксикислот.
Группа COOH- электрофильный центр молекулы и группа-NH2- нуклеофильный центр, способны взаимодействовать. Это взаимодействие в зависимости от расположения функциональных групп в молекуле может протекать межмолекулярно или внутримолекулярно.
1. α- аминокислоты – вступают в межмолекулярное взаимодействие.
В результате образуется устойчивый шестичленный цикл – ди-кетопиперазин. Способны гидролизироваться до исходных α - аминокислот.

2. β-аминокислоты – отщепляют аммиак, в результате чего образуются α, β, -непредельные кислоты.

3. γ-аминокислоты – вступают во внутримолекулярное взаимодействие.
В результате образуются циклические амиды – γ-лактамы. Они способны
гидролизоваться до исходных аминокислот.

6. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ АМИНОКИСЛОТ, ПРИМЕНЯЕМЫЕ В МЕДИЦИНЕ.
КИСЛОТА ГЛЮТАМИНОВАЯ – играет важную роль в жизнедеятельности организма, участвует в белковом и углеводородном обмене, стимулирует окислительные процессы, способствует обезвреживанию и выведению из организма аммиака, повышает устойчивость организма к гипоксии.
В медицинской практике глютаминовая кислота находит применение при лечении заболеваний ЦНС: эпилепсии, психозов, реактивных состояний, протекающих с явлением истощения, депрессии и др.
В педиатрии препарат применяют при задержке психического развития различной этиологии, церебральных параличей, болезнь Дауна.
АНЕСТЕЗИН - одно из самых первых синтетических соединений, применяемых
в качестве местноанестезирующих средств. Анестезин является активным поверхностным местноанестезирующим средством. Его широко применяют в виде мазей, присыпок и др.
лекарственных форм.
АМИНАЛОН - стимулирует обучение, улучшает процесс запоминания и воспоминания – при расстройствах памяти, при черепно-мозговых травмах, при нарушении мозгового кровообращения.
Показаны детям с задержкой умственного развития.
ГЛИЦИН (ГЛИКОКОЛ) – снимает раздражительность, улучшает сон, уменьшает депрессивности.
ГИСТИДИН – используют в медицине для лечения гепатитов, язвенных процессов в желудке и двенадцатиперстной кишке.
МЕТИОНИН – применяют для лечения и предупреждения заболеваний и токсических поражений печени; для лечения дистрофии, возникающей в результате белковой недостаточности у детей и взрослых после инфекционных заболеваний.
ЦИСТЕИН – применяют для задержки катаракты и просветления хрусталика глаза при начальных формах возрастной, миопической, лучевой и контузионной катарактах.
7. ЛИТЕРАТУРА:
1) Л.М. Пустовалова «Органическая химия», Ростов-на-Дону «Феникс», 2005г.
2) Н.А. Тюкавкина, Ю.И. Бауков «Биоорганическая химия», М. «ДРОФА», 2004г.
3) В.П. Комов, В.Н. Шведова «Биохимия», М. «ДРОФА», 2004 г.
4) М.Д. Машковский «Лекарственные средства», М. «Новая волна», 2005 г.
ПРИЛОЖЕНИЕ
a -аминокислоты входящие в состав белков.
Общая формула: R – CH – COOH
|
NH2
| Название | Формула радикала | ||||||||||||||||||
| Глицин | Н – | ||||||||||||||||||
| Аланин | СН3 – | ||||||||||||||||||
| Валин | СН3 – СН – | СН3 | ||||||||||||||||||
| Лейцин | СН3 – СН – СН2 – | CH3 | ||||||||||||||||||
| Изолейцин | CH3 – CH2 – CH – | CH3 | ||||||||||||||||||
| Серин | HO – CH2 – | ||||||||||||||||||
| Треонин | CH3 – CH – | OH | ||||||||||||||||||
| Цистин | HOOC – CH – CH2 – S – S – CH2 – | NH2 | ||||||||||||||||||
| Цистеин | HS – CH2 – | ||||||||||||||||||
| Метионин | CH3 – S – CH2 – CH2 – | ||||||||||||||||||
| Аргинин | H2N – C – NH – CH2 – CH2 – CH2 – || NH | ||||||||||||||||||
| Лизин | H2N – CH2 – CH2 – CH2 – CH2 – | ||||||||||||||||||
| Аспарагиновая кислота | HOOC – CH2 – | ||||||||||||||||||
| Глутаминовая кислота | HOOC – CH2 – CH2 – | ||||||||||||||||||
| Фенилаланин |    – CH2 –
– CH2 –

| ||||||||||||||||||
| Тирозин |   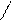   HO – – CH2 –
HO – – CH2 –
| ||||||||||||||||||
| Триптофан |     – CH2 – – CH2 –
H | ||||||||||||||||||
| Гистидин |
   – СН2 – – СН2 –
Н | ||||||||||||||||||
| Пролин |
Н | ||||||||||||||||||
| Оксипролин |
Н |
| 16 пуст. | 1 облож. | 15 пуст | |
| 14 пуст. | 13 пуст | ||









 НО –
НО –