Электрические характеристики биожидкостей
https://megapredmet.ru/1-70460.html
Первое упоминание об исследовании электрической проводимости биологических объектов принято относить к работам В. Томсона, датированным 1880 г. Вильям Томсон (W. Thomson, 1824-1907), с 1892 г. Лорд Кельвин – английский физик, президент Лондонского королевского общества (1890-1895). Основополагающие результаты в исследовании электропроводности биологических тканей были получены в начале и середине ХХ в. Установление типичных значений удельного сопротивления и диэлектрической проницаемости тканей, органов и жидких сред живого организма, а также выявление и частичное объяснение зависимости проводимости и диэлектрической проницаемости биологических жидкостей и клеточных суспензий от частоты зондирующего тока связаны с именами Г. Фрике, К.Коула, Х. Шванна.
Электропроводность биологической ткани – это количественная характеристика способности биомембран, клеток и тканей проводить электрический ток.
Биологические ткани являются композиционными средами, поскольку одни структурные элементы обладают свойствами проводников а другие – диэлектриков. При анализе действия ЭМП на живой организм его ткани принято рассматривать как среду, образованную проводниками и диэлектриками.

Таким образом, особенность биологических тканей состоит в том, что они обладают свойствами проводников и диэлектриков. Наличие свободных ионов в клетках и тканях обусловливает проводимость. Диэлектрические свойства и величина диэлектрической проницаемости e определяются структурными компонентами биологических тканей и явлениями поляризации. Характерная особенность биологических тканей, как многокомпонентных сложноструктурированных сред – наличие высокой поляризационной ёмкости, высокой диэлектрической проницаемости на низких частотах внешнего воздействующего ЭМП.
При постоянном зондирующем токе закон Ома для биологической ткани (рис. 1), как проводника электрического тока, можно записать в виде I (t)=(U - E (t))/ R, где U – приложенное напряжение, E (t) – возникающая в ткани противо-ЭДС, R – эквивалентное активное сопротивление цепи «электрод-биообъект-электрод». Уменьшение во времени тока через биоткань обусловлено явлениями поляризации. При прохождении постоянного тока через биологическую ткань в ней возникает нарастающая до некоторого предела ЭДС противоположного направления, которая уменьшает приложенную к ткани эффективную ЭДС, что приводит к уменьшению тока.
Характеристикой поляризации является время релаксации t, соответствующее максимальной частоте внешнего поля, которую индуцированные диполи способны «отслеживать» своими поворотами на 180°, «противодействуя» внешнему полю. Выделяют несколько видов поляризации, возникающих во внешнем ЭМП:
1) электронная поляризация; определяется смещением электронов на своих орбитах относительно положительно заряженного ядра; в результате возникает индуцированный диполь с направлением вектора дипольного момента, противоположным направлению внешнего поля; характерна для неполярных молекул H2, O2, N2;t1=10-16 – 10-14 с;
2) ионная поляризация; вызывается смещением иона относительно кристаллической решётки; характерна для кристаллических диэлектриков, таких как NaCl; t2=10-14 – 10-12 с;
3) дипольная или ориентационная поляризация; характерна для полярных молекул (воды, спиртов, малых органических молекул), которые под действием внешнего поля ориентируются в соответствии с этим полем; t3=10-13 – 10-7 с;
4) макроструктурная поляризация; связана с чередованием слоев с высокой и низкой электропроводностью, скоплением свободных зарядов на границах слоев с разной электропроводностью, а в биотканях – и с наличием крупных органических молекул – белков; t4=10-8 – 10-3 с;
5) другие виды поляризации, связанные с поляризационными явлениями на границах электрод-электролит-биоткань; t5=10-3 – 100 с.
Для импедансных измерений при исследовании биологических тканей наименее существенную роль играют электронная и ионная виды поляризации.
ЭДС поляризации обусловливает высокое удельное сопротивление (r=106-107 Ом*см) тканей постоянному току. Величина поляризационной ёмкости (cп) может быть вычислена по следующей формуле:
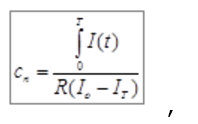
где I 0 – начальное значение тока; IT – установившееся через время T значение тока (рис. 1).
При прохождении переменного тока электрические свойства биологических тканей описываются не только активным, но и емкостным сопротивлением.
Все явления поляризации могут быть описаны с помощью диэлектрической проницаемости вещества. Диэлектрическая проницаемость e характеризует уменьшение величины электрического поля в веществе по сравнению с величиной электрического поля в вакууме. Если Е 0 – напряженность однородного поля, образуемого некоторыми зарядами в вакууме, а Е – напряжённость поля, создаваемого этими же зарядами, в веществе, то
 = Е 0/ Е.
= Е 0/ Е.
Электрическая модель биологического объекта (исследуемого образца биологической ткани) может быть представлена упрощённо в виде комбинаций поляризационных ёмкостей (C) и активных сопротивлений (R): последовательной (рис. 2, а) и параллельной (рис. 2, б) схемами замещения [3-5].

Реактивное ёмкостное сопротивление определяется по формуле
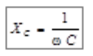 ,
,
где w - скорость изменения фазы тока (круговая частота); С – эквивалентная ёмкость биоткани на определенной частоте.
Электрическое сопротивление образца биоткани (или между какими-либо участками тела) представляет собой комплексное сопротивление – импеданс (Z). Импеданс биоткани для последовательного соединения C и R определяется как

Импеданс биоткани и его составляющие, активная и ёмкостная, изменяются с изменением частоты тока, на котором производится измерение.
Проводимость органов и тканей обусловлена присутствием в них ионов, которые являются свободными зарядами, создающими в организме ток проводимости под действием электромагнитных полей, как создаваемых внешними источниками, так и генерируемых живыми клетками. Ток проводимости в живых тканях зависит от их типа, вида и возраста организма, а для тканей, клетки которых представляют собой волокна, - от их ориентации относительно направления ЭМП.
Существенное влияние на электропроводность биотканей и биологических объектов (БО) оказывает содержание в них воды. К тканям с низким содержанием воды, около 15% массы ткани, относятся костная и жировая. Их удельная электропроводность невелика: L=0,02 – 0,03 См/м (удельное сопротивление r=1/L=30-50 Ом×м) на частотах ЭМП ниже 1 кГц и около L=0,2 – 0,3 См/м (удельное сопротивление r=3-5 Ом×м) на более высоких частотах, вплоть до 10 ГГц [2].
В тканях с большим содержанием воды (от 70 до 80% массы ткани – в почках, печени, сердечной и скелетной мышцах, головном мозге) удельная электропроводность примерно на порядок выше - до 1 См/м.
Электропроводность самой воды мала. Так у дистиллированной воды при комнатной температуре L=10-5 – 10-4 См/м (r=104 – 105 Ом×м). Растворение в воде солей резко повышает электропроводность. Например, изотонический раствор NaCl в воде (0,85% или 0,15М) при температуре тела человека (примерно 37°С) имеет удельную электропроводность L=1,5 См/м (r=0,7 Ом×м). Примерно такой же удельной электропроводностью обладают биологические жидкости, не содержащие клеток: плазма крови и ликвор – 1,5 См/м (r=0,7 Ом×м), желчь – 1,7 См/м (r=0,6 Ом×м) [2].
За счёт форменных элементов (эритроцитов, лейкоцитов, тромбоцитов) цельная кровь обладает меньшей удельной электропроводностью, чем плазма крови, L=0,5 – 0,7 См/м (r=1,4 – 2,0 Ом×м). У целых органов L в 4-6 раз ниже, чем у жидкостей, выделенных из них. Причиной несовпадения являются малые объёмы, занимаемые свободными электролитами в органах и тканях животных. В клетке электролиты заключены в мельчайшие отсеки, компартменты, образованные
биомембранами, составляющими более 50% массы клетки. Каждый клеточный органоид – тоже компартмент. Его содержимое и окружающий цитозоль обладают относительно высокой электропроводностью, тогда как разделяющая их мембрана является диэлектриком (удельная электропроводность мембраны L=10-11 См/м). Однако, на высоких частотах диэлектрическими свойствами биотканей можно пренебречь.
В целом, электропроводность живых тканей определяется, прежде всего, электрическими свойствами крови, лимфы, ликвора, межклеточной и внутриклеточной жидкостей. Причем подвижность ионов в биологических жидкостях примерно такая же, как и в растворах соответствующих солей, приготовленных на дистиллированной воде.
Живым тканям свойственна зависимость электропроводности от частоты воздействующего ЭМП. Это явление получило название дисперсии электропроводности. С повышением частоты увеличивается и удельная электропроводность. Дисперсия электропроводности установлена для различных биологических тканей в низкочастотном и высокочастотном диапазонах. При изменении частоты ЭМП от 40 Гц до 200 кГц удельная электропроводность мозга кролика увеличивается в 20 раз. На средних частотах дисперсия электропроводности менее выражена, на высоких – проявляется отчетливо. Так, при изменении частоты ЭМП от 25 МГц до 8,5 ГГц сопротивление скелетной мышцы снижается примерно в 10 раз. На 10 ГГц удельная электропроводность жировой ткани достигает 0,3-0,4 См/м (r=2,5 – 3,3 Ом×м), а у костной – 0,5-2,7 См/м (r=0,4 – 2,0 Ом×м) [2].
Дисперсия электропроводности присуща всем неоднородным средам, а не только биологическим. Она наблюдается в том диапазоне частот ЭМП, которые соответствуют характеристическим частотам (nx=1/t) заряженных частиц, входящих в состав той или иной среды. Дисперсия электропроводности – специфическое свойство не только биологических систем, но и других неоднородных сред.
Характерная особенность живых тканей состоит в том, что у них зависимость удельной электропроводности от частоты гораздо отчётливее, чем у сред с менее сложной организацией, и обнаруживается в широком частотном диапазоне. Это обусловлено сложной, мембранной, структурой тканей и большим разнообразием релаксационных способностей их заряженных частиц. Причём такое разнообразие связано как с различиями в размерах, так и с влиянием на их подвижность биологических мембран.
Повреждение клеточных мембран стирает в значительной мере грань между живыми тканями и органическими электролитами в дисперсии электропроводности на низких частотах.
Диэлектрические свойства биотканей определяются присутствием в них малых полярных молекул воды, полярных макромолекул, белков, находящихся в водной фазе, а также компартментализацией клеточных структур.
Компартментализация, обеспечивая оптимальные условия для внутриклеточных биохимических процессов, придаёт живым тканям сегнетоэлектрические свойства.
Физические среды, в которых чередуются слои с низкой и высокой удельной электропроводностью, ведут себя подобно сегнетоэлектрикам, если по обе стороны каждого слоя с низкой L присутствуют разноимённые электрические заряды. Такие структуры подобны доменам с одинаковой
ориентацией дипольных моментов. Внутриклеточная и межклеточная жидкости характеризуются L=0,5–1,0 См/м, а биомембраны - L=10-11 См/м.
Каждый органоид (компартмент) на мембране которого поддерживается разность потенциалов между внутри- и внекомпартментным содержимым, имеет значительный дипольный момент и подобен домену в сегнетоэлектрике. За счёт таких заряженных компартментов живые ткани обладают высокой диэлектрической проницаемостью (e). В постоянном электрическом поле она достигает нескольких десятков тысяч.
Как и всякому домену, внутриклеточному компартменту присуща характеристическая частота релаксации (nx). Применительно к диполям nxсоответствует максимальной частоте внешнего ЭМП, которую они способны воспроизвести своими
полными поворотами в нём, за счёт чего достигается максимально возможная компенсация внешнего поля собственным электрическим полем диэлектрика. Когда диполи уже не успевают совершать повороты на 180° вслед за изменениями направления вектора ЭМП по мере повышения его частоты, вектор уменьшается по абсолютной величине, что эквивалентно понижению e среды. Области резких изменений e при изменении частоты ЭМП называются областями дисперсии e.
При низких частотах дисперсия e обусловлена, по-видимому, поляризацией внутриклеточных компартментов («доменов»). Диапазон nx разных внутриклеточных компартментов находится в пределах от долей герца до 1 кГц. На более высоких частотах диэлектрические свойства биообъектов определяются полярными молекулами, сосредоточенными как в цитозоле, так и в клеточных мембранах. У разных белковых молекул nx
охватывает диапазон от 10 кГц до 100 МГц и зависит от их размеров, а также от вязкости окружающей среды. Эту зависимость выражает следующая формула:

где k – постоянная Больцмана, T – температура среды, в которой вращаются молекулы под действием ЭМП, h – вязкость среды, r – эффективный радиус полярной молекулы.
Важно отметить, что молекулы одинаковых размеров, пребывая в средах с разной вязкостью (например, в цитозоле и в биомембране), обладают неодинаковой nx.
В сверхвысокочастотных полях основной вклад в эти свойства вносит вода, обладающая очень высокой nx. Характеристическая частота релаксации внутриклеточной воды такая же, как и дистиллированной (nx»20ГГц). Именно в воде, входящей в состав живых тканей, происходят основные диэлектрические потери при действии на организм СВЧ-излучений, поскольку с nx воды совпадает частота сантиметровых радиоволн.

Таким образом, поляризация каждого из компонентов живой ткани имеет свою nx. Вблизи неё наблюдается резкое изменение e, которое прекращается, когда частота внешнего ЭМП начинает превосходить nx на порядок.
Неодинаковые величины nx разных тканевых компонентов, способных поляризоваться в ЭМП, обусловливают неравномерный ход кривой дисперсии диэлектрической проницаемости, отображающей зависимость e ткани от n электромагнитных колебаний, воздействующих на неё. На графике рисунка 3 можно выделить три участка, где кривая идёт круче, чем в промежутках. Эти участки называют областями дисперсии (зонами релаксации) и обозначают греческими буквами a, b и g [2, 5].
Первый участок (a- дисперсия живых тканей) соответствует низкочастотному диапазону (до 1кГц). Он отображает поляризацию внутриклеточных компартментов, с которыми связаны сегнетоэлектрические свойства живых тканей. В силу значительной инерционности релаксационных процессов в доменах-компартментах, вращение этих «гигантских диполей» запаздывает относительно перемен направления внешнего ЭМП даже на низких частотах, что проявляется в уменьшении e по мере повышения nx в низкочастотном диапазоне. Некоторый вклад в a-дисперсию вносит релаксация зарядов на фасциях, внутриорганных соединительнотканных прослойках, клеточных поверхностях.
Второй участок (b- дисперсия живых тканей) отображает изменение поляризации макромолекул по мере повышения частоты внешнего ЭМП. В скелетной мышце b-дисперсия наблюдается в диапазоне частот от 104 до 108 Гц. Снижение e по мере повышения n в этом диапазоне зависит от того, что всё менее крупные макромолекулы не успевают поворачиваться в соответствии с частотой внешнего ЭМП, когда она начинает превосходить nx той или иной полярной молекулы. Очевидно, что 108 Гц является частотой, соответствующей nx наименее инерционных макромолекул, а 104 Гц – наиболее инерционных макромолекул.
Третий участок (g- дисперсия живых тканей) приходится на n выше 1010 Гц, чему соответствуют частоты ориентационной поляризации молекул воды. Поскольку воде свойственно несколько значений nx, лежащих около 20ГГц, то изменение e на n > 1010 Гц имеет немонотонно убывающий характер. Диэлектрическая проницаемость уменьшается потому, что даже такие мелкие молекулы, как H2O, не успевают совершать повороты с частотой, соответствующей частотному диапазону g-дисперсии.
Под действием внешнего ЭМП в живых тканях, обладающих и диэлектрическими, и электропроводящими свойствами, возникают и токи смещения, и токи проводимости. В низкочастотном диапазоне тангенс угла диэлектрических потерь в большинстве тканей равен 20-40, но уже на n = 10 кГц он становится < 10. Следовательно, по мере повышения частоты ЭМП роль тока смещения в биологических эффектах электромагнитного излучения возрастает и становится ведущей на n выше 107 Гц. Сказанное хорошо иллюстрирует различные виды высокочастотной электротерапии: если при диатермии (n = 0,5 – 2 МГц) ткани нагреваются благодаря возникновению в них тока проводимости, то при УВЧ-терапии (n = 40 – 60 МГц) тепловой эффект связан, прежде всего, с током смещения. Можно показать, что при УВЧ-терапии именно ток смещения служит лечебным фактором.
Клеточные мембраны принято рассматривать по аналогии с диэлектриком в плоском конденсаторе. Тогда поведение мембран в ЭМП характеризует электрическая ёмкость, приведённая к 1 см2 мембранной поверхности. Эта величина (C м уд) называется удельной ёмкостью мембраны и измеряется в мкФ/ см2. Очень велика C м уд плазмолеммы гладкомышечного волокна млекопитающих – около 30 мкФ/ см2. Нервные волокна многих животных имеют плазматические мембраны, C м уд которых находится в пределах единиц мкФ/см2 [2].
Биоимпедансометрия
В настоящее время в импедансометрии биологических тканей принято рассматривать только две составляющих импеданса (полного сопротивления переменному току) ткани: активное сопротивление R и ёмкостное сопротивление XС [1-5]. Индуктивное сопротивление не учитывается.
Для оценки величины ёмкостного сопротивления, либо оценки величины диэлектрической проницаемости ткани принято использовать упрощённую формулу, определяя С по формуле плоского конденсатора:
, 
где ν – частота внешнего поля в Гц; d – толщина исследуемого образца ткани; s – эффективная площадь сечения образца.
Для биологических тканей характерно уменьшение импеданса с увеличением частоты, т.е. наблюдается частотная дисперсия импеданса [2,5]. Дисперсии L, e и Z не идентичны, но связаны.
Дисперсия импеданса отображает более широкий круг электромагнитных процессов в биотканях. Дисперсия Z сильнее зависит от разнообразных нарушений жизнедеятельности исследуемой ткани. По кривой дисперсии Z удаётся судить об уровне обмена веществ и его отклонениях от нормы. По упрощённому варианту исследования измеряют два значения импеданса: 1) на низкой частоте (Z НЧ при f £ 102 Гц) и 2) на высокой частоте (Z ВЧ при f > 106 Гц), - и определяют коэффициент поляризации K п = Z НЧ / Z ВЧ. Жизнеспособная ткань имеет высокие значения K п >1 [2].
В импедансометрии для диагностики периферического кровообращения и определения состава тела человека, наибольший интерес представляет область b-дисперсии, чаще - частоты тока в интервале от 50 кГц до 0,5 МГц. Частоты ниже 0,4 кГц не используются из-за эффекта электростимуляции тканей, а при значениях выше 0,5-1 МГц «стираются» различия между мягкими тканями и кровью, усложняется техника измерений.
Удельное сопротивление биологических тканей, определяемое для заданной частоты тока, может существенно изменяться под влиянием физиологических и патофизиологических факторов: почки и лёгкие изменяют электропроводность при различном крове- и воздухонаполнении, мышечные ткани – при различной степени сокращения мышц, кровь и лимфа – при изменении концентрации форменных элементов, белков и электролитов, очаги повреждения – в результате отёков или ишемий различной природы, опухолей и других причин. Это позволяет использовать биоимпедансометрию для количественной оценки состояния органов и систем организма при различных заболеваниях, а также для выявления изменений в тканях, вызываемых лекарственными, ортостатическими, физическими и другими нагрузками. Однако абсолютные значения импеданса не являются стабильными надёжными показателями, т.к. зависят от многих факторов и не могут рассматриваться как константы живой ткани. Наибольший интерес представляют изменения значений импеданса и его составляющих, а также относительные расчётные параметры.
Существует несколько разновидностей биоимпедансного анализа, которые классифицируются по следующим трём признакам: 1) по частоте зондирующего тока – одночастотные, двухчастотные многочастотные; 2) по объекту измерений – интегральные (объектом измерений служит значительная часть тела), локальные (измеряются отдельные участки тела или регионы), полисегментные (параметры всего организма устанавливаются на основе обработки результатов измерений составляющих его регионов); 3) по тактике измерений – одноразовые, эпизодические, мониторные; 4) по количеству измерительных каналов – одно-, двух- и многоканальные.
В биоимпедансометрии при работе на частотах от 50 кГц до 1 МГц для оценочных расчётов применяют формулы, основанные на использовании активного сопротивления R. Эти формулы базируются на простом соотношении для электрического сопротивления однородного изотропного проводника постоянного сечения:
, - где l – длина, S – площадь поперечного сечения, V – объём, r – удельное сопротивление проводника [1]. Проблема применения указанного соотношения к анализу живых систем состоит в том, что биологические ткани неоднородны по своему составу и обладают анизотропией. Например, проводимость мышц зависит от взаимной ориентации направления тока и мышечных волокон. Кроме того, площадь поперечного сечения тела может сильно варьировать вдоль направления зондирующего тока.
Формулы, применяемые в биоимпедансометрии, наряду с характеристиками импеданса, длины исследуемого участка тела расчётные формулы содержат дополнительные параметры, такие как пол, возраст, масса тела, этническая принадлежность, гематокрит и др. для повышения точности оценок (состава тела, ударных объемов крови и т.п.).
Важной характеристикой электрической проводимости тканей является отношение их ёмкостного и активного сопротивлений:

Полуокружность на рис. 4 (график Коула-Коула) описывает теоретическую зависимость между активным и реактивным сопротивлениями тканей при изменении частоты тока f от 0 до +¥. Верхняя точка полуокружности соответствует максимальному значению реактивного сопротивления тканей и характеристической частоте тока. Типичные значения XC и R при измерении импеданса всего тела составляют 20-80 Ом и 200-800 Ом соответственно. Значения j при частоте тока 50 кГц составляют в норме 7,6±1,0° у мужчин и 6,9±1,3° у женщин (пределы изменения от 3 до 10°). При увеличении частоты тока эта величина варьирует в более широких пределах. Пониженные значения XC связывают с нарушением диэлектрических свойств клеточных мембран и увеличением доли разрушенных клеток в тканях организма. Наоборот, повышенные значения ёмкостного сопротивления отражают более высокое функциональное состояние клеточных мембран и, следовательно, самих клеток. На основании этого полагают, что чем больше величина j, тем лучше состояние организма. Повышенные значения XC отражают более высокое содержание активной клеточной массы и трактуются в спортивной медицине как свидетельство тренированности. Николаев Д.В. с соавторами отмечают следующие результаты изучения величины фазового угла для различных популяций: 1) существует высокая корреляция между величиной j и массой тела, у детей с нормальным питанием; дети с пониженным питанием имеют более низкие значения j; 2) величина j снижена у пациентов с почечной недостаточностью (j<5°), что объясняется увеличением объёма внеклеточной жидкости и снижением объёма внутриклеточной жидкости [1].
Величина j в этом уравнении имеет название фазового угла, который характеризует сдвиг фазы переменного тока относительно напряжения [1,5].
Практическая часть