Белки
Задание 1: Напишите ответы на вопросы
1. Какие вещества называют белками?
2. Каковы основные функции белков в живых организмах?
3. Как классифицируют белки?
4. Каковы химические свойства белков?
5. Какие вещества образуются при полном гидролизе белков?
6. Что такое денатурация белка.
Задание 2 Заполните таблицу
| Структура белковой молекулы | Характеристика структуры | Тип связи | Графическое изображение |
Белки являются обязательной составной частью любого живого организма и играют важнейшую роль в обеспечении процессов жизнедеятельности.
В состав белков обязательно входят четыре химических элемента: углерод, водород, кислород и азот. Многие белки содержат серу. В состав некоторых входит фосфор. Есть белки, содержащие атомы металлов.
Белки — природные высокомолекулярные вещества (полимеры), состоящие из остатков аминокислот.
Аминокислотные остатки соединены в макромолекулах белков пептидной группой −NH−CO−, поэтому белки относят к полипептидам.
В состав белков входят двадцать аминокислот строения NH2−C|H−COOHR. Аминокислотные остатки соединяются в макромолекулы белков в различной последовательности. Число аминокислотных остатков в молекулах тоже может быть разное. Поэтому разнообразие белков практически безгранично и у каждого живого существа набор белковых молекул особый, неповторимый.
Белковые молекулы могут содержать от одного до нескольких сотен и даже тысяч аминокислотных остатков, поэтому их относительные молекулярные массы изменяются от десятков тысяч до нескольких миллионов. Так, относительная молекулярная масса гемоглобина равна 68000, яичного белка — 44000, а вируса гриппа — 32000000.
Свойства белка в первую очередь определяются порядком соединения аминокислотных остатков в полипептидной цепи.
Последовательность аминокислотных остатков в макромолекуле называется первичной структурой белка.

Первичная структура
Существуют вторичная (спираль) и третичная (клубок) структуры белковых молекул. Они образуются в результате внутримолекулярного взаимодействия частей полипептидной цепи.
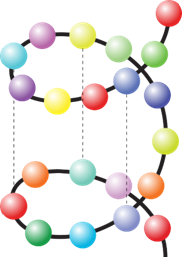
Вторичная структура
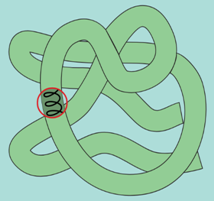
Третичная структура
Несколько белковых молекул могут соединяться друг с другом и образовывать четвертичную структуру.

Четвертичная структура
Свойства белков
Растворимость
По способности растворяться белки делятся на растворимые и нерастворимые. К растворимым относится белок куриного яйца. Не могут растворяться белки шерсти, перьев, ногтей.
Гидролиз
При действии воды в присутствии кислоты или ферментов белки подвергаются гидролизу. В результате расщепления белковых молекул водой образуется смесь аминокислот. Такой процесс происходит в органах пищеварения при переваривании белковой пищи. Получившиеся аминокислоты всасываются в кровь и используются организмом для синтеза собственных белков.
Денатурация
Денатурация — разрушение пространственной структуры белка.
Она происходит при нагревании белков, под действием радиоактивного излучения, некоторых химических веществ (кислот, щелочей, солей тяжёлых металлов). При денатурации белки изменяют свои свойства и теряют биологическую активность, несмотря на то, что их первичная структура сохраняется.

Рис. 1. Денатурация белка
Примером денатурации служит изменение яичного белка при нагревании.