Задача № 1. Охарактеризуйте отношение к окислению алканов, алкенов и аренов.
Алгоритм решения. Окисление органических соединений - это процесс, в результате которого происходит увеличение содержания кислорода в органическом субстрате или отнятие водорода, сопровождающееся образованием кратной связи или новой связи между углеродом и более электроотрицательными атомами: кислородом, азотом и серой и др. В процессе окисления осуществляется перенос электронов от субстрата на реагент-окислитель. Таким образом, роль окислителя могут выполнять вещества, обладающие высоким сродством к электрону, например, кислород, пероксиды, азотная кислота, перманганат калия, дихромат калия и т.д.
Восстановление - образование новых связей с водородом, сопровождающееся переходом электронов от реагента-восстановителя на органический субстрат. В качестве восстановителя используется водород в присутствии гетерогенных катализаторов(Pt, Pd, Ni), гидриды металлов в кислой среде (NaH, NaBH4, ZiBH4).
Способность органических соединений к окислению зависит от тенденции к отдаче электронов: чем легче субстрат отдает электроны, тем легче он окисляется. В связи с этим наиболее трудно окисляются предельные углеводороды. Для их окисления необходимы жесткие условия (горячая хромовая смесь). При окислении алканов промежуточными продуктами являются спирты, альдегиды или кетоны, а конечными – карбоновые кислоты. Причем способность к окислению атомов углерода увеличивается в ряду:
– CH3 < – CH2 – < – CH –
По аналогии с предельными углеводородами окисляются боковые цепи гомологов бензола и гетероциклов. Соединения, содержащие кратные связи (алкены, алкины), по сравнению с алканами окисляются значительно легче. Продуктами окисления алкенов могут быть эпоксиды  , диолы
, диолы  , кетоны
, кетоны  , карбоновые кислоты
, карбоновые кислоты  . В организме эпоксиды образуются при окислении конденсированных ароматических систем и оказывают канцерогенное действие.
. В организме эпоксиды образуются при окислении конденсированных ароматических систем и оказывают канцерогенное действие.
Бензол устойчив к окислению, его ядро можно окислить только в чрезвычайно жестких условиях. Более легко процесс окисления протекает при наличии в ядре электроотрицательных заместителей, таких, как гидроксигруппа. Особенность окислительно-восстановительной реакции (ОВР), в которой принимает участие 1,4-дигидроксибензол (гидрохинон), заключается в ее обратимости, что важно для процессов жизнедеятельности. Окислительно-восстановительные свойства системы гидрохинон-хинон можно представить схемой:

гидрохинон хинон
Аналогичный процесс лежит в основе переноса электронов в дыхательной цепи митохондрий коферментами Q (убихинонами).
Задача № 2. Приведите схему реакции окисления молочной кислоты, протекающей в организме in vivo.
Алгоритм решения.. Первичные и вторичные спирты окисляются легче соответствующих им алканов. Окисление спиртов можно проводить при высоких температурах в присутствии катализаторов (меди или смеси оксидов меди и хрома):

Данная реакция называется дегидрированием и имеет место в организме при биологическом окислении. Катализируется этот процесс в организме ферментами дегипрогеназами, коферментами которых является НАД+ (никотинамидадениндинуклеотид). При дегидрировании субстрат отдает два электрона и два протона или один протон и один гидрид-ион, акцептором которого является НАД+:

Задача № 3. Сравните способность к окислению альдегидов и кетонов.
Алгоритм решения. Альдегиды легко окисляются. Они могут окисляться кислородом воздуха и такими слабыми окислителями, как аммиачный раствор оксида серебра и гидроксида меди. Эти реакции используются для обнаружения альдегидов:


осадок кирпично-красного цвета
Продуктами окисления альдегидов являются карбоновые кислоты. Как указывалось ранее, функциональная группа карбоновых кислот представляет собой сопряженную систему с делокализацией электронов.
Таким образом, при окислении альдегидов происходят уменьшение энергии и переход их в более энергетически выгодное состояние.
Кетоны окисляются только сильными окислителями, например перманганатом калия. При этом происходит расщепление углеродной цепи рядом с карбонильной группой и образуется две молекулы кислоты:
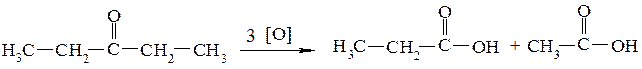 Различие в отношении к окислению альдегидов и кетонов объясняется тем, что в альдегидах окисляется С-Н связь, в кетонах - С-С связь. По продуктам окисления можно определить строение кетона.
Различие в отношении к окислению альдегидов и кетонов объясняется тем, что в альдегидах окисляется С-Н связь, в кетонах - С-С связь. По продуктам окисления можно определить строение кетона.
Задача № 4. Приведите схему окисления этилмеркаптана.
Алгоритм решения. В отличие от спиртов в тиолах происходит окисление не атома углерода, а атома серы, так как связь 5-Н менее прочная, чем связь О-Н. При действии сильных окислителей образуются последовательно сульсеновые, сульфиновые и сульфоновые кислоты.
В мягких условиях (действие пероксидов) идет образование дисульфидов:

Реакция образования дисульфидов и обратная ей реакция играют важную роль в процессах жизнедеятельности: взаимопревращения липоевой и дигидролипоевой кислот - в регулировании липидного и углеводного обменов, цистин - цистеин - в формировании пространственной структуры белка.
Вопросы и упражнения
№ 1
1. Опишите механизм превращения 5 -гидроксипентаналя в кислой среде.
2. Напишите уравнение реакции взаимодействия 1-хлорбутана с водным КОН. Приведите механизм данной реакции.
3. Какие соединения получаются при окислении н-пропилового и изопропилового спиртов. Напишите схемы реакций.
№ 2
1. Приведите механизмы реакций взаимодействия уксусного альдегида с метиламином.
2. Напишите уравнение реакции взаимодействия 1-хлорпропана со спиртовым КОН. По какому механизму протекает эта реакция?
3. Приведите механизм обратимой окислительно-восстановительной реакции гидрохинон-хинон. Какое значение имеют подобного рода реакции для процессов жизнедеятельности?
№ 3
1. Приведите механизм реакции синтеза тетамона, применяемого при спазмах сосудов и получаемого при взаимодействии триэтиламина и этилйодида.
2. Напишите по стадиям реакцию взаимодействия пропанола-2 с НBr. По какому механизму она протекает?
3. Приведите схему превращения в организме яблочной кислоты в щавелево-уксусную при ферментативном окислении.
№ 4
1. Приведите механизм образования лекарственного препарата эфедрина при взаимодействии 1-хлорэтилфенилкетона 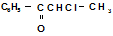 с метиламином.
с метиламином.
2. Приведите механизм реакции дегидратации яблочной (2-гидроксибутандиовой) кислоты в кислой среде.
3. Напишите схему реакции окисления этилового спирта в соответствующую кислоту. Какой промежуточный продукт образуется
в ходе этой реакции? Напишите схему реакции окисления этилового спирта в соответствующую кислоту. Какой промежуточный продукт образуется в ходе этой реакции?
№ 5
1. Приведите механизм реакции взаимодействия аммиака с хлорангидридом никотиновой кислоты (β-пиридинкарбоновой), в следствие которой получают витамин РР (амид никотиновой кислоты), который является противоаллергическим средством.
2. Синтезируйте йодистый бензил с бензилового спирта C6H5CH2OH и йодисто-водородной кислоты. Приведите механизм реакции.
3. Способное ли врачебное вещество хлоретон (1,1, метилпропанол-2), являющееся успокоительным и имеющее легкое наркотическое действие, окисляться? Ответ обоснуйте.
№ 6
1. Приведите механизм реакции образования природной аминокислоты α-аланина (α-аминопропионовой кислоты при взаимодействии α-хлорпропионовой кислоты с аммиаком).
2. Какой реагент необходимо взять для синтеза этилхлорида (средства для неингаляционного наркоза), который получают в промышленности из этилового спирта? Приведите механизм реакции.
3. Напишите уравнение реакции окисления ментола (1-изопропил -4-метилциклогексанол), входящего в состав валидола, и укажите, к какому классу органических соединений относится продукт реакции.
№ 7
1. Приведите механизм реакции алкилирования этаноламина (2-аминоэтанол-1) йодистым метилом с образованием четвертичного аммониевого основания.
2. Приведите механизм реакции дегидратации яблочной кислоты (2-гидроксибутандиовой) при нагревании. Чем объясняется легкость дегидратации яблочной кислоты?
3. Напишите схему обратимой окислительно-восстановительной реакции цистеин-цистина. Какую роль играет эта реакция в организме?
№ 8
1. Приведите схему реакции образования хлоралгидрита (снотворного и успокоительного средства) при гидратации трихлоруксусного альдегида, и объясните, почему это соединение является устойчивым.
2. Синтезируйте молочную кислоту (2-гидроксипропановую) действием водного раствора щелочи на α-галогенкарбоновые кислоты. Приведите механизм реакции.
3. Приведите схему превращения в организме пировиноградной кислоты (2-оксопропановой) в молочную кислоту.
№ 9
1. Приведите механизм реакции взаимодействия пропионового альдегида с этиламином. Встречается ли подобный тип реакций в организме? Значение данной реакции?
2. Напишите по стадиям реакцию взаимодействия бутанола-1 с НCl. По какому механизму она протекает?
3. Приведите схему реакции окисления этилмеркаптана (этантиола). Укажите условия проведения этой реакции.
№ 10
1. Приведите механизм реакции восстановления ацетона с помощью гидридов металлов в кислой среде.
2. Получите аминокислоту глицин (аминоуксусную кислоту) из хлоруксусной кислоты. Объясните механизм реакции.
3. Напишите по стадиям реакцию окисления пропанола-1, содержащегося в сивушных маслах, которые образуются при спиртовом брожении, до кислоты. Сравните способность к окислению пропанола-1 и промежуточного продукта реакции.
№ 11
1. Приведите механизм внутримолекулярной реакции, происходящей с 5- гидроксипентаналем в кислой среде.
2. Получите метиламид уксусной кислоты из хлорангидрида уксусной кислоты и метиламина. Приведите механизм реакции.
3. Напишите уравнение реакции восстановления бутаналя.
№ 12
1. Приведите механизм реакции взаимодействия ацетона с гидроксиламином NH2-OH.
2. Приведите механизм реакции дегидратации яблочной (2-гидроксибутандиовой) кислоты в кислой среде.
3. Напишите схему обратимой окислительно-восстановительной реакции цистеин-цистина. Роль этой реакции в организме.
№ 13
1. Опишите механизм образования ацеталя уксусного альдегида и пропилового спирта с использованием кислого катализатора.
2. Приведите механизм реакции образования ацетилхолина из аминоспирта и уксусной кислоты.
3. Напишите реакцию окисления ментола, который входит в состав лекарственного препарата валидола (1-изопропил-4-метилциклогексанола), и укажите, к какому классу органических соединений относится продукт реакции.
№ 14
1. Приведите механизм реакции взаимодействия пиридина с йодистым метилом. Значение этой реакции.
2. Какой реагент необходимо взять для синтеза этилхлорида (средства для неингаляционного наркоза) из этанола? Приведите механизм реакции.
3. Напишите реакцию окисления уксусного альдегида гидроксидом меди (ІІ). Что наблюдается? Какое значение имеет данная реакция?
№ 15
1. Опишите механизм реакции взаимодействия акролеина (пропеналя) с этиловым спиртом на одной из стадий синтеза глицеринового альдегида.
2. Синтезируйте йодистый бензил с бензилового спирта C6H5CH2OH и йодисто-водородной кислоты. Приведите механизм реакции.
3. Напишите реакцию окисления формальдегида оксидом серебра в водном растворе аммиака. Как называется эта реакция и какое значение она имеет?
Контрольные вопросы:
1. Уметь изображать наиболее предпочтительную конформацию:
циклогексанола;
циклогександиола;
гексахлорциклогексана;
аминоциклогексана;
1, 2-диметилциклогексана;
этилциклогексана;
бромциклогексана.
2. Уметь изображать в проекции Ньюмена:
заторможенную конформацию хлорэтана;
заслоненную конформацию этаноламина;
заторможенную конформацию этаноламина;
заторможенную конформацию этилового спирта.
3. Знать строение:
фурана;
тиофена;
пиррола;
пиридина;
нафталина;
фенантрена.
Уметь объяснять критерии ароматичности этих соединений.
4. Уметь определять вид и знак электронных эффектов:
хлора в бензоле и хлористом бензиле;
карбоксильной группы в акриловой и пропионовой кислотах;
метильной и гидроксильной групп в о-крезоле;
карбоксильной группы в бензойной и уксусной кислотах;
карбоксильной и аминогруппы в п-аминобензойной кислоте;
гидроксильной и аминогруппы в п-аминофеноле;
амино- и сульфогруппы в молекуле сульфаниловой кислоты;
гидроксильной и карбоксильной групп в салициловой кислоте.
5. Уметь приводить механизмы реакций:
хлорирование пропана;
бромирования этилена;
взаимодействия пропилена с хлористым водородом;
бромирование этана;
бромирование бутилена - 1,3;
гидратации пропилена;
бромирования изобутана;
гидратации бутена - 1;
хлорирования циклогексана;
нитрирования бензола;
хлорирования бензола.
6. Уметь приводить уравнения реакций с учетом направляющего действия заместителей:
бромирования фенола;
сульфирования пиридина;
сульфирования анилина;
бромирования толуола;
бромирования анилина;
бромирования бензойной кислоты;
бромирования пиррола;
нитрование толуола.
7. Уметь сравнивать кислотность и основность следующих соединений:
пропилового и изопропилового спиртов;
метилового и пропилового спиртов;
пропилового спирта и глицерина;
этанола и 2- хлорэтанола;
фенола и тринитрофенола;
фенола и трибромфенола;
пропионовой и 2-оксипропионовой кислот;
2- хлорпропионовой и 3- хлорпропионовой кислот;
бензойной и салициловой кислот;
бензойной и фталевой кислот;
метил-, диметил- и триметиламина;
метиламина и триброманилина;
анилина и триброманилина;
анилина и тринитроанилина;
диметиламина и диметилового эфира.
8. Уметь приводить механизмы реакций взаимодействия:
н-пропилхлорида со спиртовым раствором КОН;
изопропилового спирта с НBr;
бензилового спирта с йодисто-водородной кислотой;
н - пропилхлорида с водным раствором КОН;
дегидратации пропілового спирта в кислой среде;
последовательного получения полуацеталя и диэтилацеталя уксусного альдегида;
пропионового альдегида с этиловым спиртом;
уксусного альдегида с изопропиловым спиртом;
альдольной конденсации уксусного альдегида.
9. Уметь приводить уравнения реакций окисления:
пропилового спирта;
изопропилого спирта;
гидрохинона;
этилмеркаптана (СН3-СН2-SH)
10. Уметь писать уравнение реакций:
диспропорционирования (реакция Канницарро) бензойного альдегида;
восстановление метилэтилкетона;
окисления формальдегида аммиачным раствором солей серебра;
окисления пропионового альдегида гидроксидом меди (ІІ);
йодоформную реакцию открытия ацетона;
гидролиза диметилацеталя уксусного альдегида;
внутримолекулярную реакцию с 5- оксипентаналем в кислой среде.