I. РЕАКЦИИ ОКИСЛЕНИЯ
1. Горение (коптящее пламя):
2C6H6 + 15O2 t → 12CO2 + 6H2O + Q
Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки
3. Гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку):
А) в кислой среде до бензойной кислоты
При действии на гомологи бензола перманганата калия и других сильных окислителей боковые цепи окисляются. Какой бы сложной ни была цепь заместителя, она разрушается, за исключением a -атома углерода, который окисляется в карбоксильную группу.
Гомологи бензола с одной боковой цепью дают бензойную кислоту:

Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:

5C6H5-C2H5 + 12KMnO4 + 18H2SO4 → 5C6H5COOH + 5CO2 + 6K2SO4 + 12MnSO4+28H2O
5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 3K2SO4 + 6MnSO4 +14H2O
Упрощённо:
C6H5-CH3 + 3O KMnO4 → C6H5COOH + H2O
Б) в нейтральной и слабощелочной до солей бензойной кислоты
C6H5-CH3 + 2KMnO4 → C6H5COOК + KОН + 2MnO2 + H2O
II. РЕАКЦИИ ПРИСОЕДИНЕНИЯ (труднее, чем у алкенов)
Галогенирование
C6H6 +3Cl2 hν → C6H6Cl6 (гексахлорциклогексан - гексахлоран)

Гидрирование
C6H6 + 3H2 t,Pt или Ni → C6H12 (циклогексан)

Полимеризация

III. РЕАКЦИИ ЗАМЕЩЕНИЯ – ионный механизм (легче, чем у алканов)
Галогенирование -
a) бензола
C6H6 + Cl2 AlCl3 → C6H5-Cl + HCl (хлорбензол)

C6H6 + 6Cl2 t,AlCl3 → C6Cl6 + 6HCl (гексахлорбензол)
C6H6 + Br2 t,FeCl3 → C6H5-Br + HBr (бромбензол)

Б) гомологов бензола при облучении или нагревании
По химическим свойствам алкильные радикалы подобны алканам. Атомы водорода в них замещаются на галоген по свободно-радикальному механизму. Поэтому в отсутствие катализатора при нагревании или УФ-облучении идет радикальная реакция замещения в боковой цепи. Влияние бензольного кольца на алкильные заместители приводит к тому, что замещается всегда атом водорода у атома углерода, непосредственно связанного с бензольным кольцом (a -атома углерода).
1) C6H5-CH3 + Cl2 hν → C6H5-CH2-Cl + HCl
2)
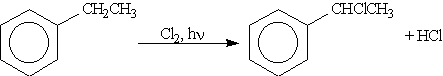
в) гомологов бензола в присутствии катализатора
C6H5-CH3 + Cl2 AlCl3 → (смесь орта, пара производных) + HCl
Нитрование (с азотной кислотой)
C6H6 + HO-NO2 t, H2SO4 → C6H5-NO2 + H2O
нитробензол - запах миндаля!

C6H5-CH3 + 3HO-NO2 t, H2SO4 → СH3-C6H2(NO2)3 + 3H2O
2,4,6-тринитротолуол (тол, тротил)
Получение аренов (бензола и его гомологов)
В лаборатории
1. Сплавление солей бензойной кислоты с твёрдыми щелочами
C6H5-COONa + NaOH t → C6H6 + Na2CO3
бензоат натрия
2. Реакция Вюрца-Фиттинга: (здесь Г – галоген)
С6H5-Г + 2Na + R-Г → C6H5-R + 2NaГ
С6H5-Cl + 2Na + CH3-Cl → C6H5-CH3 + 2NaCl
В промышленности
- выделяют из нефти и угля методом фракционной перегонки, риформингом;
- из каменноугольной смолы и коксового газа
1. Дегидроциклизацией алканов с числом атомов углерода больше 6:
C6H14 t, kat → C6H6 + 4H2

2. Тримеризация ацетилена (только для бензола) – р. Зелинского:
3С2H2 600°C, акт. уголь → C6H6

3. Дегидрированием циклогексана и его гомологов:
Советский академик Николай Дмитриевич Зелинский установил, что бензол образуется из циклогексана (дегидрирование циклоалканов
C6H12 t, kat → C6H6 + 3H2

C6H11-CH3 t, kat → C6H5-CH3 + 3H2
метилциклогексан толуол
4. Алкилирование бензола (получение гомологов бензола) – р Фриделя- Крафтса.
C6H6 + C2H5-Cl t, AlCl3 → C6H5-C2H5 + HCl
хлорэтан этилбензол
