Кафедра БТ
Лабораторная работа
по предмету “Химия отрасли”
Получение спирта из крахмала
Выполнили:
студенты гр. ТБПиВ-91
Анохин И. С.
Шипунова Т. С.
Сандакова К. Е.
Ханмурадов Р. Г.
Проверил:
доцент
Митрофанов Р. Ю.
Цель работы: ознакомиться с методом получения спирта из крахмала при помощи дрожжей и ячменного солода.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ.
ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО СПИРТА ИЗ БИОЛОГИСЕСКОГО СЫРЬЯ
Современная промышленная технология получения этилового спирта из пищевого сырья включает следующие стадии:
§ Подготовка и измельчение крахмалистого сырья - зерна (прежде всего - ржи, пшеницы), картофеля, кукурузы и т. п.
§ Ферментация. На этой стадии происходит ферментативное расщепление крахмала до сбраживаемых сахаров. Для этих целей применяются рекомбинантные препараты альфа-амилазы, полученные биоинженерным путём - глюкамилаза, амилосубтилин.
§ Брожение. Благодаря сбраживанию дрожжами сахаров происходит накопление в бражке спирта.
§ Брагоректификация. Осуществляется на разгонных колоннах.
Отходами бродильного производства являются углекислый газ, барда, эфиро-альдегидная фракция, сивушные масла.
Спирт, поступающий из брагоректификационной установки (БРУ) не является безводным, содержание этанола в нём до 95,6 %. В зависимости от содержания в нём посторонних примесей, его разделяют на следующие категории:
§ 1 сорт
§ высшей очистки
§ базис
§ Экстра
§ Люкс
§ Альфа
Производительность современных спиртовых заводов около 30 000-100 000 литров спирта в сутки.
ПОЛУЧЕНИЕ СОЛОДА.
Технология солода складывается из следующих основных процессов: замачивание и проращивание зерна; сушка солода и удаление ростков. На отечественных спиртовых заводах для осахаривания используют сырцовый - несушеный солод (неправильно называемый «зеленым»). Этот солод не может долго храниться, поэтому на каждом спиртовом заводе его готовят в количествах, необходимых для текущей работы.
В спиртовой промышленности США, Германии и некоторых других стран применяют сухой ячменный солод, вырабатываемый специализированными солодовенными заводами. Сушка солода связана с большими капитальными и эксплуатационным затратами и сопровождается снижением осахаривающей (на 25-30 %) и особенно сильно (в 4 раза) цитолитической активности ферментов.
Осахаривающая способность (ОС) выражает возможность всех амилолитических ферментов осахаривать (гидролизовать) крахмал до редуцирующих веществ (РВ). За единицу ОС принимают количество фермента, которое при температуре 30 °С в течение 1 ч расщепляет 1 г крахмала. Степень гидролиза субстрата не превышает 30 %.
Инвертазная активность (ИА) выражает способность фермента гидролизовать сахарозу. За единицу активности принимают количество фермента, которое за 1 мин гидролизует 1,25 г сахарозы при рН 4,6 и температуре 30 °С. Степень гидролиза субстрата не более 50 %. Активность препарата выражена в единицах РВ на 1 г препарата или 1 мл ферментного раствора.
СЫРЬЕ ДЛЯ СОЛОДОРАЩЕНИЯ.
Основное требование, предъявляемое к солоду, - способность как можно быстрее и полнее осахаривать крахмал, для чего он должен накопить три фермента: α-амилазу, β-амилазу и декстриназу. В солоде, приготовленном из зерна различных злаков, содержатся неодинаковые количества каждого из ферментов. Исходя из этого, все злаки делят на четыре большие группы: ячменя, проса, овса и кукурузы. Группа ячменя, объединяющая ячмень, рожь и пшеницу, дает солод с высокой α- и β-амилолитической и относительно низкой декстринолитической активностью.
ЗАМАЧИВАНИЕ ЗЕРНА.
Основная цель замачивания - увлажнить зерно; дополнительная - отмыть от остатков пыли, удалить легкие зерновые и незерновые примеси и подавить микроорганизмы. Замачивание ведут с применением воздуха и воды, чередуя насыщение зерна водой и аэрацию.
ПРОРАЩИВАНИЕ ЗЕРНА.
Цель солодоращения - накопление ферментов, растворение межклеточных пластинок и стенок клеток эндосперма, что необходимо для снабжения развивающегося зародыша питательными веществами и перехода ферментов в сусло. Зерно проращивают в таких условиях, чтобы расход крахмала на дыхание и образование новых вегетативных органов был минимальным, при возможно меньшем обсеменении микроорганизмами, особенно кислотообразующими.
Проращивание ячменя и овса ведут следующим образом: в течение первых 2 суток поддерживают температуру 19-20 °С, в дальнейшем ее снижают ежесуточно на 1-2 °С и к окончанию проращивания доводят до 13-14 °С. Влажность готового солода должна быть 44-45 %. Прекращают проращивание, как правило, на 10-е сутки.
ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ КРАХМАЛА.
Цель ферментативного гидролиза крахмала - получение сусла. Разваренную массу зерна или картофеля осахаривают (гидролизуют) ферментами солода или культур плесневых грибов. Получаемый в результате этого продукт (сусло) в литературе прошлых лет называли «сладкий затор», «осахаренная масса». Термин «затор» сохранился с того давнего времени, когда на спирт перерабатывали муку, которую «затирали» - смешивали с водой и солодом при определенной температуре.
ХИМИЗМ ГИДРОЛИЗА.
 | |||
 |
|




Независимо от природы катализатора при разрыве каждой α-1,4- и α-1,6-глюкозидной связи в крахмале по месту разрыва присоединяется молекула воды:
В амилозе при разрыве α-1,4-глюкозидной связи гидроксил воды присоединяется к первому углеродному атому левого остатка глюкозы, образуя альдегидную группу в скрытой (полуацетальной) форме, водород воды присоединяется к кислороду глюкозидной связи при четвертом углеродном атоме правого остатка глюкозы. Гидролиз амилопектина в точке ветвления (α-1,6-глюкозидной связи) сопровождается присоединением гидроксила воды также к первому углеродному атому, а водорода воды - к шестому углеродному атому.
В пределе - при разрыве всех глюкозидных связей - присоединяется n-1 молекул воды (где n - число глюкозных остатков в макромолекулах амилозы и амилопектина, или СП) и образуется n молекул глюкозы. Так как n очень велико, то числовое значение n-1 будет практически пренебрежимо мало отличаться от n и реакция гидролиза может быть выражена уравнением
(С6Н10О5)n + nН2О = nС6Н12О6
или применительно к одному глюкозному остатку
C6H10О5 + Н2О = C6H12О6.
162 18 180
Отсюда теоретический выход глюкозы в процессе гидролиза составляет 111,11 % к массе крахмала.
Механизм действия всех ферментов основан на образовании неустойчивых промежуточных соединений - комплексов из реагирующих молекул субстрата и активных центров ферментов. При этом в реагирующих молекулах происходит деформация, обеспечивающая вступление их в реакцию. После реакции фермент и химически измененный субстрат отталкиваются один от другого и фермент может реагировать с новой молекулой субстрата.
ОСАХАРИВАНИЕ.
Осахаривание разваренной массы, как правило, осуществляют непрерывным способом и лишь на некоторых заводах малой мощности - периодическим. Независимо от способа процесс осахаривания складывается из следующих операций: охлаждение разваренной массы до определенной температуры, которая после смешивания массы с солодовым молоком (микробной культурой) понизится до заданной для осахаривания; смешивание разваренной массы с солодовым молоком (микробной культурой); осахаривание крахмала; охлаждение сусла до температуры «складки» - начальной температуры брожения сусла; перекачивание сусла в бродильное и дрожжевое отделения завода.
Все эти операции, кроме перекачивания сусла, при периодическом процессе выполняются в одном аппарате, называемом заторным баком; при непрерывном процессе или в отдельных аппаратах, установленных последовательно, или в одном аппарате (сочетается несколько операций).
СБРАЖИВАНИЕ ЗЕРНО-КАРТОФЕЛЬНОГО СУСЛА.
Все сусло кроме той части, что идет на приготовление дрожжей, направляют в бродильные аппараты, и содержащийся в нем сахар сбраживается дрожжами в спирт. При сбраживании зерно-картофельного сусла одновременно происходит доосахаривание декстринов. Бродящее сусло называют бражкой, или культуральной жидкостью.
Показание сахарометра в фильтрате бражки - это видимая плотность, показание сахарометра в фильтрате бражки после отгонки спирта и доведения дистиллированной водой до первоначального объема - содержание истинных сухих веществ бражки. Последние всегда больше видимой плотности. Этими терминами заменены ранее применявшиеся - соответственно видимый и истинный отброды.
Содержание спирта в зрелой бражке (и в водно-спиртовом растворе) в объемных процентах называют крепостью бражки (и этилового спирта). На отечественных спиртовых заводах в настоящее время применяют в основном непрерывно-проточный, проточно-рециркуляционный и циклический, а на малых заводах еще периодический способы сбраживания сусла.
ПЕРЕГОНКА ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ.
В тех случаях, когда нагревание не сопровождается распадом вещества или когда перегоняемая жидкость, имеет не слишком высокую температуру кипения, для очистки пользуются перегонкой под обыкновенным давлением. Для этой цели собирают прибор (рис. 1), состоящий, из колбы Вюрца, холодильника и приемника.
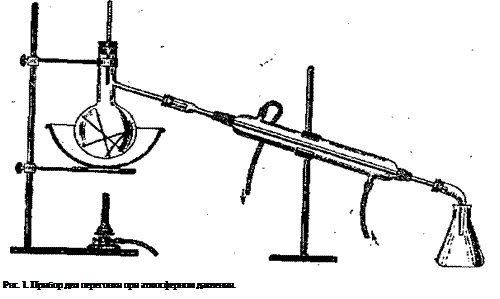 |
Колбу Вюрца выбирают таких размеров, чтобы подлежащая перегонке жидкость занимала не больше 2/3 объема колбы. Колбу снабжают термометром, присоединяют к холодильнику и укрепляют лапкой на штативе. Под колбу подводят водяную или другую баню, или же кольцо с асбестированной сеткой, если жидкость можно нагревать на горелке.
Отводная трубка колбы должна входить в форштос холодильника не менее чем на 4-5 см (считая от пробки). Убедившись в надежном соединении колбы с холодильником и прочности крепления колбы, в горло ее вставляют воронку таких размеров, чтобы нижний конец ее был на 2-3 см ниже отводной трубки, вливают жидкость, подлежащую перегонке, и закрывают горло пробкой с термометром.
Когда весь прибор собран, тщательно проверяют, хорошо ли подобраны пробки и правильно ли стоит термометр. Только тогда подставляют приемник для дистиллята и начинают нагревание. При перегонке нужно стремиться к тому, чтобы не было сильно бурлящего кипения, так как капли жидкости могут попасть в отводную трубку и загрязнить дистиллят. Для создания равномерного кипения в колбу бросают несколько стеклянных капилляров, запаянных с одного конца. Приемником могут служить химические стаканы, конические колбы и другие сосуды.
Фракционной, или дробной, перегонкой называют такой способ ведения ее, когда из смеси жидкостей с различными температурами кипения выделяются некоторые отдельные компоненты.
Дробную перегонку ведут обязательно с применением дефлегматора. К круглодонной колбе соответствующей емкости подбирают пробку, в которой высверливают отверстие для дефлегматора. Затем к дефлегматору подбирают пробку для термометра и к холодильнику для отводной трубки дефлегматора. Тот или иной дефлегматор выбирают с учетом свойств жидкостей, образующих смесь. Дефлегматор вставляют в колбу, поставленную на баню или на асбестированную сетку и прикрепленную лапкой к штативу. При помощи другой лапки дефлегматор также прикрепляют к штативу, затем его соединяют с холодильником и уже после этого вставляют в дефлегматор пробку с термометром.
Вместо дефлегматоров лучше пользоваться колонками полной конденсации, дающими возможность проводить более тонкое разделение жидкостей по температурам кипения.
Жидкость, подлежащую фракционированию (дробной перегонке), наливают в колбу или перед тем как вставят дефлегматор, или через дефлегматор после того, как последний соединен с холодильником. Прежде чем приступить к перегонке, необходимо подготовить нужное количество приемников, поставив на каждом из них восковым карандашом номер, затем подставляют приемники в порядке очередности. Одновременно следует вести запись
тех температур, в пределах которых собиралась данная фракция, например:
Фракция № 1......................... 80-86 °C
Фракция № 2....................... 86-92 °С
Если при перегонке замечаются какие-либо особенности, их также нужно отмечать в тетради против номера фракции. В некоторых случаях вначале проводят грубое фракционирование, когда отдельные фракции собирают в пределах 5-10 °С, а затем эти фракции разгоняют отдельно, но уже в более узких температурных пределах. Метод фракционной перегонки является весьма кропотливым и его применяют главным образом при точных работах.
Нужно отметить, что не все смеси жидкостей с отличающимися друг от друга температурами кипения можно разделить дробной перегонкой. Если, например, имеется смесь, состоящая из 7 частей этилового спирта и 93 частей бензола, температура кипения смеси будет 60 °С, несмотря на то, что спирт кипит при 78 °С, а бензол при 80 °С. Бывают смеси, которые имеют и более высокую температуру кипения, чем каждое из образующих их веществ. Например, вода кипит при 100 °С и хлористый водород при минус 84 °С. Смесь же их, образующая соляную кислоту и содержащая 20,2 % хлористого водорода, кипит при 110 °С (при давлении 760 мм рт. ст.). Эти смеси нельзя разделить перегонкой, и они получили название нераздельно кипящих смесей, или азеотропных смесей.
Такие смеси в лабораторной практике встречаются довольно часто; в специальных справочниках имеются таблицы двойных и тройных азеотропных смесей с указанием температур кипения смесей и их процентного состава. При работе с большими количествами диэтилового эфира нужно помнить, что эфир может содержать перекисные соединения; последние при отгонке эфира остаются на дне колбы и при накоплении могут вызвать взрыв.
Количество перекисных соединений, в эфире может быть различным. Присутствие их можно обнаружить по образованию коричневого окрашивания при смещении иодкалийкрахмального раствора с испытуемым эфиром. Для отделения перекисных соединений в эфир добавляют подкисленный раствор FeSO4 и оставляют стоять в течение суток, затем эфир отделяют и перегоняют над смесью FeSО4 • 7Н2О и NaOH, взятой в эквимолекулярном соотношении компонентов. Очищенный таким образом эфир будет свободен от перекисных соединений и безопасен в работе. Накопление перекисных соединений идет очень заметно, если эфир стоит на свету. Поэтому эфир следует хранить в темном месте.
Иногда одна перегонка, даже фракционированная, не дает нужной очистки продукта. В таких случаях часто совмещают перегонку с какой-либо химической обработкой. Например, в эфире могут быть в качестве примесей органические кислоты (уксусная, муравьиная), альдегиды, перекиси и ненасыщенные соединения. Наиболее простым способом очистки эфира от всех этих загрязнений, даже если они присутствуют одновременно, является следующий. К 500 мл эфира, содержащего примеси, добавляют 30 мл водного 12,5 %-ного раствора AgNO3. и затем 50 мл водного 4 %-ного (1н) раствора NaOH. Смесь энергично перемешивают встряхиванием в течение 5-7 мин. После этого дают эфиру отстояться и отделяют водный слой. Работу нужно проводить в делительной воронке. Очищенный таким образом эфир подвергают перегонке.
Точно таким же приемом можно очистить и многие другие органические жидкости, кроме тех, которые могут диссоциировать с образованием ионов хлора.
О перегонке под обыкновенным давлением необходимо запомнить следующее:
1. Прибор для перегонки должен быть собран правильно, красиво и аккуратно. В местах соединений не должно быть неплотностей.
2. Нагревание огнеопасных жидкостей надо вести вдали от нагревательных элементов на предварительно нагретой водяной или иной бане.
3 Термометр должен быть помещен вдоль оси горла колбы Вюрца. и не касаться стенок ее; резервуар термометра должен находиться на одном уровне с отводной трубкой или немного ниже ее.
4-. В колбу надо бросить 2-3 «кипелки» маленькие кусочки не глазированного фарфора.
5. При атмосерном давлении можно перегонять только те вещества, которые при нагревании не претерпевают каких-либо изменений и не разлагаются.
ПРАКТИЧЕСКАЯ ЧАСТЬ.
Ход работы:
1. Отбор зерна для проращивания.
Мы отделили качественные зерна от сора и обломков зерна, после чего взвесили:
· mнавески = 87,54 г
· mотобр = 82,36 г
2.Замачивание зерна.
Отобранное зерно промываем и выкладываем в чашки Петри, предварительно положив на дно чашек смоченную фильтровальную бумагу.
3.Прорастание зерна в чашках Петри происходит 3-4дня, каждый день мы промываем зерно.
4.Отделение ростков. Вручную отделяем ростки и взвешиваем солод.
· mсолода = 92,80 г
· mотходов = 119,06 г
5.Определение коэффициент всхожести.
· Квсх = (59,6 / 82,36) * 100% = 72,4 %
6.Высушивание зерна.
· mсолода = 59,60 г
7.Приготовление крахмала и измельчение солода. Из высушенного солода отбираем 15 г, растираем в керамической чашке, приливаем 50 мл воды и оставляем на час при температуре 40 °С.
9.100 г крахмала картофельного залили водой и влили его в доведенную до кипения воду постоянно перемешивая. Получили гель.
10.Осахаривание крахмала. После чего определяли наличие крахмала, капая в отдельно отобранную пробу(5 мл) раствор йода до тех пор пока он не перестал менять окраску.
11. Количество мальтозы в геле определяли титрованием, затем проводим рачеты:
· Vтитр1 = 0,5 мл; xмальт 1 = ((25-0,5)*0,0171*100*25)/10 = 105 г
· Vтитр2 = 1,1 мл; xмальт 2 = ((25-1,1)*0,0171*100*25)/10 = 102 г
В полученный гель вливаем приготовленное заранее солодовое молочко.
12.Брожение. Полученный затор перелили в трёх литровую банку, добавив 10 г дрожжей хлебопекарных прессованных (ГОСТ 171-81) и надели на банку медицинскую перчатку и оставили для брожения. Брожение продолжалось 7 дней при комнатной температуре
13.Перегонка. Из полученной смеси спирт выделяют отгонкой. Собрав установку поместили раствор на 2/3 объема в круглодонную колбу и проводим перегонку при температуре от 81 до 92 °С. Выход спирта:
· I фракция = 190 мл (tкип = 81-86 °С)
· II фракция = 50 мл (tкип = 86-92 °С)
· mпогона = 193,06 г
11.Определение плотности, объемных процентов, а также коэффициента преломления спирта.
· ρ = mпогона/Vпогона= 0,9810 г/дм3
· n = 1,3382
Вывод:
При выполнении лабораторной работы «Получение спирта из крахмала» мы ознакомились с получением солода путем проращивания ячменя. Ячмень перебрали, отделив цельные зерна (mнавески = 87,54 г, mотобр = 82,36 г, mсора= 5,18 г). После зерно промыли водой и разложили в чашки Петри для прорастания. Через 4 дня зерно проросло, мы вручную отделили ростки и определили коэффициент всхожести, равный 68 %. Солод оставили сушиться. Из высушенного солода приготовили солодовое молоко, растерев 15 г солода и добавив к нему 50 мл воды. Из 100 г крахмала получили клейстер и осахарили его солодовым молоком, после чего измерили содержание мальтозы (хмальт ≈ 103,5 г) и получили затор. Брожение продолжалось в течении 7 дней. Из бражки путем перегонки под атмосферным давлением получили погон и спиртометром измерили содержание спирта в нем (13 % об.). Измерили плотность погона ареометром (0,9810 г/дм3), измерили массу погона (193,06 г), а также коэффициент преломления погона рефрактометром (1,3382). В справочной литературе посмотрели, какому содержанию спирта соответствует измеренная плотность погона. В результате получили, что плотность погона 0,9810 г/дм3 соответствует содержанию спирта 13,2 % об. (что не сильно отличается от измеренных нами 13 % об.). Следовательно, делаем вывод, что все измерения были проведены с достаточной точностью.