Пассивная иммунотерапия
Использование вакцин на основе БЦЖ
Один из эффективных методов — это внутрипузырная БЦЖ-терапия. Вакцина БЦЖ — это взвесь жизнеспособных бацилл КальметтаГерена (Calmette-Guerin). Внутриклеточно размножаясь, они стимулируют местный иммунитет, в котором задействованы макрофаги, Т-лимфоциты и цитокины. В 20 исследованиях, проведенных с использованием различных форм поддерживающей БЦЖ-терапии, отмечено снижение шансов прогрессирования рака на 37 %. Более того, клинически доказано, что вакцина БЦЖ более эффективна по сравнению с митомицином С.
БЦЖ - это вакцина, приготовленная на основе бактерии Mycobacterium bovis, которая вызывает туберкулез у крупного рогатого скота. Для человека БЦЖ не опасна, но обладает способностью активировать иммунитет. Вакцина БЦЖ действует наподобие цитокинов, усиливая работу всей иммунной системы. Непосредственно на клетки меланомы вакцина не влияет. Иногда она используется при лечении меланомы стадии III и вводится в саму опухоль.
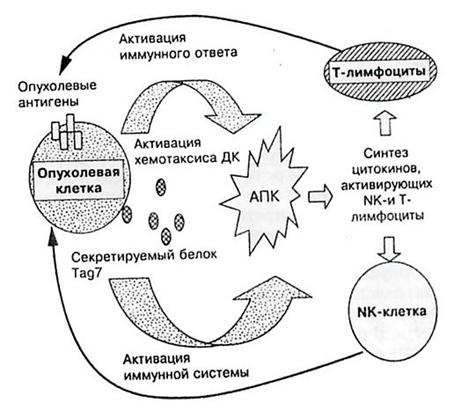
Использование иммуностимуляторных цитокинов (интерлейкин -2, интерлейкин-4, интерлейкин-12; интерферон альфа, бэта, гамма; фактор некроза опухолей альфа, GM-CSF)
Добавление других цитокинов, например IL-4, IL-13, IL-15 или TNF-, противодействовало эффектам выделения, связанным с активацией этих клеток. Использование на практике способов данного изобретения обеспечивает простой и более экономичный способ получения и поддержания незрелых дендритных клеток с состоянии, оптимизированном для поглощения, процессинга и презентации выбранного антигена.
Новые гены можно внедрить в клетки с тем, чтобы на их поверхности экспонировались новые белки. Новые белки включают иммунную сигнализацию и стимулирование молекул, например, такого цитокина, как интерлейкин-2, гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) и других стимулирующих молекул. Генетически-измененные вакцины опухолевых клеток создают клетки, которые синтезируют опухолеспецифические антигены, так же как и новые иммуностимуляторные молекулы на их клеточной поверхности. Эти клетки могут быть введены пациенту. Комбинация молекул на поверхности ведет к усиленному иммунному ответу. Добавленные молекулы на поверхности измененных опухолевых клеток стимулируют иммунную систему, чтобы атаковать даже те клетки опухоли, которые остались в организме и не имеют новых белков на своей поверхности.
интерлейкины – это цитокины, которые организм производит естественным образом, и которые можно получить в лаборатории. Определены многие интерлейкины. Применение интерлейкина-2 (альдеслейкина) в лечении рака наиболее изучено. Интерлейкин-2 стимулирует рост и активность многих иммунных клеток, таких как лимфоциты, которые разрушают раковые клетки. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило применение интерлейкина-2 для лечения метастатического рака почки и метастатической меланомы.
Интерлейкин-2 (ИЛ-2) применяют через 10-14 суток после введения вакцины в дозе 100000-125000 МЕ на м2 поверхности тела в день, внутривенно капельно, в течение 4 часов. Курс лечения состоит из 15-60 введений. Затем проводят поддерживающую иммунотерапию ИЛ-2 в течение 6-12 месяцев, с интервалом 2 месяца. ИЛ-2 вводят ежедневно, 4 дня, в дозе 125000 МЕ на м2.
Гамма-интерферон (ИФН-γ) применяется по следующей схеме: внутримышечное введение 1000000 МЕ ИФН-g через день – 1 месяц, затем 2 месяца – 1 раз в неделю. Гамма-интерферон начинают вводить через день после инъекций вакцины РЕСАН.
Если есть возможность во время основного курса иммунотерапии доставлять ИЛ-2 и ИФН-γ непосредственно к опухоли, то это наиболее предпочтительный вариант.
Интерферон (ИФН), также как и интерлейкин_2 (ИЛ_2), не является типичным противоопухолевым препаратом. Тем не менее, его можно отнести к классу средств, обладающих противоопухолевым действием, благодаря целому ряду биологических свойств, включая влияние на процессы программированного клеточного роста, дифференцировку и другие клеточные функции. По структуре ИФН – это секреторные гликопротеины. На сегодняшний день известно 5 типов ИФН (альфа, бэта, гамма и еще 2). У человека ИФН альфа, бета, гамма кодируются 3 различными генами и, следовательно, существует лишь один тип каждого из этих интерферонов. ИФН альфа кодируется 25 генами, что объясняет существование 25 различных
подтипов ИФ альфа. На долю ИФН альфа приходится 90% всех альфа_ИФН. На практике
широко используются 2 разновидности рекомбинантного ИФН – интерферон альфа (роферон А) и интерферон_альфа (интрон А, реаферон). Биологическая активность ИФН заключаются в их противовирусном, противомикробном, антипролиферативном и иммуномодулирующем действии. Антиканцерогенные свойства α_ИФН связаны со способностью стимулировать систему репарации ДНК, модулировать экспрессию генов, вовлеченных в процесс канцерогенеза, подавлять клеточную репликацию онковирусов, контролировать ангионеогенез, активировать эффекторные клетки (Т_лимфоциты, макрофаги, дендритные клетки), а также увеличивать клеточную адгезию, продукцию других цитокинов. Более чем в 50% случаев солидные опухоли (меланома, колоректальный рак, рак шейки матки, рак молочной железы, мелкоклеточный рак легкого, хорионкарцинома) утрачивают один или большее число аллелей главного комплекса гистосовместимости (МНС) класса I. В то же время молекулы MHC I класса, представленные на поверхности опухолевых клеток, являются мишенями для макрофагов, которые запускают противоопухолевую иммунную реакцию. ИФН регулирует экспрессию МНС_антигенов I типа на поверхности опухолевых клеток и МНС_антигенов II типа на макрофагах, что делает опухолевую клетку уязвимой для различных эффекторов иммунной системы. Помимо антипролиферативного действия, ИФН влияет также на различные физиологические параметры клеток. Он вызывает изменения цитоскелета, включая повышение структурированности микрофиламентов, перераспределение фибронектина, увеличение объема клеток, которые становятся более уплощенными, повышение ригидности плазматической мембраны и снижение подвижности клеток. Эти эффекты играют существенную роль в противоопухолевой активности.
Интерлейкины объединяются следующими общими свойствами: 1) синтезируются клетками иммунной системы в процессе реализации механизмов естественного или специфического иммунитета; 2) проявляют свою активность при очень низких концентрациях (порядка 10_11 моль/л); 3) служат медиаторами иммунной и воспалительной реакций и обладают аутокринной, паракринной и эндокринной активностью; 4) действуют как факторы роста и дифференцировки клеток (при этом вызывают преимущественно медленные клеточные реакции, требующие синтеза новых белков); 5) образуют регуляторную сеть, в которой отдельные элементы обладают синергическим или антагонистическим действием; 6) обладают полифункциональной активностью.
Активная иммунотерапия.