| Элементы характеристики | Алканы | Алкены | Алкины | Циклоалканы | Арены | ||||||
| Общая формула | СnH2n+2, n ≥ 1 | СnH2n, n ≥ 2 | СnH2n-2, n ≥ 2 | СnH2n, n ≥ 3 | СnH2n-6, n ≥ 6 | ||||||
| Представители | Н ׀ Н – С – Н, СН4 - метан ׀ Н Н Н ׀ ׀ Н – С – С – Н, С2Н6 - этан ׀ ׀ Н Н С3Н8 - пропан С4Н10 - бутан С5Н12 - пентан С6Н14 – гексан С7Н16 – гептан С8Н18 - октан | СН2=СН2, С2Н4 - этилен, этен СН2=СН-СН3, С3Н6 -пропилен, пропен СН2=СН-СН2-СН3, С4Н8 – бутилен, бутен-1 СН3-СН=СН-СН3, С4Н8 бутен-2 - изомер бутена-1 | СН≡СН, С2Н2 - ацетилен, этин СН≡С-СН3, С3Н4 - пропин СН≡С-СН2-СН3, С4Н6 – бутин-1 СН3-С≡С-СН3, С4Н6 – бутин-2 - изомер бутина-1 |
СН2
 
циклопропан
׀ ׀ Н2С – СН2, циклобутан
- циклопентан |
 , С6Н6 -бензол
, С6Н6 -бензол
 -СН3, С6Н5-СН3 –
метилбензол, толуол
-СН3, С6Н5-СН3 –
метилбензол, толуол
| ||||||
| Нахождение в природе | да | нет | нет | да | да | ||||||
| Тип гибридизации ключевых атомов углерода | sp3 - | sp2 - | sp - | sp3 - | sp2 - | ||||||
| Отличительный признак | Все связи одинарные С-С | Есть двойная связь С=С | Есть тройная связь С≡С | Есть цикл |   Бензольное кольцо Бензольное кольцо
| ||||||
| Типы связи | σ - связи | σ – связи и π - связь | Σ – связи и π - связи | σ - связь | σ - связи и π – связи (π – система) | ||||||
| Типичные химические свойства | Радикальное замещение | Присоединение. Полимеризация | Присоединение | В зависимости от размера цикла: малые – присоединение большие – радикальное замещение | Электрофильное замещение. Возможно присоединение | ||||||
| Характерные типы изомерии | Углеродного скелета С-С-С-С бутан С-С-С 2-метилпропан ׀ С |
Углеродного скелета.
Положения кратной связи
С=С-С-С бутен-1
С-С=С-С бутен-2
С=С-С 2-метилбутен-1
׀
С
Межклассовая:
С=С-С и
алкен и циклоалкан
| Углеродного скелета. Положения кратной связи С≡С-С-С-С пентин-1 С-С≡С-С-С пентин-2 С≡С-С-С 3-метилбутин-1 ׀ С Межклассовая: С≡С-С-С и С=С-С=С алкин и алкадиен |
Углеродного скелета:
а) С2Н5
 ׀
этилциклопропан ׀
этилциклопропан
 и
Н3С- -СН3
1,2 - диметилциклопропан и
Н3С- -СН3
1,2 - диметилциклопропан
  б) б)
 СН3 СН3   метилциклобутан
метилциклобутан
 и
циклопентан
Межклассовая (с алкенами) и
циклопентан
Межклассовая (с алкенами)
|
  Углеродного скелета
СН3 Углеродного скелета
СН3
 СН3
1,2 – диметилбензол
(о – ксилол)
СН3
СН3
1,3 – диметилбензол
(м – ксилол) СН3
1,2 – диметилбензол
(о – ксилол)
СН3
СН3
1,3 – диметилбензол
(м – ксилол)
1,4 – диметилбензол
С2Н5
этилбензол | ||||||
| Отношение к раствору KMnO4 (окисление) | Не реагируют |
Обесцвечивают
[O]
 С=С С - С
׀ ׀
ОН ОН
этиленгликоль
реакция Качественная С=С С - С
׀ ׀
ОН ОН
этиленгликоль
реакция Качественная
| Обесцвечивают Качественная реакция | Не реагируют |
Бензол не реагирует.
 Гомологи обесцвечивают.
[O] Гомологи обесцвечивают.
[O]
  С2Н5 С2Н5

 СООН
бензойная кислота СООН
бензойная кислота
| ||||||
| Отношение к бромной воде Br2 (H2O) | Не реагируют | Обесцвечивают СН2=СН2 + Br2 (H2O) → СH2Br-CH2Br 1,2 - дибромэтан Качественная реакция | Обесцвечивают СН≡СН + Br2 (H2O) → СHBr=CHBr (1 стадия) 1,2 – дибромэтен СHBr=CHBr + Br2 (H2O) → СHBr2-CHBr2 (2 стадия) 1,1,2,2 – тетрабромэтан Качественная реакция | Не реагируют | Бензол не реагирует. Гомологи – обесцвечивают. | ||||||
| Взаимодействие с галогенами (Cl2, Br2) | hν, t
 СН4 + Cl2
CH3Cl + HCl
хлорметан
hν, t СН4 + Cl2
CH3Cl + HCl
хлорметан
hν, t
 С2Н6 + Br2
C2H5Вr + HBr
бромэтан С2Н6 + Br2
C2H5Вr + HBr
бромэтан
| СН2=СН2 + Cl2 → СН2Cl-СН2Cl 1,2 - дихлорэтан | СН≡СН + Cl2 → СНCl=СНCl (1 стадия) 1,2 – дихлорэтен СНCl=СНCl + Cl2 → СНCl2-СНCl2 (2 стадия) 1,1,2,2 - тетрахлорэтан |  t t
 + Br2
CH2Br-CH2-CH2Br
1,3 – дибромпропан + Br2
CH2Br-CH2-CH2Br
1,3 – дибромпропан
t
+ НBr
бромциклогексан |  t, FeBr3
t, FeBr3
 + Br2 + Br2
  Br
+ HBr
бромбензол Br
+ HBr
бромбензол
 hν
hν
 + 3Cl2 + 3Cl2
 Сl Cl
Cl Cl
Cl Cl
1,2,3,4,5,6 – гексахлор -
циклогексан
(гексахлоран) Сl Cl
Cl Cl
Cl Cl
1,2,3,4,5,6 – гексахлор -
циклогексан
(гексахлоран)
| ||||||
| Каталитическое гидрирование | Нет | p, t, cat
 СН2=СН2 + Н2
CH3-CH3
этан СН2=СН2 + Н2
CH3-CH3
этан
| p, t, cat
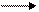 СН2≡СН2 + 2Н2
CH3-CH3
этан (в две стадии) СН2≡СН2 + 2Н2
CH3-CH3
этан (в две стадии)
|  p, t, cat p, t, cat
 + Н2
CH3-CH2- CH3
пропан + Н2
CH3-CH2- CH3
пропан
|  p, t, cat
p, t, cat
 + Н2 + Н2
 Циклогексан
Циклогексан
| ||||||
| Нитрование (HO-NO2) | Реакция Коновалова
t
 СН4 + HNO3
разбавл.
СН3NO2 + Н2О
нитрометан СН4 + HNO3
разбавл.
СН3NO2 + Н2О
нитрометан
|  t, H2SO4
концентр. t, H2SO4
концентр.
 + HNO3
концентр. + HNO3
концентр.

 NO2 + Н2О
нитробензол NO2 + Н2О
нитробензол
| |||||||||
| Горение | При полном горении образуется углекислый газ СО2 и вода Н2О | ||||||||||
| Гидрогалогенирование (HCl, HBr) | CH2=CH-CH3 + HCl → CH3-CHCl-CH3 2 – хлорпропан По правилу | CH≡C-CH3 + HCl → CH2=CCl-CH3 (1 стадия) 2 – хлорпропен CH2=CCl-CH3 + HCl → CH3-CCl2-CH3 (2 стадия) 2,2 - дихлорпропан Марковникова | |||||||||
| Гидратация (+ Н2О) | CH2=CH-CH3 + H2О → CH3-CHОН -CH3 пропанол – 2 (спирт) По правилу | H+, Hg2+
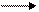 CH≡CH + H2О CH≡CH + H2О
 CH3-C=O (реакция
Кучерова)
H
этаналь (альдегид)
Марковникова CH3-C=O (реакция
Кучерова)
H
этаналь (альдегид)
Марковникова
| |||||||||
| Полимеризация |
p, t, cat
 nCH2=CH2 nCH2=CH2
  (СН2-СН2) n
полиэтилен
p, t, cat (СН2-СН2) n
полиэтилен
p, t, cat
 nCH2=CH2-СН3 nCH2=CH2-СН3
  (СН2-СН2) n
׀
СН3 полипропилен (СН2-СН2) n
׀
СН3 полипропилен
|
t, cat
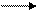 3С2Н2 С6Н6
бензол 3С2Н2 С6Н6
бензол
| |||||||||
| Применение | - топливо, горючее -получение сажи, водорода, непредельных углеводородов; - галогеналканы – растворители, анестезирующие средства, реагенты в органич. синтезах. | - получение галоген-производных (растворителей, анестезир. веществ); - получение этанола; - производство пластмасс; - получение антифризов (этиленгликоль) | - получение галоген-производных (растворителей); - в производстве полихлор-винила; - получение уксусного альдегида и уксусной кислоты | - для получения растворителей (С6H5Cl), лекарств, ВВ, анилина (С6H5NH2) и красителей; - в производстве гербицидов (гексахлоран) |
Дополнение:
1. Получение метана из карбида алюминия Al4C3 + 12H2O → 3CH4 ↑ + 4Al(OH)3
2. Получение ацетилена из карбида кальция CaC2 + 2H2O → C2H2 ↑ + Ca(OH)2
t t
3. Дегидрирование метана СН4 → С + Н2 и 2CH4 → 3H2 + C2H2
сажа ацетилен
t
4. Крекинг алканов С4Н10 → С2Н6 + С2Н4 (алкан и алкен)
этан этен
 Н2С СН2,
Н2С СН2, Н2С – СН2
Н2С – СН2



 Н3С СН3
Н3С СН3
 (п-ксилол)
(п-ксилол)

 Br
Br