СОДЕРЖАНИЕ
| Введение…………………………………………………………………….... | |
| 1 Способы фиксации азота…………………………………………………… | |
| 1.1 Химический способ ………………...……………………………... | |
| 1.2 Биологический способ ……………………………………………… | |
| 2 Бактериальные удобрения и перспективы развития направления …………… | |
| 3 Фиксация азота по-новому ……………………………………………….… | |
| Заключение…………………………………………………………………… | |
| Список использованных источников………………………………………….. |
ВВЕДЕНИЕ
Фиксация молекулярного азота — одиниз процессов, определяющих биологическуюпродуктивность на нашей планете, в связис чем его изучение отнесено к числу первостепенных задач современной биологии. Круговорот азота в природе является одним из ключевых звеньев биогеохимических цикловЗемли, атмосфера которой почти на 80% (пообъему) состоит из этого химического элемента и служит его основным источником.
Азот входит в состав протеинов, а также других молекул, составляющих основу структурной организации всех уровней живого.Человеку и животным он необходим в видепротеинов животного и растительного происхождения, растениям — солей азотнойкислоты и ионов аммония.
Экономический и экологический кризис, снижение качества продукции растениеводства, падение естественного плодородия почв обусловливают всевозрастающее внимание к биологическому земледелию, суть которого заключается в использовании потенциальных возможностей естественных экосистем, в частности микроорганизмов азотфиксаторов [1,2].
Способы фиксации азота
Существует два способа обеспечения растений азотным питанием denovo:
- биологический (фиксация молекулярного азота живыми организмами);
- химический (внесение азотных удобрений) [3].
Химический способ
Немецкие химики Ф.Габер и К.Бош создали процесс, позволяющий превратить атмосферный азот в смеси с водородом в аммиак (промышленный синтез).Это экзотермическая обратимая реакция.
При обычных условиях она протекает с очень маленькой скоростью, поэтому, чтобы её увеличить, применяют катализатор (металлическое железо с добавками Al2O3, K2O) и повышенную температуру (t = 400-600оС). При этом скорость реакции существенно возрастает, но зато резко уменьшается выход NH3 (т.к. при повышении t равновесие смещается в сторону обратной реакции). Чтобы повысить выход NH3, увеличивают давление. Это приводит к смещению равновесия в сторону прямой реакции. В заводских условиях применяют давление от 15 до 100 МПа. Большие значения давления использовать нецелесообразно, т.к. резко возрастает вероятность разрушения оборудования и удорожается сам процесс производства. Максимальный выход NH3 при этом может достигать 60%. Непрореагировавшую азото-водородную смесь после отделения NH3 и доочистки опять возвращают в колонну синтеза NH3. Благодаря такой циркуляции, использование азото-водородной смеси удается довести до 95%.
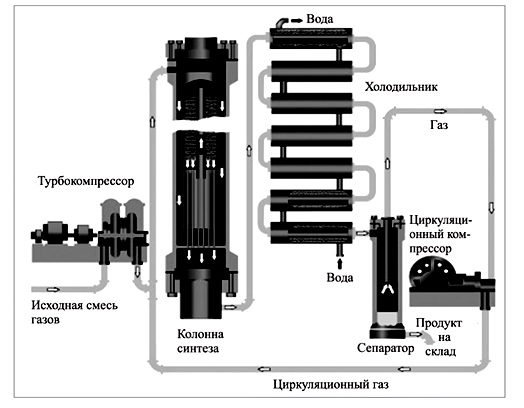
Рисунок 1 – Промышленный синтез аммиака
Условия, в которых происходит синтез аммиака (высокие температура и давление), весьма жесткие: все дело в высокой химической инертности азота. Два атома азота связаны тройной связью, однако она заметно отличается от тройной связи между атомами углерода (например, в ацетилене). Труднее всего разорвать в азоте первую связь из трех, для этого требуется заметная затрата энергии – 125 ккал/моль. Интересно, что разрыв именно первой связи в азоте наиболее труден, вторая связь раскрывается заметно легче – 63 ккал/моль, и еще легче третья связь – 37 ккал/моль. Поэтому в реакциях с участием молекулярного азота обычно раскрываются все три связи. Главное – расшевелить самую прочную, первую связь, а остальные как будто бы сами «покатятся под горку».
Итак, удалось решить главную задачу – химически связать атмосферный азот с помощью процесса Габера–Боша. Громадное количество современных заводов синтезируют аммиак именно таким способом. Далее полученный аммиак каталитически окисляют до оксидов азота, в конечном итоге получают азотную кислоту и нитраты, которые помимо сельского хозяйства и изготовления взрывчатых веществ, необходимы также в производстве красителей, медикаментов и в химической отрасли промышленности [4].
Биологический способ
Атмосферный азот усваивают (фиксируют) почвенные микроорганизмы. Биологическая фиксация производится определенными микроорганизмами – диазотрофами – в одиночку или в симбиозе с некоторыми растениями и животными. Существует три группы азотфиксирующих микроорганизмов:
- свободноживущие азотфиксирующие бактерии:
а)свободноживущие нефотосинтезирующие облигатно анаэробные бактерии. Данные микроорганизмы проживают в почвах и разлагающихся веществах растительного происхождения (Clostridium), также некоторые метаногены способны фиксировать азот в кишечнике животных;
б) факультативные анаэробы. Книмотносятся: Klebsiella pneumonia, PaenibacillusPolymyxa, Bacillusmacerans и EscherichiaIntermedia;
в) свободноживущиенефотосинтезирующиеаэробныебактерии Azotobacter, BeijerinckiaиDerxia;
г) свободноживущие фотосинтезирующие бактерии Chromatium, Rhodopseudomonas, Rhodospirillum. Сюда также относятся цианобактерии (Anabaenacylindrica и Nostoc communa);
д) свободноживущие хемосинтезирующие бактерии (Desulfovibrio.)
- ассоциативные азотфиксирующие бактерии. К ним относятся микроорганизмы, находящиеся в тесной связи с растениями и использующие их выделения как источник органического вещества, например, Azotobacter и сахарный тростник;
- симбиотические диазотрофы. К ним относятся:
а) бактерии, вступающие в симбиоз с растениями семейства бобовых. Кислород связывается с белком леггемоглобином в корневых клубеньках и транспортируется в клетку в количестве, необходимого для дыхания. К таким микроорганизмам относятся представители рода Rhizobium;
б) бактерии, вступающих в симбиоз с двудольными растениями (Frankia);
в) симбиотические цианобактерии. Некоторые виды связываются с грибами, лишайниками и папоротниками (Anabaena) [5].
Фиксация биологического азота осуществляется в результате процесса превращения азота в аммиак, катализируемого ферментом нитрогеназой.
Нитрогеназа представляет собой ансамбль из белковых молекул (рис. 2):
– белок 1 – молибдоферредоксин (Мо – Fe – протеин), или собственно нитрогеназа, содержащая четыре идентичные субъединицы, в каждую из которых входят два атома молибдена, негеминовое железо, лабильный сульфид;
– белок 2 – азоферредоксин, или редуктазный компонент (Fe – белок) является димером, содержит негеминовое железо и лабильный сульфид.
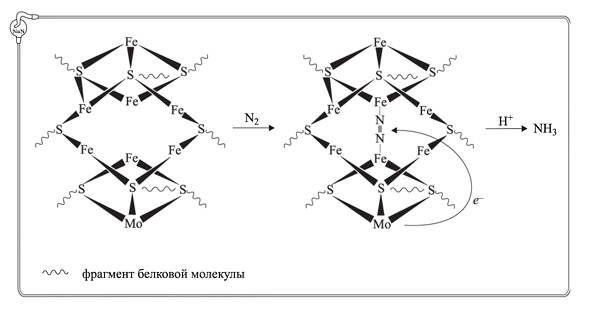
Рисунок 2 – фиксация молекулы азота каталитическими центрами нитрогеназы
Восстановление молекулярного азота до NH3 идет в три этапа по схеме (рис.3):

Рисунок 3 – этапы восстановления молекулярного азота
Для восстановления N2 в NH3 требуется 6 электронов и 6 протонов источником которых должен быть мощный восстановитель. Донором водорода для нитрогеназного комплекса является НАДФН+Н+. Для фиксации азота требуется также энергия в виде АТФ. На каждый перенесенный электрон затрачивается 1 молекула АТФ. Электроны переносятся к белкам нитрогеназы двумя различными типами белков – переносчиков электронов: ферредоксином (Fe –S белок) и флаводоксином (ФМН – содержащий белок).
Превращение азота в аммиак можно представить следующей схемой (рис. 4):
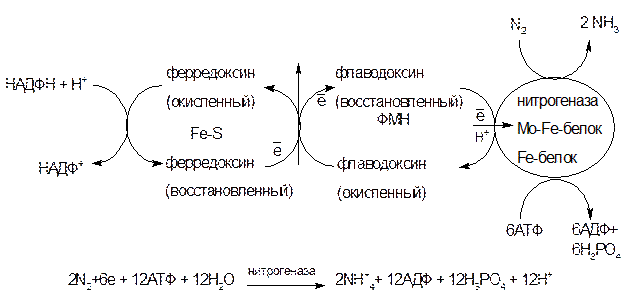
Рисунок 4 – превращение азота в аммиак
Наконец, N2 связывается с белком 1 и восстанавливается до NH3 – продукт фиксации азота микроорганизмами NH3 может прямо использоваться растениями для всех азотосодержащих органических соединений [4,6].
Бактериальные удобрения и перспективы развития направления
Микрофлора почвы оказывает непосредственное влияние на её плодородие и, как следствие, на урожайность растений. Почвенные микроорганизмы в процессе роста и развития улучшают структуру почвы, накапливают в ней питательные вещества, минерализуют различные органические соединения, превращая их в легко усвояемые растением компоненты питания. Для стимуляции этих процессов применяют различные бактериальные удобрения, обогащающие ризосферу растений полезными микроорганизмами. Микроорганизмы, используемые для производства бактериальных препаратов, способствуют снабжению растений не только элементами минерального питания, но и физиологически активными веществами (фитогормонами, витаминами и др.). Экспериментально установлено, что азот, фиксированный микроорганизмами,на 100% усваивается растениями, в то время каказот минеральных удобрений - всего на 50% [7].
В настоящее время выпускают такие бактериальные удобрения, как нитрагин, ризоторфин, азотобактерин, фосфобактерин, экстрасол.
Производственный процесс включает стадии:
- культивирование бактерий на производственных качалках в колбах или в ферментерах;
- выделение конечного продукта
- подготовка носителя(фасовка и стерилизация субстрата, внесение добавок)или тары для жидкой препаративной формы(стерилизация емкостей);
- инокуляция носителя [1].
Одновременно не прекращаются работы по выделению новых штаммов клубеньковых бактерий. В Китае американской экспедиции микробиологов удалось выделить новый штамм, скорость роста и размножения которого была почти в трираза выше, чем у бактерий почв США. Однако уровень азотфиксациикитайского штамма был невысоким. Плазмида, выделенная из
китайского штамма, была пересажена американскому коллекционному штамму, отличающемуся активной азотфиксацией, но низкой скоростью роста. В результате получили новый штамм, унаследовавший положительные качества обоих родителей и сразу же запушенный в производство.
В Индии, где почвы в основном кислые, был выведенкислотоустойчивый штамм ризобий, способный активно фиксироватьазот даже при pH почвенного раствора, составляющей 4,5. ВКанаде был получен холодоустойчивый штамм, который обеспечивалбольший приток азота в почву за вегетационный сезон благодаряболее раннему началу азотфиксации - уже при температуре+ 10 ОС. При этом эталонный штамм ризобий начинает фиксироватьазот при температуре не ниже + 17 ОС.
Весьма перспективным направлением в настоящее время являетсяусовершенствование непосредственно самого нитрогеназногокомплекса клубеньковых бактерий при помощи методов генной инженерии.В Национальном университете Австралии проводятся исследованияпо переносу генов, отвечающих за азотфиксацию, не толькоот одного вида клубеньковых бактерий к другому, но и к почвеннымбактериям, не способным к азотфиксации, например к бактериямродов Lignobacter, Corinebacterium и др. Растения, инокулированныетакими бактериями, в 10 случаях из 100 приобретали способностьобразовывать псевдоклубеиьки [7].