Все биологические реакции сопровождаются изменениями энергии, так что термин «биоэнергетика» можно принять ко всей биологии. Центральной проблемой биоэнергетики на протяжении 30 лет было выяснение механизма, с помощью которого энергия, освобождаемая при окислении субстратов или при поглощении света, может использоваться на синтез АТР из АDР и Рi или перенос ионов через мембрану против градиента их концентрации. Хотя синтез АТР частично происходит и в растворимых ферментных системах (субстратное фосфорилирование), все же большая часть АТР образуется в ферментных комплексах, расположенных в мембранах определенных классов. К таким «сопрягающим » мембранам относятся плазматическая мембрана прокариотических клеток (бактерий и сине-зеленых водорослей), внутренняя мембрана митохондрий и мембрана тилакоидов хлоропластов. Механизмы синтеза АТР и транспорта ионов в этих мембранах весьма близки, несмотря на различную природу различных источников энергии. Это позволяет выделить изучение этих механизмов в отдельную область, названную энергетическое сопряжение или биоэнергетика. Сопрягающие мембраны имеют ряд отличительных черт. Каждая такая мембрана имеет белковые ансамбли двух типов. Одни из них обычно называют АТР-азой, хотя более правильным было бы название АТР-синтетазы, т.к. он катализирует энергозависимый синтез АТР из АDР и Рi. Этот комплекс присутствует во всех сопрягающих мембранах. Природа второго белкового ансамбля зависит от первичного источника энергии, используемого в данной мембране. В случае митохондрий и аэробных бактерий – это дыхательная цепь, катализирующая перенос электронов от субстратов к конечным акцепторам, таким как О2. В хлоропластах и фотосинтезирующих бактериях сходная система обеспечивает использование энергии поглощенных квантов света.
hυ →  →? → ~АТР
→? → ~АТР
о/в реакции →  →? → ~АТР
→? → ~АТР
Поиск «энергетического интермедиата» (энергетического посредника, от лат. intermedius – находящийся по середине), связывающего эти две системы, оказалcя чрезвычайно сложной проблемой. Многолетние попытки найти высокоэнергетическое химическое соединение, сопрягающее окисление с синтезом АТР, не дали успеха. Именно в этот момент на научной сцене появился Питер Митчелл со своей хемоосмотической гипотезой (ХОГ) (1961 г.), в которой утверждалось, что единственным «интермедиатом» служит градиент протонов на мембране. ХОГ была подвергнута самой тщательной проверке, пожалуй, более тщательной, чем любая другая биохимическая теория. В результате П.Митчеллу в 1978г. была присуждена Нобелевская премия по химии.
Хемоосмотическая теория Митчелла в настоящее время является более распространенной, объясняющей механизм образования АТР. При разработке этой теории автор использовал как собственные результаты опытов, так и экспериментальные данные других исследований.
Опытами Пэкера и Хинда было показано, что при освещении хлоропластов in vitro величина рН внешнего раствора возрастает, в то время как рН внутри тилакоидов понижается (рис. 1). На основании этих опытов Митчелл выдвинул предположение, согласно которому в результате работы ЭТЦ, локализованной в мембране тилакоидов, происходит активный перенос Н+ через мембрану стромального пространства хлоропластов во внутритилакоидное пространство. В результате такого переноса происходит разделение зарядов и накопление протонов внутри тилакоидов. При этом на одной стороне мембраны возникает положительный, а на другой стороне – отрицательный заряд. Образование такого градиента концентрации протонов на внутренней и внешней поверхности тилакоидной мембраны и представляет собой богатое энергией состояние структур хлоропластов. Возникший электрохимический мембранный потенциал является движущей силой для синтеза АТР.
Электрохимический потенциал ионов водорода (∆μН+) включает две составляющие: концентрационную (∆рН), возникающую в результате неравномерного распределения ионов Н+ по обе стороны мембраны, и электрическую (∆Ψ), обусловленную возникновением противоположного заряда на поверхности мембран, т.е. образованием мембранного потенциала.
Основным доказательством определяющей роли рН в фосфорилировании являются опыты с кислотно-основными переходами, в результате которых было показано, что в данных условиях синтез АТР может осуществляться в темноте. Так, Ягендорф в своих опытах искусственно создавал градиент Н+ в темноте в результате последовательного переноса хлоропластов из кислой среды в щелочную. При этом наблюдалось образование АТР.
 ∆ рН АТР
∆ рН АТР
Подтверждают эту теорию и опыты с разобщителями. Так, при разобщении ∆рН хлористым аммонием NH4Cl, ATP не образуется, хотя ток  происходит, о чем свидетельствует факт восстановления NADPH2 (или экзогенных акцепторов электронов).
происходит, о чем свидетельствует факт восстановления NADPH2 (или экзогенных акцепторов электронов).

 Н+ NH3
Н+ NH3
 | |||||
 | |||||
 | |||||


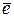 ∆рН ~АТР
∆рН ~АТР
«гасится»
NH3 проникает быстрее, чем Н+ и связывает Н+ внутри тилакоида, тем самым гасит образование ∆рН.
Суть механизма протонного насоса заключается в следующем. В ЭТЦ наблюдается чередование переносчиков 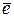 (цитохромы) и компонентов, переносящих
(цитохромы) и компонентов, переносящих  вместе с протонами (пластохиноны).
вместе с протонами (пластохиноны).
 |  | ||
Н+



 hυ тилакоид
hυ тилакоид

рис. 1О
+2Н+
 +2
+2 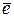

 О Н
О Н



 ║
║







 | |||||
 |  | ||||


 ║
║
 О
О
ОН
хинон гидрохинон
Для восстановления хинона необходимы  и он их получает от цитохрома, но кроме
и он их получает от цитохрома, но кроме  для его восстановления необходимы и Н+, которые он забирает из наружной фазы. Далее Пх отдает
для его восстановления необходимы и Н+, которые он забирает из наружной фазы. Далее Пх отдает  цит, а Н+ выделяется во внутритилакоидное пространство. Векторный перенос обусловлен анизотропией мембран.
цит, а Н+ выделяется во внутритилакоидное пространство. Векторный перенос обусловлен анизотропией мембран.
Согласно последним представлениям, механизм преобразования электрохимической энергии в форму ~АТР сопряжен с функционированием АТР-азного комплекса (прямой и косвенный механизм синтеза АТР, см. в теме «дыхание»).
Образование ∆рН идет не только за счет работы протонной помпы, но и за счет фотолиза воды (см. Гавриленко, стр.209).