Что такое диализ, электродиализ, ультрафильтрация,для чего и как они используются, какое значение имеют при лечении больных и в производстве лекарственных препаратов.?
Диализ является простейшим методом очистки коллоидных систем. Очистка коллоидных методом диализа заключается в том, что с помощью полупроницаемой перегородки (мембраны) коллоидные мицеллы могут быть отделены от примесей растворенных в дисперсионной среде низкомолекулярных веществ. При диализе молекулы растворенного низкомолекулярного вещества проходят через мембрану, а коллоидные частицы, неспособные диализировать (проникать через мембрану), остаются за ней в виде очищенного коллоидного раствора. Явление диализа для коллоидных систем возможно благодаря тому, что размер мицелл гораздо больше размера молекул низкомолекулярных веществ.
Простейшим прибором для диализа - диализатором - является мешочек из полупроницаемого материала (коллодия), в который помещается диализируемая жидкость. Мешочек опускается в сосуд с растворителем (водой). Периодически или постоянно меняя растворитель в диализаторе можно практически полностью удалить из коллоидного раствора примеси электролитов и низкомолекулярных неэлектролитов. Недостатком метода является большая длительность процесса очистки (недели, месяцы). Отчасти также недостатком диализа является факт, что длительный диализ обусловливает не только удаление из раствора примесей, но и стабилизатора, что может повлечь за собой коагуляцию коллоидного раствора.
В настоящее время существует много усовершенствованных конструкций диализаторов, ускоряющих процесс диализа. Интенсификация процесса достигается увеличением поверхности, через которую идет диализ, непрерывной заменой растворителя и нагреванием, ускоряющем процесс.
Процесс диализа обусловлен процессами осмоса и диффузии, что объясняет методы интенсификации процесса диализа.
Электродиализ - процесс диализа, ускоряемый действием электрического тока. Электродиализ применяют для очистки коллоидных растворов, загрязненных электролитами. В случае необходимости очистки коллоидных растворов от низкомолекулярных неэлектролитов, процесс электродиализа малоэффективен. В принципе, процесс электродиализа мало отличается от обычного диализа. Существенное отличие заключается в том, что с помощью внешнего электрического поля удается более быстро и полно отделить катионы и анионы электролитов от коллоидного раствора.
Простейший электродиализатор представляет собой сосуд, разделенный на 3 камеры. В среднюю камеру, снабженную мешалкой, наливают подлежащий очистке коллоидный раствор. В боковые камеры помещены электроды, подключенные к источнику постоянного тока и трубки для подвода и отвода растворителя (воды). Под действием электрического поля происходит перенос катионов из средней камеры в катодную камеру, а анионов - в анодную.
Преимуществом электродиализа перед обычным диализом является малое количество времени, необходимое для очистки (минуты, часы).
Следует отметить, что электродиализ особенно эффективен только после предварительной очистки с помощью обычного диализа, когда скорость диффузии из-за падения градиента концентрации электролитов между золем и водой мала и можно применять электрическое поле большого напряжения, не боясь сильного разогревания золя.
Ультрафильтрация - фильтрование коллоидных растворов через полупроницаемую мембрану, пропускающую дисперсионную среду с низкомолекулярными примесями и задерживающую частицы дисперсной фазы или макромолекулы. Для ускорения процесса ультрафильтрации ее проводят при перепаде давления по обе стороны мембраны: под вакуумом или повышенным давлением. То есть, ультрафильтрация есть ничто иное, как диализ, проводимый под давлением.
Ультрафильрация позволяет скорее отделить от коллоидного раствора электролиты и другие примеси (низкомолекулярные неэлектролиты), чем это происходит при диализе.
При ультрафильтрации достигают высокой степени очистки золя, периодически разбавляя последний водой. При разбавлении водой золь будет содержать меньше низкомолекулярных примесей, но одновременно и стабилизаторов.
На конечной стадии путем отсасывания дисперсионной среды можно сконцентрировать коллоидный раствор. При этом важно, что повышается концентрация только дисперсной фазы, состав же дисперсионной среды остается практически постоянным.
Ультрафильтрация может применяться в сочетании с электродиализом (электроультрафильтрация), благодаря чему значительно ускоряется удаление электролитов из коллоидного раствора.
Применение мембран с определенным размером пор позволяет разделить коллоидные частицы на фракции по размерам и ориентировочно определить эти размеры.
Предложено много приборов для проведения ультрафильтрации. Так как ультрафильтрация всегда проходит под давлением, то во всех приборах для ультрафильтрации мембрана либо накладывается на пластинку с мелкими отверствиями, служащую для нее опорой, либо непосредственно получается на стенках неглазурованного фарфорового сосуда. Например, ультрафильтры Бехгольда получают путем нанесения на стенки пористого фарфорового сосуда разбавленного коллодия и последующего его высушивания.
Все это говорит о том, что ультрафильтрация является не только методом очистки коллоидных систем, но и может быть использована для дисперсионного анализа и препаративного разделения дисперсных систем.
Компенсационный диализ и вивидиализ, значение методов очистки коллоидных систем в медицине.
Компенсационный диализ и вивидиализ - методы, разработанные для исследования биологических жидкостей, представляющих собой коллоидные системы.
Принцип метода компенсационного диализа состоит в том, что в диализаторе вместо чистого растворителя используют растворы определяемых низкомолекулярных веществ различной концентрации. Например, для определения свободного, не связанного с белками, сахара крови проводят ее диализ против изотонического солевого раствора, содержащего различные концентрации сахара. В том растворе, где концентрация сахара равна концентрации свободного сахара в сыворотке крови, в ходе диализа концентрация сахара не изменяется. Этот метод позволил выявить присутствие в крови глюкозы и мочевины в свободном состоянии.
К этому методу близок метод вивидиализа для прижизненного определения в крови низкомолекулярных веществ. Для проведения анализа в концы перерезанного кровеносного сосуда вставляют стеклянные канюли, разветвленные части которых соединены между собой трубками из полупроницаемого материала, и всю систему помещают в сосуд, заполненный физиологическим раствором соли или водой. Таким методом было обнаружено, что в крови помимо глюкозы находятся свободные аминокислоты.
Принцип компенсационного вивидиализа был использован при создании аппарата, названного "искусственной почкой". С помощью него можно очищать кровь больного от различных низкомолекулярных веществ - продуктов обмена, замещая временно функцию больной почки при таких показаниях, как острая почечная недостаточность в результате отравлений, при тяжелых ожогах и т.п.
10.Как классифицируют дисперсные системы по агрегатному состоянию фаз?Дать объяснения и пример.
В соответствии с составом и строением коллоидные дисперсии классифицируются следующим образом:
| ТИПЫКОЛЛОИДНЫХ СИСТЕМ | |||
| Дисперсная фаза | Дисперсионная среда | Наименование | Примеры |
| Жидкость | Газ | Жидкие аэрозоли | Туман, кучевые облака |
| Твердое тело | Газ | Твердые аэрозоли | Дым, пыль, перистые облака |
| Газ | Жидкость | Пены | Мыльные пены |
| Жидкость | Жидкость | Эмульсии | Молоко (М/В), масло (В/М), нефть |
| Твердое тело | Жидкость | Золи | Жидкая глина, зубная паста |
| Газ | Твердое тело | Твердые пены | Пенополистирол, пенопласт, пенобетон |
| Жидкость | Твердое тело | Твердые эмульсии | Опал, жемчуг, почва |
| Твердое тело | Твердое тело | Твердые суспензии | Окрашенные пластмассы |
11.Дать общую характеристику методов получения и необходимых условий образования лиофобных коллоидных систем конденсационным методом?
Для характеристики взаимодействия между веществом дисперсной фазы и жидкой дисперсионной средой используют термины лиофобный («боящийся жидкости») и лиофильный («любящий жидкость») используются для описания тенденции поверхности или функциональной группы к смачиванию или сольватации. Если жидкой дисперсионной средой является вода, используются термины гидрофобный и гидрофильный
Чем обусловлено броуновское движение частиц в коллоидных растворах, отчего зависит его интенсивность?
Броуновское движение (название дано в честь английского ботаника Броуна, обнаружившего с помощью микроскопа непрерывное движение мелких частичек цветочной пыльцы, взвешенных в воде) проявляется в хаотическом и непрерывном движении частиц дисперсной фазы под действием ударов молекул растворителя (дисперсионной среды), находящихся в состоянии интенсивного теплового движения. В зависимости от размера частиц их движение может быть различным.
Частицы коллоидной степени дисперсности, испытывая с разных сторон многочисленные удары молекул жидкости, могут перемещаться поступательно в самых разнообразных направлениях. Если частица имеет сравнительно большой размер, то число ударов велико, и по соответствующему закону статистики результирующий импульс становится равным нулю, такая частица не может двигаться под действием теплового движения молекул.
Кроме того, частицы с большой массой обладают инерционностью и малочувствительны к ударам молекул. Очень малые частицы имеют значительно меньшие массу и поверхность. На такую частицу будет приходиться существенно меньшее число ударов, поэтому вероятность неравномерного распределения импульсов, получаемых с разных сторон, увеличивается. Это происходит как вследствие неодинакового числа ударов с разных сторон частицы, так и вследствие различной энергии молекул, сталкивающих с частицей. В зависимости от размеров частица приобретает колебательное, вращательное и поступательное движение.
Таким образом, броуновское движение является следствием теплового движения в дисперсионной среде и прямым отражением статистики.
Броуновское движение – следствие случайных микроотклонений (флуктуаций), эффект которых возрастает с уменьшением размеров системы, и наглядное проявление отклонений от второго закона термодинамики в микросистемах, т.е. подтверждение его статистического характера.
21.Как проявляется осмотическое давление в коллоидных растворах, чем оно отличается от осмотического давления истинных растворов?.
Осмотическое давление. Уравнение Вант-Гоффа
уравнение Вант-Гоффа:
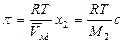 (3)
(3)
где 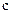 - массовая концентрация;
- массовая концентрация; 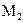 - молекулярная масса частицы.
- молекулярная масса частицы.
Осмотическое давление дисперсной системы определяется только численной концентрацией и зависит от природы и размера частиц. Малое осмотическое давление коллоидной системы объясняется благодаря большой массе коллоидных частиц при одной и той жен весовой концентрации численная концентрация коллоидной системы всегда значительно меньше, чем у истинного раствора.
Вторая особенность осмотического давления лиозолей – его непостоянство – объясняется явлением агрегации, характерным для коллоидных систем.
Малое значение и непостоянство осмотического давления лиозолей являются причиной того, что осмометрия, а также криоскопия и эбуллиоскопия не применяются для определения численной концентрации или размера коллоидных систем.
Как проявляется диффузия в коллоидных системах сравнительно с другими дисперсными системами? какие характеристики коллоидных систем позволяет установить определение их скорости диффузии?
Диффузией называют самопроизвольный процесс выравнивания концентрации частиц по всему объему раствора или газа под влиянием броуновского движения.
Процесс диффузии идет самопроизвольно, поскольку он сопровождается увеличением энтропии системы. Равномерное распределение вещества в системе отвечает наиболее вероятному ее состоянию.
Часто за причину диффузии принимают осмотическое давление. Это представление было развито Нернстом (1885 г.). Так как осмотическое давление может проявляться лишь при наличии полунепроницаемой перегородки, то это давление бессмысленно рассматривать как какую-то реальную силу, существующую вне связи с мембраной. Тем не менее, осмотическое давление, являющееся также результатом хаотического движения молекул, иногда удобно принимать за причину диффузии.
Что такое седиментация частиц и седиментационное равновесие в коллоидных системах?Какие количественные параметры их характеризуют? Ультрацинтриугирование и его применение при исследовании коллоидных систем?
Седиментацией- называют процесс оседания частиц дисперсной фазы в жидкой или газообразной среды под действием силы тяжести.
Между процессами седиментации и диффузии устанавливается равновесие, которое называется седиментационно- диффузионным равновесием.
Более значительной центробежной силой обладает ультрацентрифуга.
Что такое пептизация? Дать объяснения, привести пример.
Пептизацция – расщепление агрегатов, возникших при коагуляции дисперсных систем, на первичные частицы под действием жидкой среды (например воды). Пептизация – один из способов получения коллоидных растворов.\
16. В чем состоит получение коллоидных систем методом химической конденсации? Разновидности метода и их применение.
. Методы, основанные на образовании частиц в результате кристаллизации или конденсации, называют конденсационными
13. В чем состоит получение коллоидных систем методом физического диспергирования?
Известны два способа получения дисперсных систем. В одном из них тонко измельчают (диспергируют) твердые и жидкие вещества в соответствующей дисперсионной среде, в другом вызывают образование частиц дисперсионной фазы из отдельных молекул или ионов.
Методы получения дисперсных систем измельчением более крупных частиц называют диспергационными.