Геном эукариот составляют уникальные и повторяющиеся последовательности нуклеотидов. Содержание уникальных последовательностей в геноме, определенное на основании кинетики реассоциации фрагментированной ДНК, варьирует у разных организмов, и их доля составляет 15–98% от всей ДНК. Несмотря на то, что во фракцию уникальных последовательностей попадают многие структурные гены, большая часть уникальных последовательностей является некодирующей и обычно не заключает в себе генетической информации в общепринятом значении этого термина: не кодирует функционально значимые полипептидные цепи или РНК. Хорошо известным примером таких уникальных последовательностей являются интроны, общий размер которых, как правило, на порядок и более превышает суммарный размер экзонов содержащих их генов.
Эволюционное возникновение мозаичной (интрон–экзонной) структуры генов эукариот, так же как и консервативный характер наследования размеров и взаимного расположения интронов в генах, не находит в настоящее время исчерпывающего объяснения из-за кажущегося отсутствия фактора давления естественного отбора на последовательности нуклеотидов без четких биологических функций. Наибольшее распространение получила концепция В. Гилберта (1977 г.), согласно которой появление интронов, по-видимому, совпавшее по времени с эволюционным возникновением многоклеточных организмов, обеспечило возможность обмена экзонами между неродственными генами (exon shuffling). Такой обмен должен сопровождаться образованием новых белков мозаичного строения, составленных из готовых полипептидных функционально значимых модулей (доменов), ранее принадлежавших другим белкам. Следствием этого, по мнению сторонников данной концепции, было резкое ускорение образования белков и ферментов с новыми функциями, а также глубокие эволюционные преобразования самих организмов, реализующих такие молекулярные механизмы. Эта точка зрения получила название "гипотезы позднего возникновения интронов" (intron late). В соответствии с другой гипотезой Дж.Е. Дарнелла и В.Ф. Дулиттла (1978 г.) современные интроны представляют собой "эволюционные реликты". Когда-то интроны были частью гигантских генов.
Не менее загадочным с эволюционной точки зрения остается и феномен появления в геноме многоклеточных организмов большого количества некодирующих повторяющихся последовательностей. Такие повторы представлены в гаплоидном геноме эукариот множественными копиями. В современной классификации повторов принято различать часто повторяющиеся последовательности, число которых превышает 105 на гаплоидный геном, и умеренно повторяющиеся, представленные 10–104 копиями. Хорошо изученным представителем первых является сателлитная ДНК, которая состоит из коротких тандемных повторов длиной 1–20 п.о., организованных в длинные блоки. Одними из первых среди повторяющихся последовательностей ДНК эукариот были открыты сателлитные ДНКтимуса телят. Свое название они получили на основании того, что при анализе суммарной эукариотической ДНК центрифугированием в градиенте плотности хлористого цезия они сопровождали основной пик оптической плотности в виде плеча (спутника, сателлита). Именно гомогенный нуклеотидный состав фракции сателлитных ДНК, определяемый наличием в ней многочисленных коротких повторов, изменял ее плавучую плотность, что легко обнаруживалось при центрифугировании. В своем классическом определении сателлитных ДНК Р.Д. Бриттен и соавт. (1974 г.) отмечали, что сателлиты – это минорный компонент ДНК, отделяющийся от основной ДНК при равновесном ультрацентрифугировании в градиенте плотности CsCl. Для сателлитов характерен ряд свойств, среди которых наиболее важны: а) быстрая и точная реассоциация в процессе ренатурации ДНК; б) множество копий; в) простая первичная структура; г) гомогенный состав (протяженные кластеры одних и тех же повторяющихся блоков последовательны); д) пурин–пиримидиновая асимметрия в распределении нуклеотидов по цепям ДНК; е) концентрирование в прицентромерном гетерохроматине; ж) ограниченная репликация (недорипликация) при политенизации хромосом; з) нахождение в составе хромосом в виде тандемно (друг за другом) расположенных кластеров. Содержание сателлитной ДНК в геноме эукариот может достигать 5–50% от суммарного количества ДНК. Микро - (от 1 до 4 п.о. в основном повторяющемся блоке) и минисателлитные (с б ó льшим числом п.о. в индивидуальном повторе) ДНК характеризуются высокой вариабельностью по числу копий в геномах организмов даже одного вида и в ряде случаев обладают генетической нестабильностью как в норме, так и при некоторых патологических состояниях организмов. Благодаря этому свойству мини- и микросателлиты часто называют тандемными повторами с изменяющимся числом копий VNTR (variable number of tandem repeats).
Другой тип повторов – диспергированные повторяющиеся последовательности ДНК, не организованные в крупные блоки, а рассеянные по геному. Повторы этого типа, иначе называемые умеренно повторяющимися последовательностями (medium reiterated frequency repeats – MERs), разделяют на два обширных класса: SINE (short interspersed elements) – короткие и LINE (long interspersed elements) – длинные диспергированные элементы. Длина SINE-элементов составляет 90–400 п.о., тогда как длина LINE-последовательностей может достигать 7 т.п.о. Хорошо изученными повторами класса SINE в геноме человека и некоторых приматов являются так называемые Alu-повторы, длина повторяющейся единицы которых составляет ~300 п.о. Alu-повторы представлены в геноме человека ~106 копиями и в среднем встречаются через каждые 4 т.п.о., составляя ~5% от суммарного количества ДНК. Аналогичные в структурном отношении повторы, названные B1, обнаружены в геноме мышей и под другими названиями описаны у многих млекопитающих.
Хотя LINE-последовательности заключают в себе гены обратных транскриптаз, что является признаком ретротранспозонов (мобильных генетических элементов животных, обладающих структурным сходством с геномом ретровирусов), для них характерно отсутствие последовательностей длинных концевых повторов (long terminal repeats – LTR), типичных для ретротранспозонов (подробнее о геноме ретровирусов см. раздел 7.2.7). В качестве примера LINE-последовательности можно упомянуть LINE-1-повтор, широко распространенный в геноме животных. LINE-1-элемент мышей содержит две открытые рамки считывания ORF-1 и ORF-2, вторая из которых кодирует белок, гомологичный обратной транскриптазе. ORF фланкированы короткими нетранслируемыми последовательностями, а сами LINE-1 – короткими прямыми повторами (SDR). 5’-Концевые последовательности повтора функционируют в качестве промоторов транскрипции. Этот участок LINE-1 грызунов (но не человека) построен из коротких тандемных повторов двух типов A и F, называемых мономерами. Длина мономеров у крыс составляет 600 п.о. При этом A- (но не F) мономеры обладают активностью промоторов.
Так же как и сателлитные ДНК, SINE- и LINE-повторы характеризуются генетической нестабильностью. Их общими чертами являются транскрибируемость и способность к транспозициям. Последовательности РНК, транскрибированные с умеренных повторов, обнаруживают среди гетерогенных ядерных РНК, где их доля достигает 20–30%. Имеются экспериментальные свидетельства того, что новые копии повторяющихся элементов обоих типов возникают в геноме в результате функционирования механизма, названного ретротранспозицией, или ретропозицией. При участии подобного механизма под действием обратной транскриптазы сначала образуется кДНК на матрице РНК-транскрипта соответствующего повтора, которая далее интегрируется в новый локус генома, как это имеет место у ретровирусов. Такой механизм дает возможность локально изменять число копий определенных последовательностей нуклеотидов в эукариотическом геноме. Тем не менее, большая часть LINE-последовательностей неспособна к транспозициям, и их ORF, по-видимому, могут быть отнесены к псевдогенам – неэкспрессирующимся последовательностям, гомологичным последовательностям истинных генов. Помимо вышеупомянутых повторяющихся последовательностей геном человека содержит более 100 000 копий MaLR-повторов длиной в 2–3 т.п.о., содержащих LTR, и несколько тысяч последовательностей генома ретровирусов.
Несмотря на широкую распространенность повторяющихся и уникальных некодирующих последовательностей в геноме эукариот и их очевидную активность во время жизненного цикла организмов, биологическое значение этих и других некодирующих элементов генома остается непонятным. Вызывает сомнение правильность активно обсуждаемой в литературе гипотезы об "эгоистичности" избыточной геномной ДНК, в соответствии с которой вся избыточная ДНК является геномным паразитом и распространяется в геноме в результате транспозиций точных копий немногочисленных исходных последовательностей. Действительно, слишком велики были бы энергетические затраты на биосинтез предшественников ДНК и самой ДНК в клетках, в которых содержание "паразитической" ДНК в геноме на 2–3 порядка превышает количество функционально значимой ДНК, заключающей в себе последовательности нуклеотидов генов. Клетки с геномом, "зараженным" эгоистической ДНК, не смогли бы выдерживать конкуренции с клетками, не содержащими "паразита", из-за значительного возрастания энергетических затрат на редупликацию генома. Кроме того, концепция эгоистической ДНК, в соответствии с которой предполагается отсутствие эволюционного давления отбора на "паразитические" последовательности нуклеотидов, не объясняет высокую консервативность мест локализации и размеров интронов в гомологичных генах филогенетически близких организмов, а также не указывает на механизм, поддерживающий число копий повторов на относительно постоянном уровне в ряду поколений организмов. Такого рода концепции не могут ответить на вопрос: где же предел, до которого может самопроизвольно увеличиваться размер генома клетки-хозяина в филогенезе?
Функциональную значимость избыточной ДНК лишь частично объясняют концепции, приписывающие ей структурную роль в пространственной организации генома и участие в конъюгации гомологичных хромосом в мейозе или репликации теломерных участков хромосом. Таким образом, основные положения знаменитого парадокса C, указывающие на необъяснимое присутствие в геноме эукариотических организмов большого количества избыточной ДНК, по-прежнему остаются загадочными и парадоксальными. Попытка нового объяснения основной функциональной роли "избыточной" ДНК в геноме эукариот сделана в разделе 5.3.
Хроматин
Хроматином называют сложную смесь веществ, из которых построены хромосомы эукариот. Основными компонентами хроматина являются ДНК, гистоны и негистоновые белки, образующие высокоупорядоченные в пространстве структуры. Соотношение ДНК и белка в хроматине составляет ~1:1, а основная масса белка хроматина представлена гистонами. Гистоны образуют семейство высококонсервативных основных белков, которые разделяются на пять больших классов, названных H1, H2A, H2B, H3 и H4. Размер полипептидных цепей гистонов лежит в пределах ~ 220 (H1) и 102 (H4) аминокислотных остатков. Гистон H1 сильно обогащен остатками Lys, для гистонов H2A и H2B характерно умеренное содержание Lys, полипептидные цепи гистонов H3 и H4 богаты Arg. Внутри каждого класса гистонов (за исключением H4) на основании аминокислотных последовательностей различают несколько субтипов этих белков. Такая множественность особенно характерна для гистонов класса H1 млекопитающих. В этом случае различают семь субтипов, названных H1.1–H1.5, H1o и H1t.
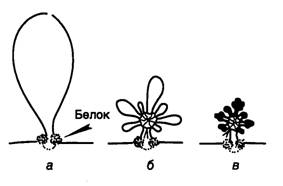
Рис. I.2. Схематическое изображение петельно-доменного уровня компактизации хроматина
а – фиксация петли хромомера на ядерном матриксе с помощью MAR/SAR-последовательностей и белков; б – "розетки", образованные из петли хромомера; в – конденсация петель "розеток" с участием нуклеосом и нуклеомеров
Важным результатом взаимодействия ДНК с белками в составе хроматина является ее компактизация. Суммарная длина ДНК, заключенной в ядре клеток человека, приближается к 1 м, тогда как средний диаметр ядра составляет ~10 мкм. Длина молекулы ДНК, заключенной в одной хромосоме человека, в среднем равняется ~4 см. В то же время длина метафазной хромосомы составляет ~4 мкм. Следовательно, ДНК метафазных хромосом человека компактизована по длине, по крайней мере, в ~104 раз. Степень компактизации ДНК в интерфазных ядрах значительно ниже и неравномерна в отдельных генетических локусах. С функциональной точки зрения различают эухроматин и гетерохроматин. Эухроматин характеризуется меньшей по сравнению с гетерохроматином компактизацией ДНК, и в нем главным образом локализуются активно экспрессирующиеся гены. В настоящее время широко распространено мнение о генетической инертности гетерохроматина. Поскольку его истинные функции сегодня нельзя считать установленными, эта точка зрения по мере накопления знаний о гетерохроматине может измениться. Уже сейчас в нем находят активно экспрессирующиеся гены.
Гетерохроматизация определенных участков хромосом часто сопровождается подавлением транскрипции имеющихся в них генов. В процесс гетерохроматизации могут быть вовлечены протяженные участки хромосом и даже целые хромосомы. В соответствии с этим считается, что регуляция транскрипции генов эукариот в основном происходит на двух уровнях. На первом из них компактизация или декомпактизация ДНК в хроматине может приводить к длительной инактивации или активации протяженных участков хромосом или даже целых хромосом в онтогенезе организма. Более тонкая регуляция транскрипции активированных участков хромосом достигается на втором уровне при участии негистоновых белков, включающих многочисленные факторы транскрипции.
Структурная организация хроматина и хромосом эукариот. Вопрос о структурной организации хроматина в интерфазных ядрах в настоящее время далек от своего разрешения. Это связано, прежде всего, со сложностью и динамичностью его структуры, которая легко меняется даже при незначительных экзогенных воздействиях. Большинство знаний о структуре хроматина было получено in vitro на препаратах фрагментированного хроматина, структура которого значительно отличается от таковой в нативных ядрах. В соответствии с распространенной точкой зрения различают три уровня структурной организации хроматина у эукариот: 1 ) нуклеосомная фибрилла; 2) соленоид, или нуклеомер; 3) петельно-доменная структура, включающая хромомеры.
Нуклеосомные фибриллы. В определенных условиях (при низкой ионной силе и в присутствии двухвалентных ионов металлов) в изолированном хроматине удается наблюдать регулярные структуры в виде протяженных фибрилл диаметром 10 нм, состоящих из нуклеосом. Эти фибриллярные структуры, в которых нуклеосомы расположены как бусы на нитке, рассматриваются в качестве низшего уровня упаковки ДНК эукариот в хроматине. Нуклеосомы, входящие в состав фибрилл, расположены более или менее равномерно вдоль молекулы ДНК на расстоянии 10–20 нм друг от друга. В состав нуклеосом входят четыре пары молекул гистонов: H2a, H2b, H3 и H4, а также одна молекула гистона H1. Данные по структуре нуклеосом в основном получены с использованием трех методов: рентгеноструктурного анализа низкого и высокого разрешения кристаллов нуклеосом, межмолекулярных сшивок белок–ДНК и расщепления ДНК в составе нуклеосом с помощью нуклеаз или радикалов гидроксила. На основании таких данных А. Клугом была построена модель нуклеосомы, в соответствии с которой ДНК (146 п.о.) в B-форме (правозакрученная спираль с шагом 10 п.о.) намотана на гистоновый октамер, в центральной части которого расположены гистоны Н3 и Н4, а на периферии – Н2а и Н2b. Диаметр такого нуклеосомного диска составляет 11 нм, а его толщина – 5,5 нм. Структура, состоящая из гистонового октамера и намотанной на него ДНК, получила название нуклеосомной к ó ровой частицы. К ó ровые частицы отделены друг от друга сегментами линкерной ДНК. Общая длина участка ДНК, включенного в нуклеосому животных, составляет 200 (±15) п.о.
Полипептидные цепи гистонов содержат структурные домены нескольких типов. Центральный глобулярный домен и гибкие выступающие N- и С-концевые участки, обогащенные основными аминокислотами, получили название плеч (arm). С-концевые домены полипептидных цепей, участвующие в гистон–гистоновых взаимодействиях внутри к ó ровой частицы, находятся преимущественно в виде a-спирали с протяженным центральным спиральным участком, вдоль которого с двух сторон уложено по одной более короткой спирали. Все известные места обратимых посттрансляционных модификаций гистонов, происходящих на протяжении клеточного цикла или во время дифференцировки клеток, локализованы в гибких основных доменах их полипептидных цепей (табл. I.2). При этом N-концевые плечи гистонов H3 и H4 являются самыми консервативными участками молекул, а гистоны в целом – одними из наиболее эволюционно консервативных белков. С помощью генетических исследований дрожжей S. cerevisiaeбыло установлено, что небольшие делеции и точковые мутации в N-концевых частях генов гистонов сопровождаются глубокими и разнообразными изменениями фенотипа дрожжевых клеток. Это указывает на чрезвычайную важность целостности молекул гистонов в обеспечении правильного функционирования эукариотических генов.
В растворе гистоны Н3 и Н4 могут существовать в виде стабильных тетрамеров (Н3)2(Н4)2, а гистоны Н2А и Н2В – в виде стабильных димеров. Постепенное повышение ионной силы в растворах, содержащих нативный хроматин, приводит к освобождению сначала димеров Н2А/Н2В, а затем тетрамеров Н3/Н4.
Дальнейшее уточнение тонкой структуры нуклеосом в кристаллах было проведено недавно в работе К. Люгера с соавт. (1997 г.) с помощью рентгеноструктурного анализа высокого разрешения. Было установлено, что выпуклая поверхность каждого гистонового гетеродимера в составе октамера огибается сегментами ДНК длиной 27–28 п.о., расположенными по отношению друг к другу под углом 140о, которые разделены линкерными участками длиной в 4 п.о.
В соответствии с современными данными пространственная структура ДНК в составе к ó ровых частиц несколько отличается от B-формы: двойная спираль ДНК перекручена на 0,25–0,35 п.о./виток двойной спирали, что приводит к образованию шага спирали, равному 10,2 п.о./виток (у В-формы в растворе – 10,5 п.о./виток). Стабильность комплекса гистонов в составе к ó ровой частицы определяется взаимодействием их глобулярных частей, поэтому удаление гибких плеч в условиях мягкого протеолиза не сопровождается разрушением комплекса. N-концевые плечи гистонов, по-видимому, обеспечивают их взаимодействие со специфическими участками ДНК. Так, N-концевые домены гистона Н3 контактируют с участками ДНК на входе в к ó ровую частицу и выходе из нее, тогда как соответствующий домен гистона Н4 связывается с внутренней частью ДНК нуклеосомы.
Упомянутые выше исследования структуры нуклеосом высокого разрешения показывают, что центральная часть сегмента ДНК длиной в 121 п.о. в составе нуклеосомы образует дополнительные контакты с гистоном H3. При этом N-концевые части полипептидных цепей гистонов H3 и H2B проходят через каналы, образуемые малыми бороздками соседних супервитков ДНК нуклеосомы, а N-концевая часть гистона H2A контактирует с малой бороздкой внешней части супервитка ДНК. В совокупности данные высокого разрешения показывают, что ДНК в составе коровых частиц нуклеосом огибает гистоновые октамеры неравномерно. Кривизна нарушается в местах взаимодействия ДНК с поверхностью гистонов, и такие изломы наиболее заметны на расстоянии 10–15 и 40 п.о. от центра супервитка ДНК.
Таблица I.2