Вариант 14
| f (V) |
| V |
| dV |
| Vвер |
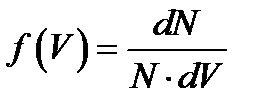 - доля молекул, скорости которых заключены в интервале от
- доля молекул, скорости которых заключены в интервале от 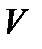 до
до 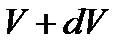 в расчете на единицу этого интервала.
в расчете на единицу этого интервала.
Если, не меняя температуры, взять другой газ с м еньше й молярной массой и таким же числом молекул, то…
1) величина максимума увеличится;
2 ) площадь под кривой уменьшится;
3) максимум кривой сместится вправо, в сторону больших скоростей.
4) площадь заштрихованной полоски уменьшится;
| Т |
| n |
14.2.На рисунке представлена зависимость концентрации идеального газа от температуры для трех процессов. Изохорический процесс соответствует участку …. Поясните свой ответ.
14.3. Какую массу углекислого газа можно нагреть при Р = const от температуры 20°Cдо температуры 100° С количеством теплоты Q = 222 Дж?
14.4. Кислород занимает объем V 1 = 1 м3 и находится под давлением Р 1 = 2×105 Па. Газ нагрет сначала при постоянном давлении до объема V 2 = 5 м3, а затем при постоянном объеме до давления Р2 = 3×105 Па.Найти количество сообщенной газу теплоты.
14.5. В результате нагревания m =22 г азота его абсолютная температура увеличилась в n =1,2 раза, а энтропия увеличилась на D S =4,19 Дж/К. При каких условиях производилось нагревание (при постоянном объеме или при постоянном давлении)?
ИДЗ «МКТ. Термодинамика»
Вариант 15
15.1.Укажите номера правильных утверждений о средней квадратичной скорости (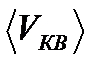 ) частиц системы, подчиняющейся распределению Максвелла. Поясните свой выбор.
) частиц системы, подчиняющейся распределению Максвелла. Поясните свой выбор.
1) При одинаковой температуре 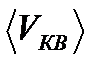 молекул различных идеальных газов одинакова.
молекул различных идеальных газов одинакова.
2) Средняя квадратичная скорость 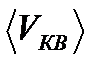 молекул газа при любой температуре меньше наиболее вероятной скорости.
молекул газа при любой температуре меньше наиболее вероятной скорости.
3) Чем больше масса молекулы газа, тем меньше 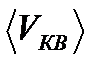 .
.
4) При возрастании температуры системы в четыре раза средняя квадратичная скорость 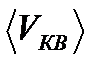 молекул увеличивается в два раза.
молекул увеличивается в два раза.
| Т |
| P |
| D |
| B |
| C |
| A |
1) в точке А 2) в точке В 3) в точке С 4)в точке D
15.3. Кислород занимает объем V 1 = 1 м3 и находится под давлением Р 1 = 2×105 Па. Газ нагрет сначала при постоянном давлении до объема V 2 = 5 м3, а затем при постоянном объеме до давления Р2 = 3×105 Па.
Найти работу совершенную газом.
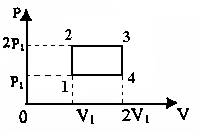
15.4. Кислород совершает круговой процесс, состоящий из двух изохор и двух изобар (см. рисунок). Отношение работы 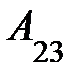 , совершенной газом на участке 2–3, к количеству теплоты
, совершенной газом на участке 2–3, к количеству теплоты 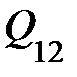 ,полученного газом на участке 1–2,
,полученного газом на участке 1–2,  равно …
равно …
1) 0,5 2) 0,8 3) 1,33 4) 2,5
15.5. Изменение энтропии при изохорическом охлаждении кислорода от 550 до 275 К составило ΔS = - 28,80 ·103 Дж/К. Сколько молей кислорода было использовано?
ИДЗ «МКТ. Термодинамика»
Вариант 16
16.1.В сосуде, разделенном на равные части неподвижной непроницаемой перегородкой, находится газ. Температуры газа в каждой части сосуда равны, но масса газа в левой части больше, чем в правой (М1 > М2 ). Функции распределения молекул газа по скоростям 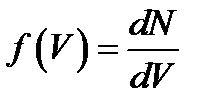 в разных частях сосуда будут описываться кривыми…
в разных частях сосуда будут описываться кривыми…
| V |
| f (V) |
| V |
| f (V) |
| V |
| f (V) |
| Т |
| V |
16.2.Идеальный газ совершает круговой процесс, как показано на рисунке. Давление газа максимально в состоянии …
16.3. Один моль азота, занимающего при давлении Р 1 = 105 Па объем V 1 = 10-2 м3, расширяется вдвое. Считая процесс изотермическим, найти работу, совершенную газом.
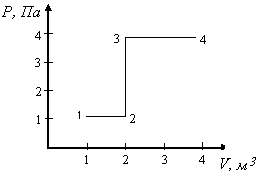
16.4.При переходе газа из состояния 1 в состояние 4 отношение количества теплоты  ,полученной двухатомным газом, к работе
,полученной двухатомным газом, к работе 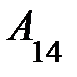 , совершенной газом в этом процессе,
, совершенной газом в этом процессе, 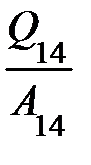 равно
равно
16.5. Кусок льда массой m = 0,2 кг, взятый при t 1 = –10 °C, был нагрет до температуры t 2 = 0 °C и расплавлен. Определить изменение энтропии ΔS в ходе указанных процессов, если удельная теплота плавления льда λ = 3,35×105 Дж/кг, удельная теплоемкость льда С УД = 2,1×103 Дж/(кг×К).