
Производные:
1) холестана или стерины: холестерин, эргостерин, витамин D2;
2) холана (желчные кислоты) – холевая и дезоксихолевая; гликохолевая и таурохолевая кислоты;
3) андростана (андрогенные вещества) – тестостерон, андростерон
4) эстрана (эстрогенные вещества)– эстрон, эстрадиол, эстриол;
прегнана (кортикостероиды)– дезоксикортикостерон, гидрокортизон, преднизолон
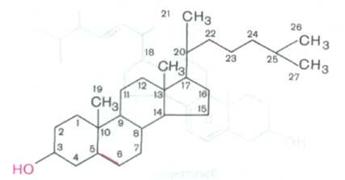
Для холестерола (т.е. стеринов) характерно наличие гидроксильной группы в положении 3, а также боковой цепи в положении 17. У холестерина все кольца находятся в транс–положении; кроме того, он имеет двойную связь между 5-м и 6-м углеродными атомами. Следовательно, холестерин является ненасыщенным спиртом:
Кольцевая структура холестерина отличается значительной жесткостью, тогда как баковая цепь- относительной подвижностью. Итак, холестерин содержит спиртовую гидроксильную группу при С-3 и разветвленную алифатическую цепь из 8 атомов углерода при С-17.
Химическое название холестерина 3-гидрокси-5,6-холестен или холестен 5-ол - 3β. Гидроксильная группа при С-3 может быть эстерифицирована высшей жирной кислотой, при этом образуются эфиры холестерина (холестериды).
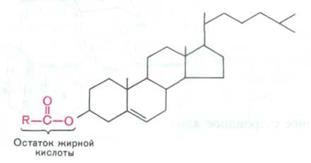
Эфир холестерина
Холестерол содержащится почти во всех тканях организма Его много в центральной и периферической нервной системе, подкожном жире, почках и др. Холестерол является одним из главных компонентов цитоплазматической мембраны, а также липопротеинов плазмы крови. В липопротеиновых фракциях крови примерно только одна треть его находится в виде спирта, а две трети – в форме эфиров жирных кислот (холестеридов).
Холестерол служит исходным предшественником для синтеза всех стероидов, функционирующих в организме – половых гормонов и гормонов коркового слоя надпочечников (кортикостероидов), желчных кислот, витамина D3
1. & Агликоны сердечных гликозидов: дигитоксигенин, строфантидин. Общий принцип строения сердечных гликозидов.
Гликозиды – представляют собой вещества, в которых гликозильная часть молекулы (циклическая форма сахаров) связана через атом кислорода, серы или азота с радикалом органического соединения, не являющегося сахаром Последний носит название агликона или генина. Вещество, которое действует на полуацетальный гидроксил моносахарида называется агликоном, а продукт реакции- гликозидом
По природе сахарной части молекулы гликозиды делят на две большие группы: пиранозиды (гликозиды с шестичленным циклом сахарного компонента) и фуранозиды (гликозиды с пятичленным циклом сахарного компонента). Агликон связан в молекуле гликозида с сахарным компонентом по типу эфирной связи через полуацетальный гидроксил.
Классификации гликозидов. С точки зрения химического строения гликозиды делят на три группы в зависимости от атома, связывающего сахар и агликон. Различают О-гликозиды, S-гликозиды (тиогликозиды) и N-гликозиды. Каждую из этих групп классифицируют по химической структуре агликона.
Стероидные гликозиды или сердечные гликозиды — это группа О-гликозидов растительного происхождения. Выделяют эти соединения из различных видов наперстянки (наперстянки: крупноцветковая, пурпуровая, ржавая, шерстистая) (дигиталиса)), ландыша, горицвета весеннего, олеандра, ландыша майского и другие растения.
В растениях обычно содержатся первичные (генуинные) гликозиды. Это очень лабильные вещества,. При гидролитическом расщеплении, а также при хранении и высушивании сырья под действиям энзимов первичные гликозиды разрушаются с образованием вторичных гликозидов и других продуктов гидролиза. Вторичные также могут легко гидролизоваться на агликоны и сахарный компонент. Например, первичные гликозиды наперстянки шерстистой под действием ферментов могут вначале терять только по одной молекуле глюкозы.
Из-за отсутствия легко ионизирующихся групп растворимость сердечных гликозидов не зависит от рН.
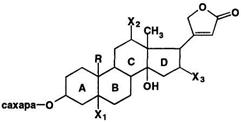
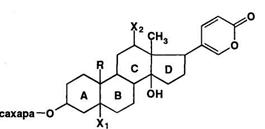
Агликоны сердечных гликозидов имеют стероидную струкутру, т.е. являются производными циклопентанпергидрофенантрена. Они представляют собой ненасыщенные стероидные лактоны (лактоны– образование сложных эфиров за счет взаимодействия между гидроксильной и карбоксильной группами одной и той же молекулы, т.е. внутримолекулярно).
По химическому строению агликоны можно разделить на две группы, отличающиеся структурой присоединенного в положении 17 лактонного цикла, который обычно занимает β-конфигурацию. Пятичленный лактонный цикл входит в структуру агликонов карденолидов, а шестичленный — буфадиенолидов.
| 
|
| карденолиды | буфадиенолиды |
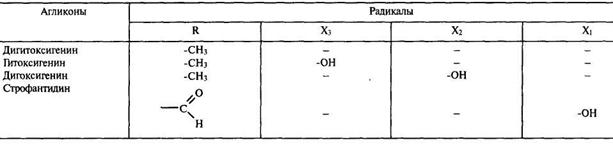
Радикал R — СНз или -СОН; a X1, Х2, Хз — Н или ОН.
В стероидной части молекулы могут также быть кето-, ацильные, эпоксигруппы, изолированные С=С связи.
В отличие от большинства других стероидов кольца С и D в карденолидах и буфадиенолидах имеют цис-сочленение, а кольца А и В могут иметь как цис-, так и транс-сочленени. Кольца В и С всегда имеют транс- сочленение.
Большинство сердечных гликозидов по химическому строению представляют собой карденолиды, которые отличаются друг от друга радикалами R, X1, Х2, Хз.
Радикалы агликонов сердечных гликозидов
. 
Молекула сердечного гликозида включает один, два или три остатка сахаров, соединенных в положении 3 с агликоном α- или β-гликозидной связью.
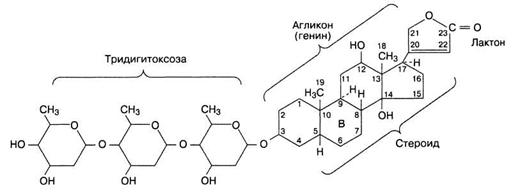
Структура типичного сердечного гликозида дигоксина (вторичный гликозид)
Дигоксин состоит из стероидного ядра с ненасыщенным пятичленным лактонным кольцом в 17-ом положении и сахаров, связанных с агликоном через углерод в 3-ем положении.
Между химической структурой и фармакологическим действием сердечных гликозидов существует определенная взаимосвязь. Носителем биологической активности является агликон. Сахарный компонент, присоединенный в положении 3 к агликону, влияет на скорость всасывания, а следовательно, на продолжительность действия. Чем больше остатков моносахаридов в молекуле гликозида, тем активнее он действует.
Специфическое действие гликозида на сердце (замедление частоты и усиление сердечных сокращений) обусловлено наличием в молекуле агликона пяти- или шестичленного лактонного цикла, присоединенного в положении 17, и гидроксила в положении 14. На кардиотоническое действие большое влияние оказывает заместитель в положении 10. Большая часть агликонов в этом положении имеет метильную или альдегидную группу. Окисление альдегидной группы до карбоксильной значительно ослабляет действие на сердечную мышцу. Замена стероидного цикла агликонов производными бензола, нафталина, так же как замена лактонного цикла другими радикалами и даже изменение характера связи между стероидным ядром и лактоном, приводит к потере фармакологической активности.
.