В нейтрализатор 1 (рис.1) мерным цилиндром наливают 200 мл азотнокислотной вытяжки. Рассчитанные количества растворов аммиака и фосфорной кислоты (карбоната калия, серной кислоты) наливают в капельные воронки (бюретки) 4 и 5. Водяную баню 2 заполняют холодной водой, включают магнитную мешалку 3 и начинают нейтрализацию вытяжки. Для этого из капельной воронки (бюретки) в течение 10–15 минут по каплям прибавляют раствор аммиака до достижения значения рН 2–3. Затем нейтрализацию продолжают при одновременной подаче аммиака и фосфорной кислоты (карбоната калия, или серной кислоты). В процессе опыта каждые 5 мин контролируют значение рН пульпы: скорость приливания растворов должна быть такой, чтобы каждые 10–15 мин значение рН пульпы повышалось на 0,5–1, а температура раствора не поднималась выше 40 °С (60 °С или 110 °С соответственно).
В случае резкого подъёма температуры необходимо приостановить прибавление растворов в нейтрализатор и снизить температуру пульпы интенсивным перемешиванием и добавлением холодной воды в водяную баню. После прибавления всего количества фосфорной кислоты (карбоната калия, или серной кислоты) величина рН достигает значения 5,5–6 и процесс завершают прибавлением оставшегося аммиака до достижения значения рН 7,5–8. При указанном режиме образуется маловязкая пульпа и предотвращается ее загустевание.
Основным условием нормального осуществления процесса карбонизации при получение нитрофоски карбонатным способом является соблюдение определенного изменения значения рН, равномерное поступление растворов аммиака и карбоната калия. Образующийся на первой стадии гидрофосфат кальция – CaHPO4 – выделяется в осадок и приводит к загустеванию пульпы. Загустевание наблюдается преимущественно в интервале значений рН от 2 до 2,7. Слишком быстрое возрастание величины рН способствует обильному образованию осадка и загустеванию массы настолько, что мешалка приостанавливается, и нормальный ход процесса нарушается. Получение подвижной пульпы обеспечивается при равномерной подаче растворов и интенсивном перемешивании. При этих условиях значение рН раствора в течение первых 60 мин изменяется примерно от 1 до 7,5, а затем в последующие 30 мин колеблется в пределах 7,5–8.
После прибавления всех растворов и достижения значения рН 7,5–8 перемешивание продолжают еще 10–15 мин, после чего останавливают магнитную мешалку и переносят пульпу в большую фарфоровую чашку. Туда же вносят определённое количество добавок – KCl и KNO3 – общей массой до 50 г (20 г, 20 г соответственно). После тщательного перемешивания массу упаривают на электроплитке до загустевания и помещают в сушильный шкаф, где продукт высушивают при температуре 50–60 °С примерно 4 часа. Высушенную нитрофоску измельчают в ступке, взвешивают, результат взвешивания заносят в табл. 2.
Обработка результатов
По уравнениям реакций (для своего варианта) теоретически рассчитывают количества образовавшихся продуктов:
а) фосфатным способом – CaHPO4, NH4H2PO4, NH4NO3;
б) карбонатным способом – CaHPO4, NH4H2PO4, NH4NO3, CaCO3, KNO3;
в) сульфатным способом – CaHPO4, NH4H2PO4, NH4NO3, CaSO4.
Полученные результаты расчетов заносят в табл. 2.
Содержание питательных веществ в нитрофоске в (%) рассчитывают по формулам:
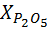 =
= 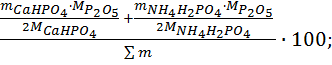 (8)
(8)
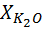 =
= 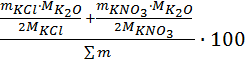 ; (9)
; (9)
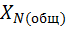 =
= 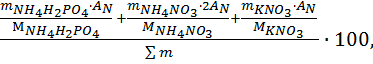 (10)
(10)
где 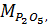
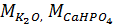 ,
, 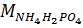 ,
, 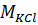 ,
, 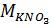 ,
, 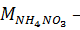 молекулярные массы компонентов системы, г/моль;
молекулярные массы компонентов системы, г/моль;
AN – атомная масса азота, г/моль;
Σm – масса нитрофоски, рассчитанная теоретически, как сумма масс отдельных компонентов, г.
Таблица 2
Расчет компонентного состава
| Компонент | Масса компонента m, г | Содержание, % | масса нитрофоски, г | |
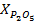
| 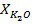
| 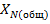
| ||
| продукты | ||||
| CaHPO4 | ||||
| NH4H2PO4 | ||||
| NH4NO3 | ||||
| KNO3 | ||||
| CaCO3 | ||||
| CaSO4 | ||||
| Добавки | ||||
| KCl | ||||
| KNO3 | ||||
| Всего Σm: |
Теоретически рассчитанное содержание питательных веществ в нитрофоске сравнивают с требуемым составом.
Определяют практический выход, делают выводы по работе.
2.2. Анализ нитрофоски [5, 6]
Полученный продукт – нитрофоску – анализируют на содержание влаги; усвояемого водо- и цитратнорастворимого, а также общего P2O5; аммонийного, нитратного и общего N; калия (в пересчете на K2O) и CaO.
Влагу в нитрофоске определяют гравиметрическим методом. Продукт сушат при температуре 100–105 ºС, при этом удаляется вся гигроскопическая влага и некоторое количество кристаллизационной.
Содержание калия в нитрофоске определяют осаждением его в виде тетрафенилбората с объёмным или весовым окончанием анализа. При отсутствии необходимых реактивов для осаждения в виде тетрафенилбората, калий можно определить кобальтинитритным методом, который также пригоден для количественного определения калия в нитрофоске.
Анализ на содержание CaO проводят по методике, описанной в лабораторной работе «Разложение фосфатов. Получение и анализ азотнокислотной вытяжки».
В настоящей работе определяют содержания нитратного азота оксидиметрическим (ускоренным) методом титрованием перманганатом калия и фосфатов фотоколориметрическим методом по желтому фосфорнованадиевомолибденовому комплексу.