Составьте конспект лекции по теме «Главная подгруппа 3 группы»
Выполненные задания присылать в личном сообщении ВК в виде фото или скринов (не перевернутые). Под своим именем.
Срок сдачи: до 09.10.2020г.
Обратите внимание: Не нужно переписывать лекцию дословно!!!!
Ваша задача: составить конспект таким, каким вам он будет понятен и доступен для изучения предложенной темы.
Тема: p – Элементы III группы
1. Общая характеристика элементов III -a группы.
Известно 30 р - элементов в периодической системе, это элементы, расположенные в III-A - VIII-A группах. У р - элементов заполняется электронами р- подуровень внешнего электронного уровня.
III-A группа – B, Al, Ga, In, Tl – характеризуются наличием 3-х электронов в наружном электронном слое атома, причем у бора на предвнешнем слое атома – 2 электрона, у алюминия – 8 электронов, Ga, In, Tl – 18 электронов. III группа самая элементоемкая – содержит 37 элементов, включая лантаноиды и актиноиды. Все элементы металлы, за исключением бора.
При переходе от Al к Ga радиус атома уменьшается. Это связано с тем, что у Ga заполнение р - подуровня начинается после того, как заполняется 3d10 электронная оболочка. Под действием 3d10 - электронов электронная оболочка всего атома сжимается и размер атома уменьшается (эффект d - сжатия).
Монотонного (последовательного) изменения металлических свойств не наблюдается. Металлические свойства резко усиливаются при переходе от бора к алюминию, несколько ослабевают у галлия, и вновь постепенно растут при переходе к таллию.
Температура кипения закономерно уменьшается от B к Tl. Температура плавления незакономерно из-за особенностей строения кристаллической решетки.
|
|
Самый легкоплавкий металл – Ga (Тпл = 29,8˚С).
В невозбужденном состоянии конфигурация внешнего уровня ns2np1, в возбужденном состоянии - ns1np2.
В невозбужденном состоянии имеется 1 неспаренный электрон, однако соединения большинства этих элементов, в которых их степень окисления +1, очень неустойчивы и наиболее характерна для них степень окисления +3 в возбужденном состоянии, т.к. на перевод электрона из s-состояния в р - надо немного энергии.
B – неметал, Al – еще не типичный металл, Ga, In, Tl –типичные металлы. Соединения: ЭН3, Э2О3, Э(ОН)3.
B2O3 кислотный оксид
Al2O3 амфотерный оксид
Ga2O3 амфотерный оксид (с преобладанием основных свойств)
In2O3 амфотерный оксид (с преобладанием основных свойств)
Tl2O (Tl2O3) основной оксид
H 3BO3 ортоборная кислота
Al(OH)3 амфотерный гидроксид
Ga(OH)3 амфотерный гидроксид
In(OH)3 амфотерный гидроксид
TlOH основной гидроксид
Бор. Получение. Химические свойства
Бор по своим свойствам наиболее схож с элементом IV-A группы кремнием («диагональное сходство»).
Бор – кристаллическое вещество, черного цвета, тугоплавкое при t = 2300 С.
Наиболее распространены две модификации бора: аморфный и кристаллический. Аморфная модификация наиболее реакционноспособна.
Получение бора
1. Термическое разложение гидридов бора:
B2H6 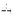 2B + 3H2
2B + 3H2
2. Магнийтермией из оксида бора:
B2O3 + 3Mg 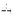 3MgO + 2B
3MgO + 2B
B2O3 + Zn 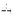 ZnO + B
ZnO + B
3. Из хлорида бора:
2BCl3 + 3Zn 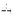 3ZnCl2 + 2B
3ZnCl2 + 2B
Непосредственно активно бор реагирует только со фтором, однако при нагревании протекает взаимодействие с кислородом, азотом, углеродом.
B + 2F2 → BF4
4B + 3O2 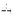 2B2O3
2B2O3
2B + N2 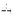 2BN
2BN
4B + 3C 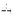 B4C3
B4C3
Бор реагирует с горячими концентрированными кислотами H2SО4 и HNO3
|
|
B + H2SO4конц. → H3BO3 + SO2↑ + H2O
B + HNO3конц. → H3BO3 + NO2↑ + H2O
Со щелочами реагирует только в присутствии сильных окислителей:
B + NaOH + H2O2 → NaBO2 + H2O
Однако аморфный бор может реагировать со щелочами при кипячении:
Bаморфн. + NaOH 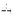 NaBO2 + H2↑
NaBO2 + H2↑
С водородом бор непосредственно не реагирует. Гидриды бора получают не прямым взаимодействием с водородом, а косвенным путем.
Например, действием соляной кислоты на борид магния.
Мg3В2 + 6HCl ® В2Н6 +3МgCl2
Получается смесь бороводородов (боранов). Бораны известны газообразные, жидкие и твердые.
В2Н6 – диборан – газ
В4Н10 – тетраборан – жидкость
В10Н14 – твердый боран.
Они имеют неприятный запах и очень ядовиты. Большинство из них самовоспламеняются и разлагаются водой.
Борные кислоты
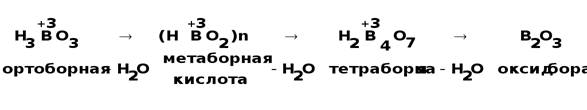
Все кислоты превращаются в ортоборную:
HBO2 + H2O → H3BO3
H2B4O7 + 5H2O → 4H3BO3
Если ортоборная наиболее устойчивая кислота, то соли ее не существуют в обычных условиях по сравнению с солями мета- и тетраборной кислот. Так при действии на раствор борной кислоты гидроксидом натрия получается не ортоборат, а тетраборат натрия (при недостатке NaOH) или метаборат (в избытке NaOH):
2NaOHнед + 4H3BO3 = Na2B4O7 + 7 H2O
NaOHизб + H3BO3 = NaBO2 + 2H2O
При избытке щелочи образующийся тетраборат натрия превращается в метаборат натрия:
Na2B4O7 + 2NaOHизб = 4NaBO2 + H2O
Кислотный гидролиз тетрабората натрия приводит к образованию ортоборной кислоты:
Na2B4O7 + 2HCl + 5 H2O = 2NaCl + 4 H3BO3
Алюминий
По содержанию в земной коре занимает первое место среди металлов и третье среди всех элементов, после кислорода и кремния.
Металлические свойства его выражены сильнее, чем у бора. Химические связи алюминия с другими металлами в основном ковалентного характера. Тип кристаллической структуры - ГПУ.
|
|
В отличие от бора атом алюминия имеет свободные d-подуровни на внешнем уровне. У Al3+ небольшой радиус и довольно высокий заряд, за счет чего он является комплексообразователем с координационным числом 4 или 6. Соединения Al более устойчивы, чем бора.
Получение алюминия
В промышленности Al получают электролизом расплава Al2O3 в криолите (Na3AlF6)
Al2O3 → Al+3 + AlO3-3
K (-) Al+3 + 3e = Al0
A (+) 2AlO3-3 – 6e = Al2O3 + 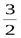 O2
O2