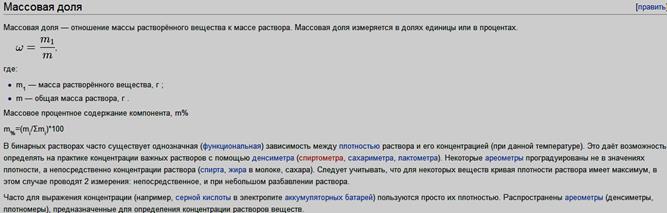
Раство́р — гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия. Раствор — однофазная система переменного состава, состоящая из двух или более компонентов. Растворы — гомогенные (однородные) системы, то есть каждый из компонентов распределён в массе другого в виде молекул, атомов или ионов[1].
Твёрдые, жидкие, газообразные растворы
Чаще под раствором подразумевается жидкое вещество, например раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама). Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше. В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким, твёрдым (твёрдый раствор), газообразным. Однако нередко допускается и микрогетерогенность Концентрированный раствор — раствор с высоким содержанием растворённого вещества в противоположность разбавленному раствору, содержащему малое количество растворённого вещества. Очевидно, что концентрированные растворы могут образовывать только хорошо растворимые вещества[источник не указан 83 дня]. Деление растворов на концентрированные и разбавленные не связано с делением на насыщенные и ненасыщеные. Так насыщенный 0,0000134М раствор хлорида серебра является очень разбавленным, а 4М раствор бромида калия, будучи очень концентрированным, не является насыщенным.
Виды концентрации и формулы.
Концентрация — величина, характеризующая количественный состав раствора.
Согласно правилам ИЮПАК, концентрацией растворённого вещества (не раствора) называют отношение количества растворённого вещества или его массы к объёму раствора (моль/л, г/л), то есть это отношение неоднородных величин. Те величины, которые являются отношением однотипных величин (отношение массы растворённого вещества к массе раствора, отношение объёма растворённого вещества к объёму раствора) правильно называть долями. Однако на практике для обоих видов выражения состава применяют термин концентрация и говорят о концентрации растворов.



Осмотическое давление.
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ, давление, производимое молекулами растворенного вещества на полупроницаемые стенки сосуда^ Теория О. д. Если чистая вода и какой-либо раствор разделены перегородкой, задерживающей растворённые молекулы, ю> пропускающей воду, то последняя начинает проходить через такую полупроницаемую мембрану. Если раствор находится в замкнутом сосуде, то вхождение воды внутрь (эндосмос) создает в таком сосуде повышенное давление, прекращающее дальнейшее проникновение воды. Это гидростатическое давление, уравновешивающее стремление воды проникать в раствор, называется осмотическим давлением раствора. Оно может быть измерено при помощи манометра, соединенного с внутренним сосудом (см. рисунок). Соответствующий прибор получил название осмометра. В качестве полупроницаемой мембраны осмометра Дютроше (Dutrochet) применял различные животные перепонки. Оказалось, что О. д. (p) численно равно давлению, которое оказало бы растворённое вещество, если бы оно при данной температуре находилось в состоянии идеального газа и занимало объём, равный объёму раствора. Для весьма разбавленных растворов недиссоциирующих веществ найденная закономерность с достаточной точностью описывается уравнением: πV = nRT, где n — число молей растворённого вещества в объёме раствора V; R — универсальная газовая постоянная; Т — абсолютная температура. В случае диссоциации вещества в растворе на ионы в правую часть уравнения вводится множитель i > 1, коэффициент Вант-Гоффа; при ассоциации растворённого вещества i < 1. О. д. реального раствора (π') всегда выше, чем идеального (π "), причём отношение π'/ π " = g, называемое осмотическим коэффициентом, увеличивается с ростом концентрации. Растворы с одинаковым О. д. называется изотоническими или изоосмотическими. Так, различные кровезаменители и физиологические растворы изотоничны относительно внутренних жидкостей организма. Если один раствор в сравнении с другим имеет более высокое О. д., его называют гипертоническим, а имеющий более низкое О. д. — гипотоническим.
О. д. измеряют с помощью специальных приборов — осмометров. Различают статические и динамические методы измерения. Первый метод основан на определении избыточного гидростатического давления по высоте столба жидкости Н в трубке осмометров (рис.) после установления осмотического равновесия при равенстве внешних давлений pA и рБ в камерах А и Б. Второй метод сводится к измерению скоростей v всасывания и выдавливания растворителя из осмотической ячейки при различных значениях избыточного давления Δp = pA — рБ с последующей интерполяцией полученных данных к ν = 0 при Δp = π. Многие осмометры позволяют использовать оба метода. Одна из главных трудностей в измерении О. д. — правильный подбор полупроницаемых мембран. Обычно применяют плёнки из целлофана, природных и синтетических полимеров, пористые керамические и стеклянные перегородки. Учение о методах и технике измерения О. д. называются осмометрией. Основное приложение осмометрии — определение молекулярной массы (М) полимеров. Значения М вычисляют из соотношения с — концентрация полимера по массе; А — коэффициент, зависящий от строения макромолекулы.
О. д. может достигать значительных величин. Например, 4%-ный раствор сахара при комнатной температуре имеет О. д. около 0,3 Мн/м2, а 53%-ный — около 10 Мн/м2; О. д. морской воды около 0,27 Мн/м2.
33. Растворы электролитов, диссоциация. Электролиты – вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Например, при растворении в воде уксусная кислота диссоциирует на ион водорода и ацетат-ион:
CH3COOH  H+ + CH3COO–
H+ + CH3COO–
Необходимым условием, определяющим возможность процесса электролитической диссоциации, является наличие в растворяемом веществе ионных * или полярных связей *, а также достаточная полярность * самого растворителя *. Количественная оценка процесса электролитической диссоциации дается двумя величинами: степенью диссоциации α и константой диссоциации K.
Степенью диссоциации (α) электролита называется отношение числа его молекул, распавшихся на ионы, к общему числу молекул электролита в растворе, т. е.  . Так, если C =0,1 моль/л, а концентрация диссоциированной части вещества С д=0,001 моль/л, то для растворенного вещества α=0,001/0,1=0,01, или α=1%. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением.
. Так, если C =0,1 моль/л, а концентрация диссоциированной части вещества С д=0,001 моль/л, то для растворенного вещества α=0,001/0,1=0,01, или α=1%. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением.
Электролиты можно разделить на две большие группы: сильные и слабые. Сильные электролиты диссоциируют практически полностью. К сильным электролитам относятся, например, H2SO4, HCl, HNO3, H3PO4, HClO3, HClO4, KOH, а также хорошо растворимые соли: NaCl, KBr, NH4NO3 и др. Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся плохо растворимые соли (см. таблицу растворимости), вода и большинство органических кислот (например, уксусная CH3COOH, муравьиная HCOOH), а также неорганические соединения: H2CO3, H2S, HCN, H2SiO3, H2SO3, HNO2, HClO, HCNO, NH4OH и др.
Константа равновесия для процесса диссоциации называется константой диссоциации (K). В общем случае для электролита, диссоциирующего на два иона:
АВ  А+ + В–
А+ + В–
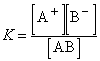
Для приведенного выше процесса диссоциации уксусной кислоты:
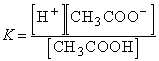
Если обозначить концентрацию электролита, распадающегося на два иона, через C, то
[A+] = [B–] = α C; [AB] = C(1–α);

Это уравнение соответствует закону разбавления Оствальда. Если электролит слабый, и диссоциация очень мала (α<<1), то закон разбавления Оствальда упрощается:
K =α2 C; 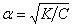 .
.
Таким образом, степень диссоциации возрастает с разбавлением раствора. Многоосновные кислоты, а также основания многовалентных металлов диссоциируют ступенчато. Например:
H2CO3  H+ + HCO3–
H+ + HCO3–
HCO3–  H+ + CO32–
H+ + CO32–
Первое равновесие – диссоциация по первой ступени – характеризуется константой

Для диссоциации по второй ступени:

В случае угольной кислоты константы диссоциации имеют следующие значения: K I = 4,3·10–7, K II = 5,6·10–11. Для ступенчатой диссоциации всегда K I> K II> K III>..., т.к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.
34. Химическая кинетика. Основные понятия и определения. Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений. Важным понятием химической кинетики является скорость химической реакции. Эта величина определяет, как изменяется концентрация компонентов реакции с течением времени. Скорость химической реакции — величина всегда положительная, поэтому если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то полученное значение домножается на −1.
Например для реакции
 скорость можно выразить так:
скорость можно выразить так:

Порядок реакции по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции. Молекулярность элементарной реакции — число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
35. Молекулярность и порядок химической реакции. Порядок химической реакции Порядок реакции по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции.