RH+O2=R-+HO2-
R-+O2=RO2-
RO2-+RH=ROOH+R-
Синтез с пероксидом водорода
(CH3CH2O)2O2+H2O2=CH3CH2COOH+H2SO4
RCl+H2O2=ROOH+HCl
Синтез с реактивами Гриньяра
RMgX+O2=ROOMgX
ROOMgX+H2O=ROOH+Mg(OH)X
Термолиз
ROOH=RO-+OH-
Тетрагидрофуран (тетраметиленоксид, фуранидин, оксолан) — химическое вещество, циклический простой эфир. Бесцветная легколетучая жидкость с характерным «эфирным» запахом. Важный апротонный растворитель. Широко применяется в органическом синтезе. Химическая формула: C4H8O
 Тетрагидрофуран производится промышленностью в количестве порядка десятков тысяч тонн в год несколькими способами. В наиболее распространённом методе используется катализируемая кислотой дегидратация 1,4-бутандиола. В другом методе производства проводят окисление n -бутана до малеинового ангидрида, который в дальнейшем подвергается каталитическому гидрогенированию. Третий промышленный способ заключается в гидроформилировании аллилового спирта с последующим восстановлением до бутандиола.
Тетрагидрофуран производится промышленностью в количестве порядка десятков тысяч тонн в год несколькими способами. В наиболее распространённом методе используется катализируемая кислотой дегидратация 1,4-бутандиола. В другом методе производства проводят окисление n -бутана до малеинового ангидрида, который в дальнейшем подвергается каталитическому гидрогенированию. Третий промышленный способ заключается в гидроформилировании аллилового спирта с последующим восстановлением до бутандиола.
Тетрагидрофуран также может быть синтезирован каталитическим гидрированием фурана, полученного из пентозы. Поскольку в этом методе используется возобновляемый ресурс (растительное сырье), этот метод находит всё более широкое применение. Используют как растворитель, например для поливинилхлорида, в лабораторной практике — вместо этилового эфира при получении магнийорганических соединений (в частности, винилмагнийбромида). Продукты гомо- и сополимеризации тетрагидрофурана — сырьё для получения уретановых каучуков. Из ТГФ синтезируют гамма-бутиролактон (по этой причине ТГФ включён в Таблицу III списка IV прекурсоров). Кроме того, используется как противокристаллизационная присадка к авиационным и ракетным топливам.
1,4-Диоксан — циклическое химическое соединение с формулой C4H8O2. Традиционно под диоксаном понимается 1,4-диоксан (диэтилендиоксид), циклический простой эфир, хотя существуют также 1,2-диоксан и 1,3-диоксан.
 Диоксан применяется в органической химии в качестве полярного апротонного растворителя. В основном используется как стабилизатор 1,1,1-трихлорэтана. Имеет сладковатый запах, схожий с запахом диэтилового эфира. Диоксан побочный продукт этоксилирования в производстве материалов для косметики, а именно натрий лаурил сульфата. По Proposition 65 в Калифорнии диоксан признан канцерогеном[2].
Диоксан применяется в органической химии в качестве полярного апротонного растворителя. В основном используется как стабилизатор 1,1,1-трихлорэтана. Имеет сладковатый запах, схожий с запахом диэтилового эфира. Диоксан побочный продукт этоксилирования в производстве материалов для косметики, а именно натрий лаурил сульфата. По Proposition 65 в Калифорнии диоксан признан канцерогеном[2].
1,4-Диоксан - бесцветная подвижная жидкость с эфирным запахом. Взрывопожароопасен. 1,4-Диоксан смешивается с водой, спиртом, эфиром; образует с водой азеотропную смесь

Диоксан используют как хороший растворитель, например для ацетилцеллюлозы, минеральных и растительных масел, красок.
Диоксан используется также как стабилизатор для 1,1,1-трихлорэтана для его хранения и транспортирования в алюминиевых ёмкостях.
11) Фенолы – органические соединения, содержащие 1 или несколько гидроксильных групп, связанных непосредственно с бензольным кольцом. Структура представителей: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол
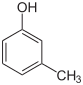 (пара, орто, мета)
(пара, орто, мета) 
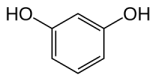
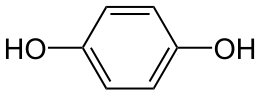

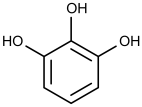

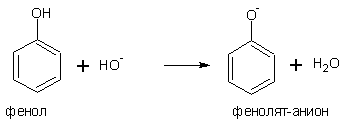
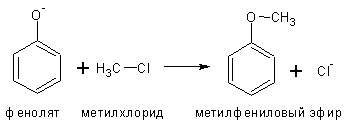
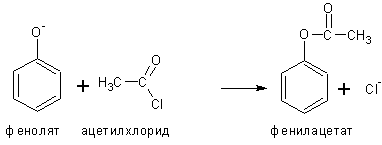
Фенолы превращаются в соли под действием водных растворов щелочей, но не водных растворов бикарбонатов.

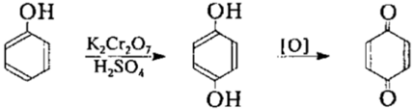
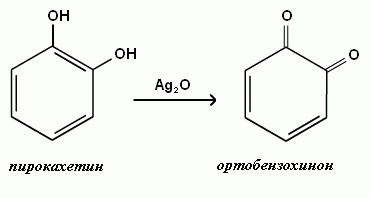
Хиноны — полностью сопряжённые циклогексадиеноны и их аннелированные аналоги. Существуют два класса хинонов: пара-хиноны с пара-расположением карбонильных групп (1,4-хиноны) и орто-хиноны с орто-расположением карбонильных групп (1,2-хиноны). Благодаря способности к обратимому восстановлению до двухатомных фенолов некоторые производные пара-хинонов участвуют в процессах биологического окисления в качестве коферментов ряда оксидоредуктаз.

Фенолы
Они встречаются в различных частях многих растений – в покровных тканях в плодах, проростках, листьях, цветках и
- придают им окраску и аромат пигменты фенольной природы - антоцианы;
большинство полифенолов –
- активные метаболиты клеточного обмена,
- играют важную роль в различных физиологических процессах, таких как, фотосинтез, дыхание, рост, устойчивость растений к инфекционным болезням, рост и репродукция;
- защищают растения от патогенных микроорганизмов и грибковых заболеваний.
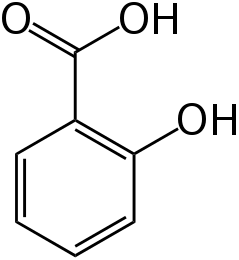
Из фенолокислот часто встречается галловая кислота и значительно реже - салициловая (фиалка трехцветная). Фенолокислоты и их гликозиды содержатся в родиоле розовой.
Флавоноиды играют важную роль в растительном метаболизме и очень широко распространены в высших растениях. Многие флавоноиды — пигменты, придающие разнообразную окраску растительным тканям. Так, антоцианы определяют красную, синюю, фиолетовую окраску цветов, а флавоны, флавонолы, ауроны, халконы — жёлтую и оранжевую. Они принимают участие в фотосинтезе, образовании лигнина и суберина, в качестве защитных агентов в патогенезе растений, вовлечены в регуляцию процессов прорастания семян, а также пролиферации и отмирания (путём апоптоза) клеток удлиняющихся растущих частей растений. Их многообразие объясняется тем, что в растениях большинство из них присутствует в виде соединений с сахарами — гликозидов. Сахарные остатки могут быть представлены моносахаридами — глюкозой, галактозой, ксилозой и др., а также различными ди-, три- и тетрасахаридами. К сахарным остаткам нередко присоединены молекулы оксикоричных и оксибензойных кислот.
Катехины и лейкоантоцианы бесцветны. Они являются родоначальниками конденсированных дубильных веществ.
ПРАКТИКА
19) 3,3,6-триметилпентан; 2,7-диметил-3-этилоктан
22)
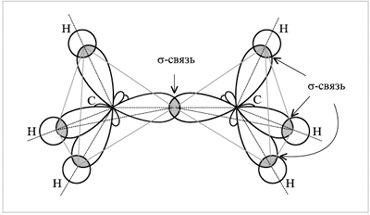
25)
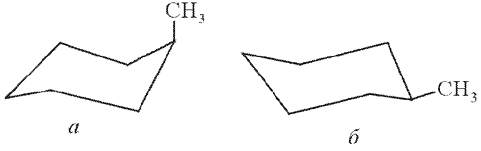
28)

31) CH2=CH-CH=CH2+Br2=CH2Br-CH=CH-CH2Br
CH2=CH-CH=CH2 + Br2 -- t=40 -->CH2Br-CHBr-CH=CH2
34) а) нафталин; б) фенантрен
37)
40) а) 2-метил-3-хлорбутан; б) 3,5-дихлорпентен-1; в)1,3-диметилбензол; г)1,2-диметибензол; д)метилбензол; е) 4-этилбромбензол; ж)2-этилфенол
43)
46) 2-метилбутан →2-метилбутен-2 →2-метил-2 хлорбутан
1)сн3-сн(сн3)-сн2-сн3->сн3-с(сн3)=сн-сн3
2) сн3-с(сн3)=сн-сн3 +HCl ---> H3C-CH2-C(Cl)(CH3)-CH3
Этилбензол 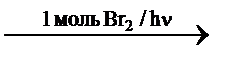 А
А 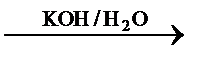 Б
Б
1) С6Н5-С2Н5 + Br2 -> C6H5-CHBr-CH3
2) C6H5-CHBr-CH3+KOH(водн)->C6H5CH(OH)-CH3
C2 Н2 
1)C2H2+H2O->CH3COH
2)CH3OH+Ag2O->CH3COOH+2Ag
3)CH3COOH+CH3OH->CH3COOCH3+H2O
4)CH3COOCH3+NaOH->CH3COONa+CH3OH

1)C6H6+CH3Br->C6H5CH3+HBr
2) C6H5CH3 + 2 KMnO4 = C6H5COOH + 2 MnO2 + 2 KOH
3) C6H5COOH+Cl2->
49) а) триолеин; б) олеопальмитостеарин
52)