Иодометрическое определение окислителей
Цель работы: определить иодометрическим методом:
– проба А – массу меди(II) или соли CuSO4 ∙ 5H2O в пробе (г);
– проба Б – массовую концентрацию «активного хлора» в водопроводной воде (мг Cl2/л).
Сущность работы. В иодометрии применяют растворы восстановителей Na2S2O3 и KI, но прямое титрование ими окислителей невозможно, поскольку реакции между окислителями и Na2S2O3 идут нестехиометрично, а между окислителями и KI – медленно. Кроме того, раствор KI неустойчив и нет возможности зафиксировать к. т. т. при титровании этим раствором.
Поэтому для определения окислителей используют титрование заместителя: окислитель замещают эквивалентным количеством
иода, затем титруют выделившийся йод раствором тиосульфата:

В качестве рабочего раствора используют стандартный раствор Na2S2O3, в качестве вспомогательных – растворы KI и Н2SO4. Специфический индикатор крахмал добавляют вблизи т. э.
Определение Cu2+ основано на взаимодействии ионов Cu2+ с иодид-ионами и последующем титровании выделившегося иода стандартным раствором тиосульфата натрия:
2Cu2+ + 4I– = I2 + 2CuI↓

Значение стандартного потенциала пары I2/2I– (0,54 В) заметно превышает соответствующее значение пары Cu2+/Cu+ (0,16 В), поэтому окисление иодида ионами меди(II) представляется нереальным. Однако на самом деле реакция между Cu2+ и I– протекает количественно. Это обусловлено образованием малорастворимого осадка CuI, что существенно повышает потенциал пары Cu2+/Cu+. Реакцию следует проводить в кислой среде для подавления гидролиза ионов меди(II).
Факторы эквивалентности веществ определяются на основании полуреакций:
Cu2+ + е – = Cu+ Þ f экв(Cu2+) = 1
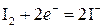 Þ f экв(I2) =
Þ f экв(I2) = 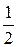
 Þ f экв(Na2S2O3) = 1
Þ f экв(Na2S2O3) = 1
Определение «активного хлора». Под термином «активный хлор» понимают суммарное содержание в воде свободного хлора Cl2, хлорноватистой кислоты НСlO, гипохлорит-ионов СlO– и хлораминов NH2Cl, NHCl2, NCl3.
При подкислении анализируемой воды и прибавлении к ней иодида калия все перечисленные вещества выделяют иод:
Сl2 + 2I– = I2 + 2Сl– (6)
СlO– + 2Н+ + 2I– = I2 + Сl– + Н2O
НСlO + 2I– + Н+ = I2 + Сl– + Н2O
NH2Cl + 2Н+ + 2I– = I2 + NH4+ + Cl–
Выделившийся иод оттитровывают тиосульфатом натрия в присутствии крахмала. Содержание «активного хлора» выражают в мг/л в пересчете на хлор.
Оборудование и реактивы: мерная колба, бюретка, пипетка Мора, мерные цилиндры (10–20 мл), коническая колба, часовые стекла.
Для анализа пробы А: стандартный 0,05 н. раствор Na2S2O3,
5%-ный раствор KI, 2 н. раствор H2SO4, раствор крахмала.
Для анализа пробы Б: стандартный 0,01 н. или 0,005 н. раствор Na2S2O3, KI (крист.), 30%-ный раствор CH3COOН, 0,5%-ный раствор крахмала, ацетатный буферный раствор с рН = 4,5.
Выполнение работы
Проба А. Cu2+ или соль CuSO4 × 5H2O. Получают у лаборантов анализируемый раствор в мерную колбу, доводят объем дистиллированной водой до метки и тщательно перемешивают. Переносят пипеткой аликвотную часть раствора в коническую колбу, добавляют цилиндром 3 мл 2 н. раствора H2SO4 и 10–15 мл раствора KI. Накрыв колбу часовым стеклом, оставляют смесь в темноте на 5 мин для завершения реакции. В ходе реакции образуется I2, придающий раствору бурую окраску, и осадок CuI цвета слоновой кости, за счет чего раствор в колбе будет мутным.
Выделившийся I2 начинают титровать тиосульфатом. Когда окраска раствора станет бледно-желтой, добавляют раствор крахмала до появления темно-синего окрашивания и продолжают титрование. В конечной точке титрования эта окраска исчезнет, в растворе останется только светлая муть (осадок CuI).
По полученным данным рассчитывают массу меди(II) или соли CuSO4 × 5H2O в пробе (г).
Проба Б. Определение «активного хлора». В коническую колбу, снабженную притертой стеклянной пробкой, наливают 50,00 или 100,00 мл анализируемой воды, вносят 0,5 г иодида калия и добавляют 10 мл уксусной кислоты. Через 5 мин оттитровывают выделившийся иод стандартным раствором тиосульфата натрия. В конце титрования прибавляют 1–2 мл раствора крахмала.
При содержании «активного хлора» выше 1 мг/л используют 0,01 н. Na2S2O3, а при содержании от 0,1 до 1 мг/л – 0,005 н. Na2S2O3.
По результатам титрования рассчитывают суммарную молярную концентрацию эквивалента хлорсодержащих соединений-окислителей в анализируемой воде:

Далее переходят к расчету массовой концентрации «активного хлора» в пересчете на хлор (мг Cl2/л):

Фактор эквивалентности Cl2 определяется по полуреакции

| & | М (Cu2+) = 63,546 г/моль М (CuSO4 × 5H2O) = 249,69 г/моль | М (Cl2) = 70,906 г/моль |
| & | Особенности методики определения «активного хлора» 1. Принятое выражение результатов анализа в пересчете на хлор (мг Cl2/л) условно, поскольку 1 моль НСlO, СlO–, NH2Cl выделяют по 1 моль I2, следовательно, соответствуют 1 моль «активного хлора» Cl2 в реакции (6). 2. В сточной воде могут содержаться и другие окислители, выделяющие I2 из KI (CrO42–, NO2–, Fe3+, СlO3– и др.). Хлораты не вступают в реакцию с KI при обычной температуре, если анализируемую воду подкисляют СН3СООН. При большом содержании NO2–, [Fe(CN)6]3–, Cu2+ или Fe3+ надо проводить титрование в среде ацетатного буфера с рН 4,5. Поправку на остальные окислители, которые встречаются в сточных водах реже (например, CrO42–), вводят, предварительно определив их другими методами. | |
| : | С использованием ПО «Практикум по АХ и ФХМА »: – оценить неопределенность измерений; – провести Q -тест и статистическую обработку результатов анализа, если имеется 4 и более результатов параллельных измерений. |

Комплексонометрическое титрование