Для анализа хлороформа в организме человека используют следующие биологические матрицы:
1)выдыхаемый воздух,альвеолярный воздух
2) кровь
3) моча
4) ткани (жировая ткань, сыворотка)
При подготовке образца выдыхаемого воздуха обычно используют адсорбент с последующей термической десорбцией или непосредственно проводят анализ аликвоты выдыхаемого воздуха. Анализ проводится с использованием метода газовой хроматографии.
Cardinali и др.(1994) описывает метод производства чистой воды для анализа органических соединений в крови человека в частях на триллион (ppt), наличие таких чистых образцов очень важно для получения точных результатов.
Анализ ткани печени является спорным для определения хлороформа, так как фосген, образующийся при воздействии на хлороформ цитохрома P-450, может быть получен при воздействии цитохрома P-450 на трибромхлорметан и четыреххлористый углерод. [10]
Качественный анализ
Большая часть современных методов определения хлорированных углеводородов, в частности хлороформа и дихлорэтана, основана на реакции Фудживара - окрашивании раствора пиридина, содержащего определяемое вещество в щелочной среде. По этой реакции образуется соль пиридиния, а под влиянием щелочи она превращается в производное глутаконового альдегида, при гидролизе которого образуется глутаконовый альдегид, имеющий окраску.[11]
Качественное определение хлороформа осуществляется с помощью ряда реакций.
Реакция отщепления галоида.
Эта реакция является общей реакцией на галогенпроизводные.

Отщепление галоида достигается нагреванием части дистиллята со спиртовым раствором едкой щелочи. Хлорид-ион обнаруживается реакцией с раствором нитрата серебра в азотнокислой среде. Образование мути или осадка говорит о наличии галогенпроизводных и необходимости проведения других реакций их обнаружения. Реакция не специфична.
2. Реакция образования изонитрила.
В случае отсутствия осадка или мути в реакции №1, учитывая ее сравнительно невысокую чувствительность, нужно проделать реакцию получения изонитрила.
CHCl3+3NaOH(спирт. р-р)+C6H5NH2 = C6H5N=C+3NaCl+3H2O
Отрицательный результат этой сравнительно чувствительной реакции (0,01 мг) позволяет судить о ненахождении в исследуемом объекте этих веществ. При положительном результате проводят другие реакции.
Реакция не специфична, ее дают все хлорпроизводные, за исключением дихлорэтана.
3. Реакция с резорцином в щелочной среде.

Появление розового или красного окрашивания в исследуемой пробе может указывать на наличие хлороформа. Параллельно выполняется «слепой» опыт, цель которого исключить ошибки за счет продуктов окисления резорцина, окрашенных в зеленый цвет и маскирующих розовое окрашивание.
Реакция не специфична, ее дают все хлорпроизводные, кроме дихлорэтана, а также формальдегид.
4. Реакция с реактивом Фелинга.
При значительных количествах хлороформа проводят реакцию восстановления Cu(OH)2 в Cu2(OH)2, переходящую далее в Cu2O при кипячении с реактивом Фелинга. При наличии хлороформа образуется желтый осадок гидрата закиси меди, переходящий в красный осадок закиси меди.
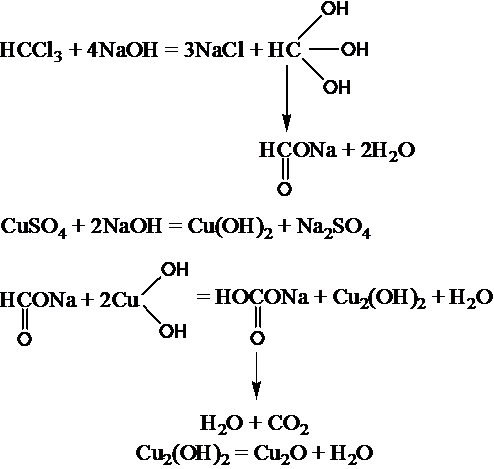
Реакция не специфична, ее дает хлороформ, хлоралгидрат и формальдегид. Не дают четыреххлористый углерод и дихлорэтан.
5. Реакция Фудживара.
Реакция взаимодействия с пиридином в присутствии щелочи. На этой реакции основано предварительное обнаружение галогенпроизводных в моче.

О наличии хлороформа судят по появлению красной окраски. Реакция не специфична, ее дают все хлорпроизводные.[11]