Спектр люминесценции кристаллов, активированных ионами хрома, существенно меняется от матрицы к матрице в зависимости от силы кристаллического поля. В кристаллах с сильным полем люминесценция обусловлена двукратно запрещенным переходом 2Е – 4А2, спектр люминесценции представляет собой узкие слабые линии, в кристаллах со слабым полем люминесценция связана с однократно запрещенным 4Т2 – 4А2, спектр излучения представляет собой широкую мощную электронно-колебательную полосу. В кристаллах со средним значением силы поля спектр излучения есть суперпозиция переходов 2Е – 4А2 и 4Т2 – 4А2. Лишь в кристаллах со средним и слабым кристаллическим полем ионы хрома демонстрируют свои выдающиеся донорные и генерационные способности. Поиск таких матриц до настоящего времени является нетривиальной задачей.
Поэтому результаты исследований люминесцентных свойств ионов хрома в гранатах обращают на себя внимание, а стереоатомный анализ их структуры и выявление связи спектральных свойств с характеристиками полиэдров Вороного-Дирихле наиболее удобными для отработки модели.
Замены ртутного разряда на Xe-разряд, обусловленна техническими, экологическими и другими причинами. Однако простая замена ртутного разряда на ксеноновый разряд невозможна, так как спектры возбуждения люминофоров, разработанных для ртутного разряда не согласуются со спектром излучения Хе-разряда, максимум полосы излучения которого приходится на 170 нм, что значительно короче длины волны ртутного разряда l = 254 нм. Это обстоятельство выдвигает более жесткие требования к люминофорам для ламп с Хе-разрядом, так как прямое преобразование одного кванта света с длиной волны 170 нм в квант видимого излучения с l » 510 нм энергетически не эффективно. Эта проблема может быть решена при реализации каскадной люминесценции.
Для наблюдения каскадной люминесценции необходимо соблюдение некоторых условий; в частности, для иона Pr3+ 1So – уровень должен быть расположен ниже дна 5d-зоны. Так как радиальное распределение 5d-орбиталей выходит за рамки 5s26р6-оболочек, в результате чего положение 5d-уровней весьма чувствительно к кристаллическому полю, т.е. к химической природе лигандов и их координации вокруг иона Pr3+. Данная глава посвящена выявлению закономерностей влияния химической природы лигандов и их координации вокруг иона Pr3+ на формирование спектров люминесценции.
4. Влияние структурных особенностей кристаллических гранатов, карунда и шпинели на величину энергетического зазора ΔЕ13 между возбужденными состояниями 4Т2 и 2Е ионов Cr3+
Из многочисленных диэлектрических материалов, используемых для возбуждения генерации СИ, соединения со структурой граната (пространственная группа О10h – Ia 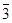 d) занимают особое место – они являются самыми применяемыми в квантовой электронике [4, 5]. Спектрально-генерационные исследования этих кристаллов с общей формулой A3BI2BII3O12 были начаты в середине 60-х годов [4]. К настоящему времени перечень лазерных матриц с этой структурой уже насчитывает более тридцати наименований, генерирующими активаторами в которых служат как Ln3+ -ионы (Nd3+, Dy3+, Ho3+, Er3+, Tm3+, Yb3+), так и ионы группы железа (Cr3+, Ti3+, Ni2+).
d) занимают особое место – они являются самыми применяемыми в квантовой электронике [4, 5]. Спектрально-генерационные исследования этих кристаллов с общей формулой A3BI2BII3O12 были начаты в середине 60-х годов [4]. К настоящему времени перечень лазерных матриц с этой структурой уже насчитывает более тридцати наименований, генерирующими активаторами в которых служат как Ln3+ -ионы (Nd3+, Dy3+, Ho3+, Er3+, Tm3+, Yb3+), так и ионы группы железа (Cr3+, Ti3+, Ni2+).
Как известно [6], в элементарную ячейку соединений структурного типа граната входят восемь формульных единиц (всего 160 атомов). Для удобства формулу гранатов можно записать как {A3}[BI2](BII3)O12, где фигурными, квадратными и круглыми скобками выделены катионы, занимающие с -, а - и d -кристаллографические позиции соответственно. BI-атомы занимают 16 октаэдрических а -положений (С3i), BII- атомы – 24 тетраэдрических d -положения (S4); а -узлы образуют объёмно-центрированную кубическую решётку, 24 А-иона находятся в додекаэдрических (D2) с -позициях. Структура иттрий-алюминиевого граната (ИАГ) приведена на рис. 4.1. Наиболее компактными в ИАГ являются тетраэдрические позиции с расстоянием до анионов 1,75 Å, для октаэдра это расстояние – 1,94 Å, для додекаэдра – 2,37 Å. Ионы кислорода расположены в 96 общих h -кристаллографических позициях. Додекаэдр имеет общие рёбра (связь О-О) с двумя тетраэдрами, четырьмя октаэдрами и четырьмя другими додекаэдрами. Координационные полиэдры несколько искажены: октаэдры – вдоль оси 3, а тетраэдры – вдоль оси 4; 8 анионов в додекаэдре двумя группами по 4 аниона расположены от а -узла на разных расстояниях. В элементарной ячейке имеется 8 неэквивалентных октаэдрических, 6 тетраэдрических и 6 додекаэдрических позиций [7, 8].
Рис. 4.1. Кристаллическая структура гранатов
Рентгеноструктурные и кристаллохимические исследования [9-17] свидетельствуют о том, что возможно существование чрезвычайно обширного ряда соединений со структурой граната, в которых а -, с - и d - положения могут занимать ионы различной валентности большого числа элементов (практически всех групп таблицы Менделеева). Причём некоторые из них, проявляя исключительную избирательность, могут заполнять полностью эти кристаллографические позиции, т.е. образовывать в трёхподрешёточной структуре граната свою подрешётку, которая определённым образом может оказывать влияние на катионы (например, на орбитальные моменты их валентных электронов) двух других подрешёток.
Изучение условий возбуждения стимулированного излучения (СИ) в кристаллах, активированными ионами Cr3+, необходимо при создании материалов для получения СИ, перестраиваемого в широкой области ИК-диапазона. Поскольку эти результаты хорошо освещены в литературе (см., например, [4, 18]), здесь будут приведены лишь некоторые важные для кристаллохимического рассмотрения выводы этих исследований.
Известно, что сила кристаллического поля уменьшается с увеличением расстояния Cr3+ – лиганд и уменьшением заряда лиганда. В галогенидах она, например, меньше, чем в оксидных соединениях, поэтому предлагалось использовать активированные Cr3+ кристаллы фторидов. Такой лазер был создан, например, на основе кристалла KZnF3:Cr3+. Весьма плодотворным оказался другой путь – поиск оксидных кристаллов с максимальным расстоянием Ме-О в октаэдрах, в которые при активации входят ионы Cr3+, с целью уменьшения величины кристаллического поля. (Уменьшения силы поля можно достичь также в гетеродесмических кристаллических оксидах с низким эффективным зарядом кислорода. Так, в кристаллических силикатах эффективный заряд кислорода -1,1).
Расстояние Ме-О в гранатах возрастает с увеличением а0. Исследования редкоземельных алюминиевых, галлиевых и других гранатов [4] позволили получить набор кристаллов с ионами Cr3+, в которых энергетический зазор между состояниями 2Е и 4Т2 (рис. 4.2) ионов Cr3+ (он характеризует силу кристаллического поля) уменьшается от ~1300 см-1 для ИАГ (Y3Al5O12) приблизительно до нуля для Gd3(Sc,Ga)5O12 и CaMg2Y2Ge3O12 [19].
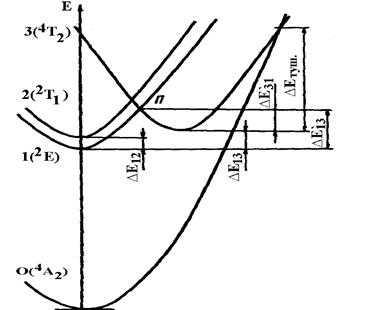
Рис. 4.2. Фрагмент схемы нижних энергетических уровней примесного иона Cr3+
Гадолиний скандий галлиевый гранат имеет большой параметр а0=12,57 Å и в силу этого высокий коэффициент распределения Кр для Ln3+-ионов и, в частности, для Nd3+. Для ионов Cr3+ в этом кристалле Кр ≈1. Теплофизические свойства Gd3(Sc,Ga)5O12 несколько хуже, чем для Y3Al5O12 (теплопроводность в гранатах обычно падает с увеличением атомной массы катионов), однако они являются вполне удовлетворительными [19].
Авторы работ [19] провели исследование спектрально-люминесцентных и кинетических характеристик синтезированных кристаллов галлиевых гранатов с примесью ионов Cr3+ и установили, что спектральные свойства и донорные возможности ионов Cr3+ определяются в значительной степени величиной энергетического зазора ∆Е между возбужденными состояниями 4Т2 и 2Е (рис. 4.2), которая, в свою очередь, зависит от симметрии и силы кристаллического поля, в котором находятся ионы Cr3+ , т.е. от геометрии окружения и расстояния до ближайших анионов.
Вследствие этого желаемое взаимное расположение уровней 4Т2 и 2Е в принципе может быть достигнуто подбором катионов основы в пределах данной структуры. Малая величина ∆Е, сравнимая (или меньше) с kТ при
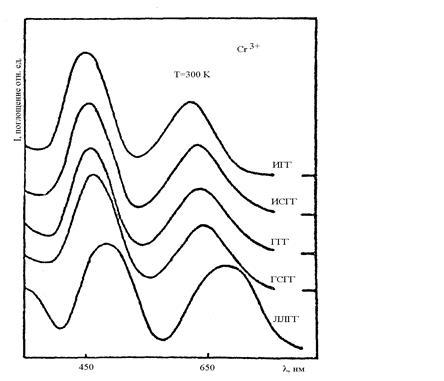
Рис. 4.3. Положение линий поглощения ионов хрома при Т=300 К
в кристаллах ИГГ (Y3Ga5O12), ИСГГ (Y3Sc2Ga3O12), ГГГ (Gd3Ga5O12), ГСГГ (Gd3Sc2Ga3O12) и ЛЛГГ (La2.55Lu2.45Ga2.96O11.93)
комнатной температуре, приводит к высокой населенности уровня 4Т2, что, в свою очередь, обуславливает наличие у ионов Cr3+ широкополосной люминесценции, связанной с переходом 4Т2 → 2Е, и высокую эффективность передачи энергии на соответствующие акцепторы благодаря активному участию в процессе передачи уровня 4Т2.
На рис. 4.3 представлены спектры поглощения, а на рис. 4.4 – люминесценции ионов Cr3+ в синтезированных кристаллах галлиевых гранатов [19], а на рис. 4.5 спектр люминесценции YAG:Cr3+. Широкие полосы поглощения связаны, как известно, с переходами 4А2 → 4Т2 или 2Т1, а люминесценция – с электронно-колебательным переходом 4Т2 →4А2.
В кристаллах ГГГ:Cr3+ так же, как и в ГСГГ:Cr3+, соотношение интенсивностей полос 4Т2 → 4А2 и 2Е → 4А2 зависит от концентрации ионов Cr3+. Как видно из зависимостей на рис. 5.6, с увеличением содержания хрома
относительная интенсивность R-линий падает. Однако кинетика распада возбужденного состояния хрома при этом не меняется [19].
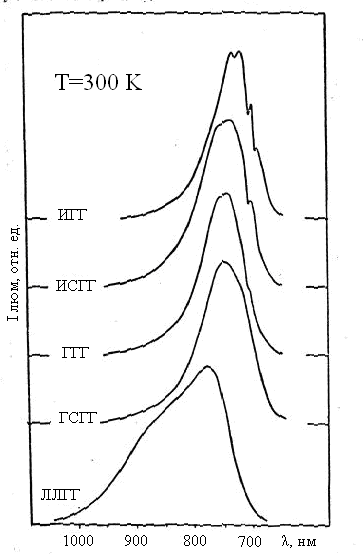
Рис. 4.4. Спектры люминесценции ионов хрома в кристаллах ИГГ, ИСГГ, ГГГ, ГСГГ и ЛЛГГ при Т=300 К

Рис. 4.5. Спектр люминесценции YAG:Cr3+ [7]
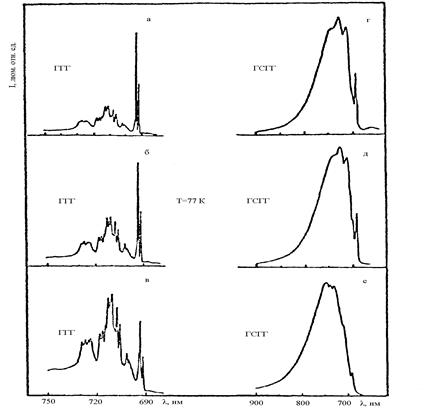
Рис. 4.6. Зависимость соотношения интенсивностей R-линий и широкой полосы люминесценции от концентрации ионов хрома в кристаллах ГГГ /содержание хрома 2·1019, 2,4·1020, 8·1020 см -3 – а, б, в/ и кристаллах ГСГГ /содержание хрома 6·1018, 6·1019, 3·1020 см-3 –г, д, е/ при Т=77К
Обращает на себя внимание изучение возможностей метода стереоатомного анализа для прогнозирования люминесцентных свойств ионов хрома в кристаллах. C целью построения модели и выявления зависимости ширины энергетического зазора ΔЕ13 от структурных особенностей окружения положения, замещаемого хромом, методами стереоатомного анализа изучим некоторые соединения со структурой граната: Gd3Ga5O12, Y3Ga5O12, (Y2.96Sc0.04)(Sc1.41Ga0.59)Ga3O12, La2.55Lu2.45Ga2.96O11.93, Gd3Sc2Ga3O12, Y3Al2(AlO4)3, Y3Sc2Al3O12, Gd3Sc2Ga3O12, Y3Ga2Al3O12, Sr3Y2(GeO4)3, Mg3Y2Ge3O12.
Структура соединений Gd3Ga5O12, Y3Ga5O12, (Y2.96Sc0.04)(Sc1.41Ga0.59)Ga3O12, La2.55Lu2.45Ga2.96O11.93, Gd3Sc2Ga3O12, изучена авторами работ [194-198]. Как и все гранаты, они относятся к кубической сингонии с пространственной группе Ia 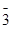 d, параметр элементарной ячейки a принимает значения 12.3770 Ǻ, 12.2730 Ǻ, 12.4250 Ǻ, 12.9810 Ǻ, 12.5440 Ǻ соответственно. Например, в элементарной ячейке содержится 8 формульных единиц Gd3Ga5O12, положение каждого из трех положительных ионов связано с различными координационными многогранниками. Ион Gd3+ окружен восемью ионами кислорода, образующими двенадцатигранник – деформированный куб. Ион Ga3+ (C3i) окружен кислородным октаэдром, а ион Ga3+ (S4) -тетраэдром. Позицию A3 занимает Gd1, позицию BI2 – Ga1, позицию BII3 – Ga2. Данные рентгеноструктурного анализа, в частности для Gd3Ga5O12, приведены в таблице 4.1.
d, параметр элементарной ячейки a принимает значения 12.3770 Ǻ, 12.2730 Ǻ, 12.4250 Ǻ, 12.9810 Ǻ, 12.5440 Ǻ соответственно. Например, в элементарной ячейке содержится 8 формульных единиц Gd3Ga5O12, положение каждого из трех положительных ионов связано с различными координационными многогранниками. Ион Gd3+ окружен восемью ионами кислорода, образующими двенадцатигранник – деформированный куб. Ион Ga3+ (C3i) окружен кислородным октаэдром, а ион Ga3+ (S4) -тетраэдром. Позицию A3 занимает Gd1, позицию BI2 – Ga1, позицию BII3 – Ga2. Данные рентгеноструктурного анализа, в частности для Gd3Ga5O12, приведены в таблице 4.1.
Таблица 4.1. Данные рентгеноструктурного анализа для Gd3Ga5O12
| Name | No | DegOx | Wyckoff | X | Y | Z | S | CN |
| Ga | C3i | 0.00000 | 0.00000 | 0.00000 | 1.000 | |||
| Ga | S4 | 0.37500 | 0.00000 | 0.25000 | 1.000 | |||
| Gd | D2 | 0.12500 | 0.00000 | 0.25000 | 1.000 | |||
| O | -2 | C1 | 0.02840 | 0.05490 | 0.64970 | 1.000 |
Как было замечено выше, при активировании граната ионами хрома, ион Cr3+ располагается в позиции ВI2, в рассматриваемом гранате данную позицию занимает атом Ga1. Рассчитаем стереоатомные характеристики окружения этого атома и атомов, замещаемых хромом в других соединений с помощью программы Dirichlet комплекса Topos, используя структурные данные работ [20-24]. Результаты расчетов для Gd3Ga5O12, Y3Ga5O12, (Y2.96Sc0.04)(Sc1.41Ga0.59)Ga3O12, La2.55Lu2.45Ga2.96O11.93, Gd3Sc2Ga3O12 приведены в таблице 4.2.
Таблица 4.2. Стереоатомные характеристики соединений со структурой граната.
| Соединение | X | SC | КЧ | VПВД, Å3 | Rsd, Å | G3 | Dist. Å |
| Gd3Ga5O12 | Ga1 | C3i | 8.086 | 1.245 | 0.083876446 | 2.000 | |
| Y3Ga5O12 | Ga1 | C3i | 7.868 | 1.234 | 0.084056683 | 1.980 | |
| (Y2.96Sc0.04)(Sc1.41Ga0.59)Ga3O12 | Ga1 | C3i | 9.008 | 1.291 | 0.084154844 | 2.070 | |
| La2.55Lu2.45Ga2.96O11.93 | Lu1 | C3i | 10.773 | 1.370 | 0.083791412 | 2.202 | |
| Gd3Sc2Ga3O12 | Sc1 | C3i | 9.224 | 1.301 | 0.083968468 | 2.089 |
Порученные данные показывают, что для исследуемых соединений с увеличением расстояния (Dist.) BI2 – О синхронно увеличиваются радиус сферического домена и объем полиэдра Вороного-Дирихле, что объясняется кубической симметрией кристаллов со структурой граната.
Рассмотрев структурные особенности соединений Gd3Ga5O12, (Y2.96Sc0.04)(Sc1.41Ga0.59)Ga3O12, Y3Ga5O12, La2.55Lu2.45Ga2.96O11.93, Gd3Sc2Ga3O12, найдем связь между величиной энергетического зазора ∆Е13 и объемом полиэдров Вороного-Дирихле (VПВД), сравнивая результаты измерений автора работы [25] с данными стереоатомного анализа (таблица 4.2). В таблице 4.3 приведены данные о величине энергетического зазора ∆Е13 для иона Cr3+ в исследуемых матрицах и объеме полиэдров Вороного-Дирихле замещаемых атомов.
Таблица 4.3. Значения энергетического зазора и объема полиэдров ВД.
| Гранат | ∆Е13, см-1 | VПВД, Å3 |
| LLGG | -1000 | 10.773 |
| GSGG (Sc2) | 9.224 | |
| YSGG | 9.008 | |
| GGG | 8.086 | |
| YGG | 7.868 |
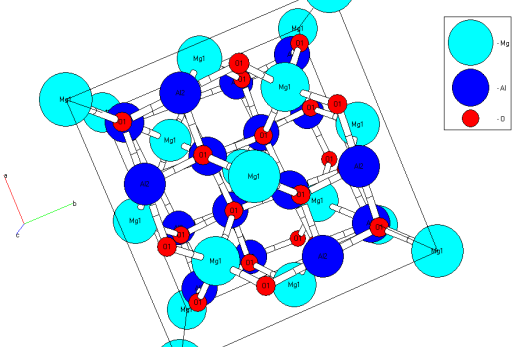
Рис. 4.7. Кристаллическая структура Mg Al2O4
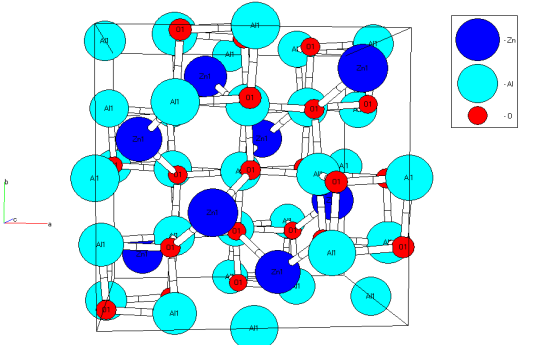
Рис. 4.8. Кристаллическая структура ZnAl2O4
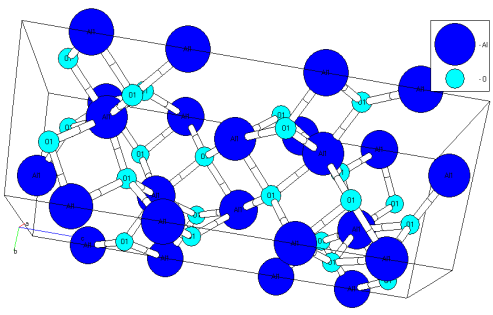
Рис. 4.9. Кристаллическая структура Al2O3
На рис. 4.10 показан график зависимости ∆Е13 от VПВД, построенный по данным таблицы 4.3. Данные, которые приведены на рис. 4.10, с достаточной точностью аппроксимируются линией тренда у=-534.55х+4892.6 (см-1), т.е. можно считать, что величина энергетического зазора ∆Е13 для иона Cr3+ в исследуемых матрицах линейно зависит от объема полиэдров Вороного-Дирихле замещаемых атомов. Поэтому, зная значение VПВД замещаемого атома в любом соединения со структурой граната, можно прогнозировать величину энергетического зазора ∆Е13 для иона Cr3+.
Оценим величину энергетического зазора ∆Е13 иона Cr3+ для некоторых других кристаллов со структурой граната. По аналогии с предыдущими расчетами, используя данные рентгеноструктурного анализа
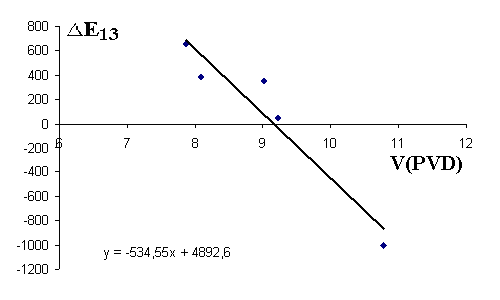
Рис. 4.10. График зависимости ∆Е13 иона Cr3+ в соединениях со структурой граната от VПВД замещаемых атомов.
базы данных [26], вычислим VПВД для Y3Al2(AlO4)3, Y3Sc2Al3O12, Gd3Sc2Ga3O12, Y3Ga2Al3O12, Sr3Y2(GeO4)3, и Mg3Y2Ge3O12. Значения VПВД приведены в таблице 5.4.
Таблица 4.4. Значения VПВД гранатов для элемента, находящегося в позиции ВI2
| Соединение | Элемент | VПВД, Å3 | |
| 1. | Y3Al2(AlO4)3 | Al1 | 8.228 |
| 2. | Y3Sc2Al3O12 | Sc1 | 8.973 |
| 3. | Gd3Sc2Ga3O12 | Sc2 | 9.224 |
| 4. | Y3Ga2Al3O12 | Ga2 | 9.446 |
| 5. | Sr3Y2(GeO4)3 | Y1 | 11.382 |
| 6. | Mg3Y2Ge3O12 | Y1 | 11.568 |
Используя значения VПВД, рассчитаем величину энергетического зазора ∆Е13 для иона Cr3+ для вышеприведенных соединений со структурой граната. Подставляя в уравнение у=-534.55х+4892.6 значения х=VПВД, находим прогнозируемую величину энергетического зазора (таблица 5.5).
Данные, приведенные в таблице, показывают, что гранат Y3Al2(AlO4)3 с VПВД=8.228 Å3 имеет самое большое положительное значение энергетического зазора – 508.2 см-1, а гранат Y3Sc2Al3O12 с VПВД= 8.973Å3 имеет самое маленькое положительное значение ∆Е13=103.9 см-1.
Таблица 4.5. Значения объема ПВД и прогнозируемого энергетического зазора ∆Е13.
| Соединение | Элемент | VПВД, Å3 | ∆Е13, см-1 | |
| 1. | Mg3Y2Ge3O12 | Y1 | 11.568 | -1304,3 |
| 2. | Sr3Y2(GeO4)3 | Y1 | 11.382 | -1203,4 |
| 3. | Y3Ga2Al3O12 | Ga2 | 9.446 | -152,7 |
| 4. | Gd3Sc2Ga3O12 | Sc2 | 9.224 | -32,2 |
| 5. | Y3Sc2Al3O12 | Sc1 | 8.973 | 103,9 |
| 6. | Y3Al2(AlO4)3 | Al1 | 8.228 | 508,2 |
| 7. | Al2O3 | Al | 7.177 | 1056.1 |
| 8. | Mg Al2O4 | Mg | 7.246 | 1019.2 |
| 9. | ZnAl2O4 | Zn | 7.158 | 1066.3 |
С помощью прикладных программ программного комплекса TOPOS установлено что структура карунда (Al2O3) принадлежит к пространственной решетке 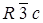 , параметры ячейки у которой 4.7540. Структура шпинели (Mg Al2O4) принадлежит к пространственной решетке F
, параметры ячейки у которой 4.7540. Структура шпинели (Mg Al2O4) принадлежит к пространственной решетке F 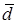 m, параметр ячейки у которой 8.0830. Структура шпинели (ZnAl2O4) принадлежит к пространственной решетке F d
m, параметр ячейки у которой 8.0830. Структура шпинели (ZnAl2O4) принадлежит к пространственной решетке F d 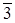 m, параметры ячейки которой 8.0860.
m, параметры ячейки которой 8.0860.
Итак, с помощью прикладных программ Dirichlet программного комплекса TOPOS рассчитаны основные характеристики соединений со структурой граната. Выявлена зависимость ширины энергетического зазора ∆Е13 от объема VПВД. Установлено, что зависимость можно аппроксимировать линейной функцией у=-534.55х+4892.6. С помощью установленной зависимости надежно прогнозируется ширина энергетического зазора ∆Е13 гранатов: Y3Al2(AlO4)3, Y3Sc2Al3O12, Gd3Sc2Ga3O12, Y3Ga2Al3O12, Sr3Y2(GeO4)3, Mg3Y2Ge3O12.
Список использованных источников:
1. Grimes N, Kay H, Thompson P
Magnesium dialuminium oxide / Proceedings of the Royal Society of London, Series A: Mathematical and Physical Sciences (76,1906-), стр. 333-345
2. Fischer P
Zinc dialuminium oxide MINR Gahnite - synthetic MINR Spinel group /Zeitschrift fuer Kristallographie,Kristallgeometrie, Kristallphysik, Kristallchemie (-144,1977), стр. 275-302
3. Ishizawa N, Marumo F, Minato I
Aluminium oxide - alpha MINR Corundum /Acta Crystallographica B (24,1968-38,1982), стр. 228-230
4. Каминский А.А., Аминов Л.К., Ермолаев В.Л. и др. Физика и спектроскопия лазерных кристаллов. М. Наука. 1986. 272 с.
5. Справочник по лазерам. Ред. Прохоров А.М. М. 1978. Сов. Радио. Т.1.
6. Geller S. Crystal chemistry of the garnets. //Z. Kristallographic. 1067. V. 125. № 1-6. P. 1-47.
7. O’Donnell K.P., Marshall A., Yamaga M. Vibronic structure in the photoluminescence spectrum of Cr3+ ions in garnets. //J. of Luminescence. 1989 V. 42 P. 365-373.
8. Ковба Л.М., Арсеньев П.А. Соединения редкоземельных элементов. Системы с оксидами элементов I- III групп. Серия «Химия редких элементов».М.: Наука, 1983. С. 280.
9. Кузьмичёва Г.М., Мухин Б.В., Жариков Е.В. Кристаллохимический анализ структурных особенностей гранатов. //Перспективные материалы. 1997. № 3. с.41-53.
10. Беляев Л.М., Любутин И.С., Милль Б.В. Катионное распределение в системе гранатов Ca3In2SnxGe3-xO12 по данным γ-резонансной спектроскопии. //Кристаллография, 1970. Т. 15. № 1. С. 174-175.
11. Недилько О.А. Изоморфное замещение в иттриево-алюминиевом гранате. //Украинский химический журнал. 1985. Т. 51. № 9. С. 899-901.
12. Морозова Л.Г., Феофилов П.П. Люминесцентное и рентгеноструктурное исследование системы 3Y2O3–(5-x)Ga2O3–xSc2O3. Изв. АН СССР. //Неорганические материалы. 1968. Т. 4. № 10. С. 1738-1743.
13. Кузьмичёва Г.М., Козликин С.Н. Кристаллохимический анализ образования твёрдых растворов на основе соединений со структурой граната. //Журнал неорганической химии. 1989. Т. 34. № 3. С. 576- 580.
14. Ефремов В.А., Захаров Н.Д., Кузьмичёва Г.М., Мухин Б.В. Иттрий- скандий- галлиевый гранат – кристаллическая структура. //Журнал неорганической химии, 1993. Т. 38. № 2. С. 220-225.
15. Ефиценко П.Ю., Касперович B.C., Кулешов А.А., Чарная Е.В. Исследование порядка в твёрдых растворах YxLu3-xA15O12 методами ЯМР. //Физика твёрдого тела, 1989. Т. 31. № 9. С. 170-173.
16. Stroka B., Hoist P., Tolksdorf W. An empirical formula for the calculation of lattice constants of oxide garnets based on substituted yttrium and gadolinium iron garnets. //Phillips J. Res., 1978. V. 33. № 3. -P. I86-202.
17. Зиновьев С.Ю., Кузьмичёва Г.М., Козликин С.Н. Особенности поведения твёрдых растворов редкоземельных галлиевых гранатов, содержащих скандий. //Журнал неорганической химии, 1990. Т. 35. № 9. С. 2197-2204
18. Аванесов А.Г., Данилов А.А., Денисов А.Л., Жариков Е.В. и др. Кристаллы иттрий-скандий-алюминиевого граната с хромом и неодимом как материал для активных сред твердотельных лазеров. //ДАН СССР. 1987. Т. 295. № 5. с. 1098-1191.
19. Аванесов А.Г., Балашов А.Б., Жуйко И.П., Игнатьев Б.В. и др. Особенности деактивации возбужденных состояний иона Cr3+ в кристаллах. Квантовая электроника. 1989. Т. 16. № 10. с. 2083-2086.
20. Sawada H. Electron density study of garnets: Z3Ga5O12; Z = Nd, Sm, Gd, Tb. //Journal of Solid State Chemistry. 1997. V. 132. P. 300-307.
21. Nakatsuka A., Yoshiasa A., Takeno S. Site preference of cations and structural variation in Y3Fe5-xGaxO12 (0<x<5) solid solutions with garnet structure. Acta Crystallographica B. 1995. V. 51. P. 737-745.
22. Efremov V.A., Zakharov N.D., Kuz'micheva G.M., Mukhin B.V., Chernyshev V.V. Yttrium-scandium-gallium garnet:the crystal structure. //Zhurnal Neorganicheskoi Khimii. 1993. V. 38. P. 220-225.
23. Yamazaki S., Marumo F., Tanaka K., Morikawa H., Kodama N., Kitamura K., Miyazawa Y. A structural study of facet and off-facet parts of rare-earth garnets, Gd3Sc2Al3O12, Gd3Sc2Ga3O12, and La3Lu2Ga3O12 La2.55Lu2.45Ga2.96O11.93. //Journal of Solid State Chemistry.1994. V. 108. P. 94-98.
24. Kondratyuk I.P., Zharikov E.V., Simonov V.I. Refinement of atomic structures of Gd3Sc2Ga3O12 and (Gd0.8Nd0.2)Sc2Ga3O12. //Kristallografiya. 1988. V. 33. P. 51-56.
25. Grinberg M. 2E→4A2 fluorescence of Cr3+ in high and intermediate field garnets. //J. of Luminescence. 1993. T. 54. P. 369-382.
26. Inorganic crystal structure database. Gmelin-Institut fur Anorganische Chemie & FIC Karlsruhe. 2004.