Рассмотрим теперь случаи, когда в полимер вводится низкомолекулярный растворитель:
а) расплав разбавляется растворителем
б) добавляем различное количество полимера в растворитель, образуются растворы полимера с различной концентрацией.
В этом случае можно, изучая свойства раствора, определять различные характеристики клубков полимерных молекул. При увеличении концентрации полимера клубки начинают взаимодействовать друг с другом, при дальнейшем увеличении концентрации клубки начинают переплетаться.
В растворах полимеров могут реализовываться несколько областей состояния:
1) в разбавленных растворах полимеров клубки макромолекул изолированы друг от друга
2) в полуразбавленных растворах начинается соприкосновение клубков и их проникновение друг в друга
3) в концентрированных растворах полимеров степень проникновения клубков друг в друга довольно велика
Для описания растворов полимеров можно использовать различные теории – теории Флори, Флори-Хаггинса, Де Жена.
В настоящее время для изучения вязкости растворов применяется нахождение степенной зависимости между вязкостью раствора и концентрацией полимера в нем (точные расчеты проводятся редко).
Согласно уравнению Эйнштейна, вязкость раствора полимера зависит от объемной доли частиц в нем следующим образом:
 ,
,
где 2,5 – коэффициент формы частицы (в данном случае частицы сферические).
Объемную долю частиц полимера в растворе можно выразить через концентрации этих частиц. Соответственно, с увеличением концентрации частиц и их объемная доля в растворе будет увеличиваться. Получаем, что с ростом концентрации частиц вязкость должна возрастать линейно. Это действительно наблюдается в некоторой области концентраций. Но при достижении некоторой концентрации с* происходит излом:
 lgη
lgη
tgβ=3.5
β
tgα=1
α
lg с* lgс
Область с tgα=1 является областью разбавленных растворов, в которых клубки макромолекул практически не сопротивляются, они как бы изолированы в пространстве и не взаимодействуют друг с другом. Эта область концентраций используется для изучения размеров и свойств клубков макромолекул. Выше концентрации с* наблюдается резкий излом, мы переходим к полуразбавленным растворам. Далее растворы становятся концентрированными (тангенс наклона кривой увеличивается). Значение критической концентрации с* связано с характеристической вязкостью:


Характеристическая вязкость [η] представляет объем изолированного клубка.
Таким образом, при с=с* весь объем раствора заполнен клубками макромолекул, которые практически не проникают друг в друга.
Для изучения свойств растворов полимеров можно использовать явление осмоса. Т.к. растворы равновесны, то можно применить уравнения состояния:
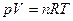 (для газов)
(для газов)
 (для жидкостей)
(для жидкостей)
При образовании растворов химический потенциал понижается:
 , появляется движущая сила перехода растворителя в раствор.
, появляется движущая сила перехода растворителя в раствор.
 |
Растворенное вещество Полупроницаемая мембрана растворитель
Если разделить растворитель и раствор полупроницаемой мембраной, то сначала уровни жидкости будут одинаковы, затем происходит миграция растворителя через мембрану из-за возникающей разности термодинамических потенциалов растворителя в чистом растворителе и в растворе, образуется разность уровней жидкости Δh, измеряя которую можно определить осмотическое давление растворителя.
Принимая раствор идеальным можно записать соотношение:

Для реальных растворов применим закон Ван-дер-ваальса:
 , где а – константа сцепления, b – константа отталкивания
, где а – константа сцепления, b – константа отталкивания
Существующую зависимость разлагают в ряд:
 , где
, где  ,
,  , слагаемыми высших порядков пренебрегают. Привязка делается к реальным системам, второе слагаемое показывает все парные взаимодействия; третий член - тройные взаимодействия, роль которых в общей картине незначительна, им пренебрегают; взаимодействия более трех частиц одновременно друг на друга очень маловероятно, ими также пренебрегают.
, слагаемыми высших порядков пренебрегают. Привязка делается к реальным системам, второе слагаемое показывает все парные взаимодействия; третий член - тройные взаимодействия, роль которых в общей картине незначительна, им пренебрегают; взаимодействия более трех частиц одновременно друг на друга очень маловероятно, ими также пренебрегают.
Существует некоторая температура, называемая тета-температурой, при которой А2=0. В этой точке силы сцепления и отталкивания точно компенсируют друг друга, а раствор ведет себя как идеальный. Можно подобрать θ-растворитель, в котором А2=0.
В зависимости от взятого растворителя могут наблюдаться различные случаи взаимодействия полимера с растворителем:


А2>0
А2=0
А2<0
c
Если А2>0, то растворитель считается "хорошим" (полимер хорошо растворим в растворителе, клубки макромолекул в растворе достаточно развернутые); если А2<0, то растворитель считается "плохим" (в нем полимер либо вообще не растворим, либо растворим ограниченно в узком интервале концентраций), либо образуемые растворы неустойчивы, клубки макромолекул в таких растворах сжаты).
Таким образом, термодинамическое состояние клубков определяется растворителем.
Рассмотрим вязкость разбавленных растворов полимеров.
Выше было рассмотрено уравнение Эйнштейна:

и вводилось понятие характеристической вязкости, которая представляется в виде:

Из этого выражения следует, что величина [η] не должна зависеть от молекулярной массы полимера, а лишь от его плотности.
Однако, реальная зависимость характеристической вязкости от молекулярной массы растворенного полимера выражается степенной зависимостью:

-это выражение носит название закона Марка-Куна-Хаувинка
Из этого полуэмпирического закона следует, что характеристическая вязкость не зависит от ММ полимера только при α=0, при α≠0 зависимость от ММ существует в любом случае. Покажем, что это вытекает из рассмотрения конформации макромолекулярных клубков и занимаемого ими объема:
принимаем, что клубки имеют сферическую форму, тогда 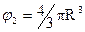 , отсюда получим, что
, отсюда получим, что  . Т. к. радиус клубка
. Т. к. радиус клубка  ,то
,то  , где Ф – комплексная константа. Полученное уравнение называется уравнением Флори-Фокса. Его можно привести к виду уравнения Марка-Куна-Хаувинка. Т. к. радиус клубка зависит от ММ макромолекулы, то справедливо соотнести оба полученных уравнения:
, где Ф – комплексная константа. Полученное уравнение называется уравнением Флори-Фокса. Его можно привести к виду уравнения Марка-Куна-Хаувинка. Т. к. радиус клубка зависит от ММ макромолекулы, то справедливо соотнести оба полученных уравнения:
 , где К является константой для данной системы полимер-растворитель. Получаем, что по теории Флори-Фокса степенной коэффициент α должен быть равен ½.
, где К является константой для данной системы полимер-растворитель. Получаем, что по теории Флори-Фокса степенной коэффициент α должен быть равен ½.
В действительности, α=1/2 описывает растворы в θ-точке (т.е. поведение макромолекул в θ-растворителе. В "хорошем" растворителе α>0,5 (обычно находится в интервале 0,6÷0,8, хотя может достигать 1 и более – для растворов полимеров, в которых макромолекулы представляют собой "палочки" или длинные плавно изогнутые цепи). В плохом же растворителе α<0,5 (обычно находится в интервале 0,2÷0,4). Случай, в котором α=0 лишен всякого смысла, поэтому в любом случае характеристическая вязкость зависит от молекулярной массы макромолекулы.