по дисциплине Физическая химия
наименование учебной дисциплины
Выполнил
Студент, группы НМб-12-1 (подпись) А.В.Тищенко
(дата)
23.12.13
Принял
Преподаватель (подпись) Ф.М.Лебедь
(дата)
Иркутск –2013
1 Краткое теоретическое введение
Составы трехкомпонентных систем удобно представлять в виде равностороннего треугольника (диаграмма Гиббса-Розебома). Вершины такого треугольника соответствуют чистым компонентам 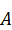 ,
, 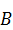 ,
, 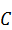 , а точки внутри – всем возможным составам трехкомпонентной системы. Точки на сторонах треугольника отвечают составам граничных двухкомпонентных систем. Приняв высоту треугольника за единицу, длина перпендикуляра, опущенного из взятой внутри треугольника точки на сторону, противоположную вершине А, будет равна мольной (весовой, объемной) доле компонента А во взятой точке. Сумма перпендикуляров, опущенных из любой точки внутри равностороннего треугольника, равна высоте этого треугольника. Сумма мольных (весовых, объемных) долей равна единице, что показано в формуле (1).
, а точки внутри – всем возможным составам трехкомпонентной системы. Точки на сторонах треугольника отвечают составам граничных двухкомпонентных систем. Приняв высоту треугольника за единицу, длина перпендикуляра, опущенного из взятой внутри треугольника точки на сторону, противоположную вершине А, будет равна мольной (весовой, объемной) доле компонента А во взятой точке. Сумма перпендикуляров, опущенных из любой точки внутри равностороннего треугольника, равна высоте этого треугольника. Сумма мольных (весовых, объемных) долей равна единице, что показано в формуле (1).
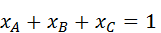 (1)
(1)
Диаграмма Гиббса-Розенбома представляет трехкомпонентную систему при фиксированных температуре 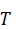 и давлении
и давлении 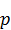 . Правило фаз записывается в виде, приведенном в формуле (2).
. Правило фаз записывается в виде, приведенном в формуле (2).
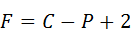 (2)
(2)
где 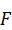 – число степеней свободы;
– число степеней свободы;
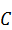 - число компонентов в системе;
- число компонентов в системе;
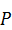 - число сосуществующих фаз.
- число сосуществующих фаз.
Чтобы определить состав тройной системы, отвечающей границе перехода из однофазной области в двухфазную, находится процент объема от общего объема добавленного компонента (например, для компонента 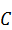 ); см. формулу (3).
); см. формулу (3).
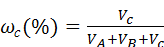 (3)
(3)
где 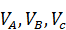 - объемы компонентов
- объемы компонентов 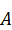 ,
, 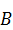 ,
, 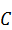 соответственно, мл.
соответственно, мл.
2 Расчетная часть
Изначально готовится раствор этиловый спирт-толуол в разных концентрациях (по объему). Затем каждый раствор титруется водой до образования второй фазы.
Примечания
1 В последующих расчетах плотности (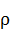 ) этилового спирта, толуола и воды были взяты 0,789 г/мл; 0,867 г/мл; 0,998 г/мл соответственно.
) этилового спирта, толуола и воды были взяты 0,789 г/мл; 0,867 г/мл; 0,998 г/мл соответственно.
2 Далее приведены примеры вычислений табличных значений для компонентов 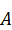 ,
, 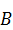 ,
, 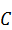 с объемами 5; 5 и 0.6 мл соответственно. Значения
с объемами 5; 5 и 0.6 мл соответственно. Значения  ,
, 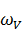 ,
, 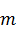 ,
, 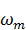 ,
, 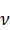 ,
, 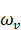 для других процентных содержаний веществ в системе находятся аналогичным образом.
для других процентных содержаний веществ в системе находятся аналогичным образом.
В соответствии с формулой (3) можно вычислить 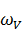
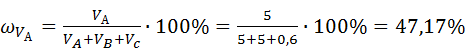
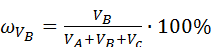 = 47,17%
= 47,17%
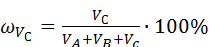 = 5,66%
= 5,66%
Далее приводятся вычисления масс, согласно формуле
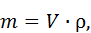 (4)
(4)
где 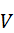 - объем жидкости, мл
- объем жидкости, мл
ρ – плотность жидкости, г/мл.
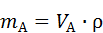 = 3,94 г.
= 3,94 г.
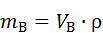 = 4,33 г.
= 4,33 г.
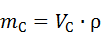 =0,6 г.
=0,6 г.
Далее приводятся вычисления 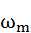 согласно формуле (3), где
согласно формуле (3), где 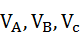 заменены на
заменены на 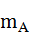 ,
, 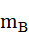 и
и 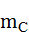 соответственно
соответственно
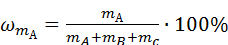 = 44,43%
= 44,43%
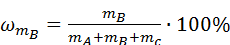 = 48,82%
= 48,82%
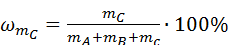 = 6,74%
= 6,74%
Далее приводятся вычисления 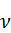 согласно формуле
согласно формуле
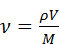 , (5)
, (5)
где 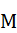 - молярная масса компонента
- молярная масса компонента
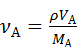 = 0.08 моль
= 0.08 моль
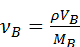 = 0,04 моль
= 0,04 моль
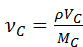 = 0,03
= 0,03
Далее приводятся вычисления 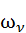 согласно формуле (3), где
согласно формуле (3), где 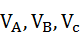 заменены на
заменены на 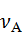 ,
, 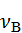 и
и 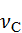 соответственно
соответственно
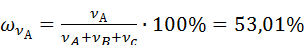
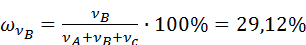
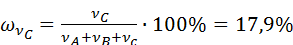
Таблица 1 – Результаты опытов по изучению растворимости в трехкомпонентной системе
| № | Вещества | 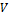 , мл , мл
| 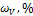
| 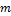 , г , г
| 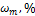
| 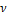 , моль , моль
| 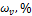
|
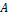
| 47,1698113 | 3,945 | 44,43168 | 0,08563242 | 53,0048311 | ||
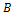
| 47,1698113 | 4,335 | 48,8241654 | 0,04704797 | 29,1217941 | ||
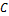
| 0.6 | 5,66037736 | 0,5988 | 6,74415462 | 0,02887549 | 17,8733749 | |
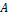
| 38,4615385 | 3,156 | 36,0389165 | 0,06850594 | 47,5030296 | ||
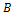
| 57,6923077 | 5,202 | 59,4025488 | 0,05645756 | 39,1485102 | ||
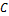
| 0.4 | 3,84615385 | 0,3992 | 4,55853469 | 0,01925033 | 13,3484602 | |
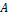
| 29,1262136 | 2,367 | 27,0966413 | 0,05137945 | 39,0171273 | ||
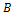
| 67,961165 | 6,069 | 69,4759255 | 0,06586716 | 50,0189704 | ||
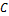
| 0.3 | 2,91262136 | 0,2994 | 3,4274332 | 0,01443774 | 10,9639022 | |
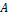
| 19,8019802 | 1,578 | 18,3194409 | 0,03425297 | 29,9565145 | ||
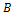
| 79,2079208 | 6,936 | 80,5219531 | 0,07527675 | 65,8345609 | ||
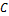
| 0.1 | 0,99009901 | 0,0998 | 1,15860596 | 0,00481258 | 4,20892462 | |
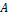
| 9,94035785 | 0,789 | 9,11940526 | 0,01712648 | 16,3576142 | ||
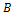
| 89,4632207 | 7,803 | 90,1884908 | 0,08468635 | 80,8844696 | ||
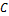
| 0.06 | 0,59642147 | 0,05988 | 0,69210391 | 0,00288755 | 2,75791625 | |
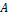
| 19.6 | 66,2162162 | 15,4644 | 62,3831154 | 0,33567909 | 53,8502913 | |
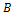
| 16,8918919 | 4,335 | 17,4873131 | 0,04704797 | 7,54752676 | ||
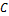
| 16,8918919 | 4,99 | 20,1295715 | 0,24062907 | 38,6021819 | ||
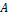
| 15.4 | 60,6299213 | 12,1506 | 57,2774069 | 0,26374786 | 55,6438934 | |
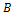
| 27,5590551 | 6,069 | 28,6090055 | 0,06586716 | 13,8962462 | ||
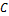
| 11,8110236 | 2,994 | 14,1135875 | 0,14437744 | 30,4598603 | ||
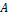
| 10,4 | 50,9803922 | 8,2056 | 48,2495031 | 0,17811544 | 57,2851809 | |
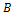
| 44,1176471 | 7,803 | 45,8821869 | 0,08468635 | 27,2366776 | ||
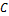
| 4,90196078 | 0,998 | 5,86830995 | 0,04812581 | 15,4781415 |
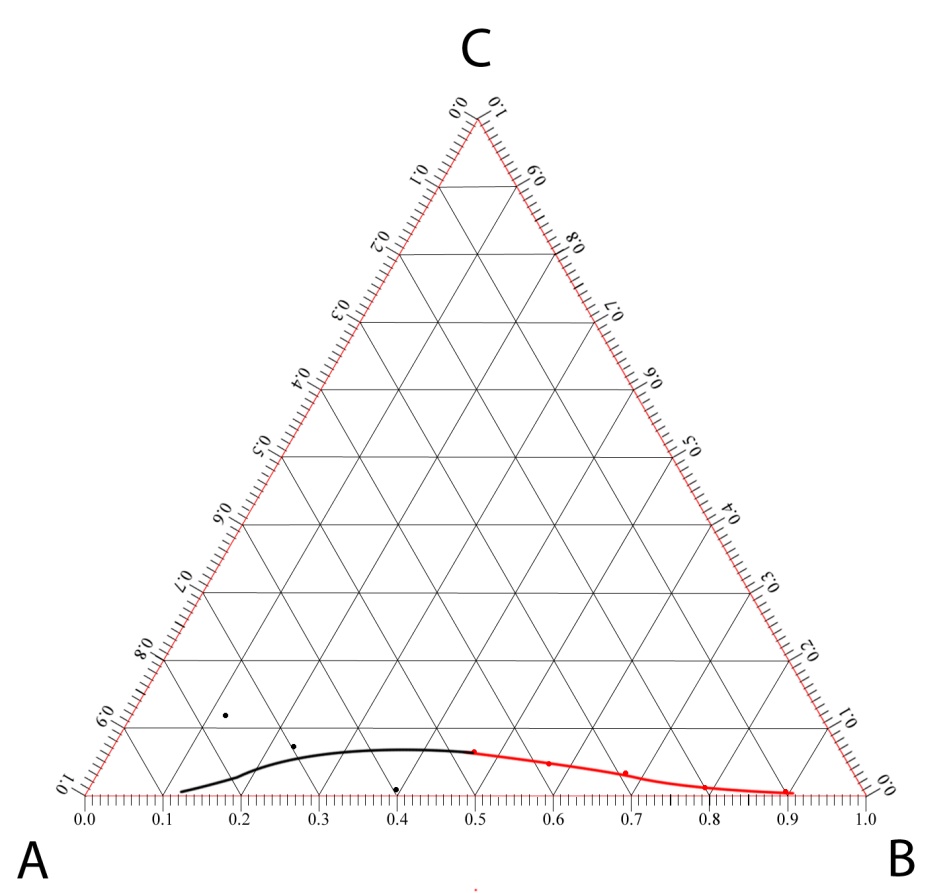
Рисунок 1 – Фазовая диаграмма
Примечание – красным цветом показана кривая расслаивания при титровании смеси водой; черным – при титровании спиртом (средняя линия). Из-за того, что точки на графике отличаются от теоретически предполагаемых, пример линии через которых представлен на рис. 2 в инструкции к выполнению лабораторной работы, то критическая точка расслаивания Q далее не приводится.
Вывод
В данной лабораторной работе была изучена фазовая диаграмма трехкомпонентной системы с ограниченной взаимной растворимостью. По сравнению с теоретической диаграммой состояния тройной жидкой системы, полученная диаграмма несколько отличается, а именно, при титровании смеси толуол – вода спиртом. Возможно при последней серии титрований было получено недостаточное количество точек диаграммы или же она была недостаточно корректно выполнена, что, в итоге, стало причиной отличного от теоретически правильного графика.