1) Тmax – максимальная температура;
2) ветви: нагрева – 1 и охлаждения – 2;
3) ω = dT/dt – скорость изменение температуры на 1 ветви ω = dT/dt > 0 – скорость нагрева на 2 ветви ω = dT/dt < 0 – скорость охлаждения;
4) ωmax – максимальная скорость охлаждения;
5) t* – время пребывания сплава выше температуры T*.

Рис. 3.25. Параметры термического цикла
0.21.3. Образование сварочной ванны и формирование шва при сварке плавлением
Цель плавления при сварке – осуществить соединение свариваемых деталей.
Теоретически достаточно расплавить свариваемые кромки на глубину нескольких атомных слоев от плоскости стыка.
Практически из-за дефектов сборки под сварку, а именно:
1) из-за зазора в стыке;
2) не прямолинейности стыка;
3) превышения кромок соединяемых деталей друг относительно друга, приходится ширину зоны плавления увеличивать до нескольких мм от оси стыка.
Дефекты сборки являются существенным препятствием для применения высококонцентрированных источников энергии, таких как электронный луч и луч лазера.
Сварочная ванна – область свариваемого материала, нагретая выше температуры солидуса.
Температура сварочной ванны не поддается пока даже численному расчету. Существующие экспериментальные данные для малоуглеродистых сталей дают диапазон tcр = 1700 – 1800°С.
Зона проплавления – след в основном металле от перемещения сварочной ванны.
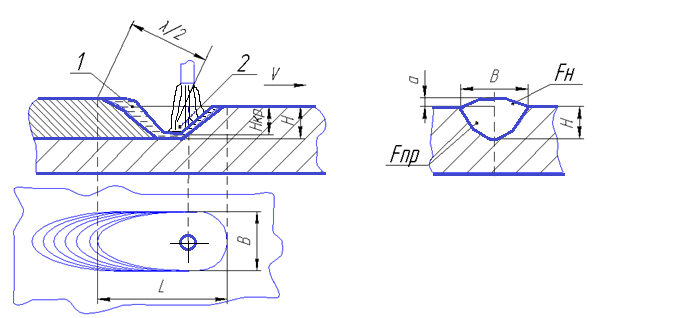
Рис. 3.26. Образование сварочной ванны и формирование шва:
1 – сварочная ванна; 2 – кратер; Нк – глубина кратера; Н – глубина проплавления;
L – длина сварочной ванны; В – ширина сварочной ванны; а – усиление сварного шва; Fпр,Fн – площадь проплавления, наплавки; Н/В – относительная глубина проплавления;
μ = Fпр/Н*В – коэффициент полноты шва (обычно μ = 0,6...0,8)
Формирование сварного шва происходит следующим образом. Под действием тепловых потоков от анодного (катодного) потока дуги и от окружающих дугу горячих газов основной металл расплавляется и под действием давления дуги оттесняется в заднюю (хвостовую) часть ванны. Это перемещение жидкого металла сварочной ванны имеет гидродинамическую природу и в сварочной ванне всегда существует полуволна жидкого металла. Гребень этой полуволны фиксируется в задней части ванны фронтом кристаллизации (рис. 3.26).
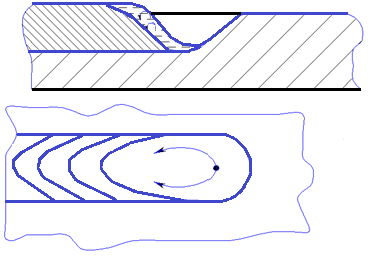
Рис. 3.27. Потоки металла в сварочной ванне
В сварочной ванне потоки жидкого металла из кратера в хвостовую часть способны создать вихри (рис. 3.27).
При некоторых способах сварки в сварочную ванну поступает и шлак, который увлекается потоками, перемещается в хвостовую часть и взаимодействует с жидким металлом.
Наиболее распространенным дефектом формирования сварного шва является подрез – опасный концентратор напряжений.
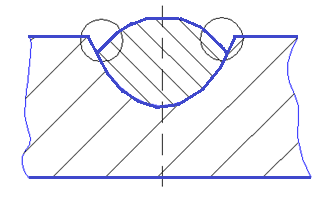
Рис. 3.28. Образование подрезов
Наличие или отсутствие подреза определяется соотношением между давлением дуги, силами поверхностного натяжения и объемом сварочной ванны. Чем больше силы давления дуги, тем выше скорость оттока жидкого металла и тем выше гребень и фиксируемый кристаллизацией подрез. Чем выше коэффициент поверхностного натяжения и чем больше вязкость жидкого металла, тем меньше величина подреза.
Правильным выбором параметров режима сварки можно добиться смещения гребня полуволны жидкого металла ближе к средней части сварочной ванны и, тем самым, добиться уменьшения величины подреза.
С ростом скорости сварки подрезы возрастают.
0.21.4. Оценка длины сварочной ванны
Для оценки используются уравнения, связывающие между собой температуру, время и координаты точек тела.
При сварке мощным быстродвижущимся источником тепла температурное поле в полубесконечном теле описывается:
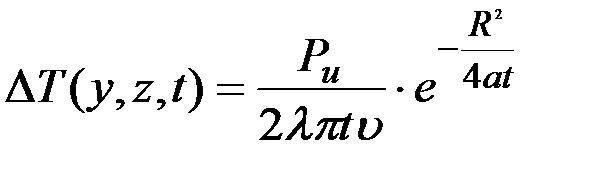 , где R2 = y2 + z2 (3.25)
, где R2 = y2 + z2 (3.25)
Так как максимальная длина ванны лежит на оси ОХ, то положим у = 0 и z = 0, R = 0. Тогда Т(0, t) = Pи/(2πλν).
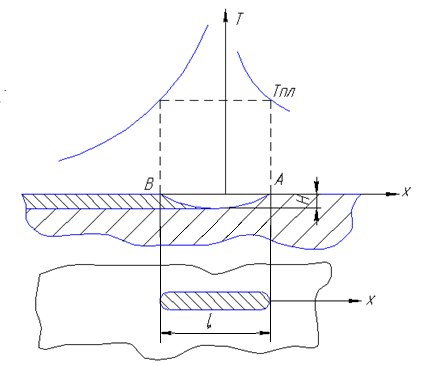
Рис. 3.29. Длина сварочной ванны
Время пребывания в жидком состоянии tж – равно времени прохождения дуги от т. А до т. Б при этом подставим Т = Тпл, t = tж, тогда
Тпл = Ри/(2πλ·ν·tж), откуда
tж = 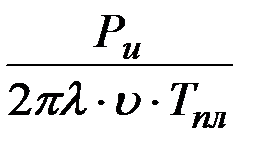 =
= 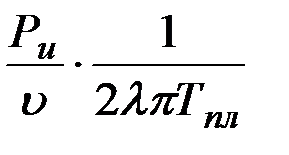 =
= 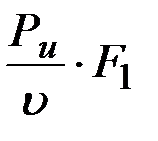 . (3.26)
. (3.26)
Т.е. время пребывания в жидком состоянии каждого элемента, лежащего на оси шва, пропорционально погонной энергии.
По известным tж и υ сварки определим длину ванны L:
L = υ·tж = 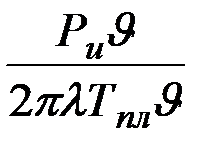 =
= 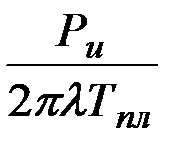 = Ри·F1. (3.27)
= Ри·F1. (3.27)
Таким образом, длина сварочной ванны пропорциональна эффективной мощности источника. При определении длины сварочной ванны с помощью ЭВМ используется уравнение температурного поля при у = 0 и z = 0.
1. Определяем координаты пребывания элементов сварочного шва при Т > Тпл.
2. L = x1 + 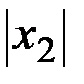 .
.
0.21.5. Расчет ширины зоны, нагретой выше заданной температуры
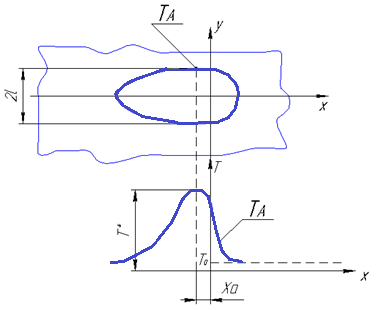
Рис. 3.30.
2l – ширина зоны, нагретой выше заданной температуры Т*; А – точка максимальной ширины изотермы
Стоит задача: определить величину 2 l.
Возможны два пути решения задачи: с помощью номограмм и ЭВМ.
1. Решение с помощью номограмм. Используем номограммы, приведенные в учебниках и справочниках по тепловым процессам при сварке, например: «Теория сварочных процессов» под редакцией В. В. Фролова.
1) Вычисляем безразмерные величины
полубесконечное тело: (4πλаТ*)/Риυ;
бесконечная пластина: (2πλδТ*)/Ри.
2) По номограммам определяем 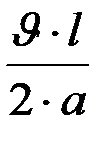
3) Определяем искомую 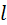 и ширину шва 2
и ширину шва 2 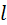 .
.
2. Алгоритм расчета на ЭВМ
Используем уравнения температурного поля:
полубесконечное тело
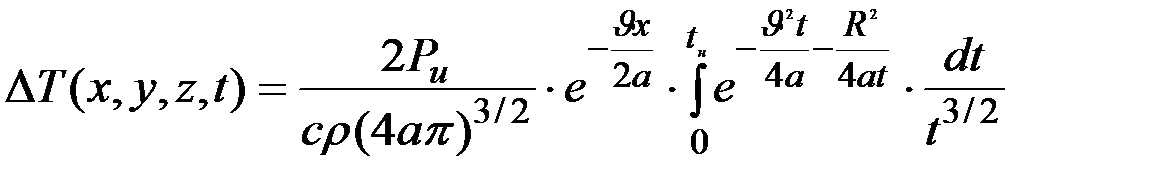 (3.27)
(3.27)

Рис. 3.31. Номограммы для определения ширины зоны нагрева 2 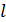
движущимся источником теплоты:
а) полубесконечное тело; б) бесконечная пластина
бесконечная пластина
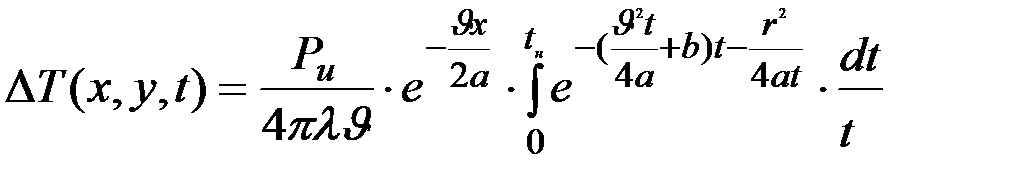 (3.28)
(3.28)
0.21.6. КПД процесса проплавления
На проплавление основного металла расходуется только часть тепла дуги. Тепло, затраченное на проплавление металла в единицу времени, или тепловую мощность можно подсчитать, зная объем проплавляемого металла в единицу времени V = Fпр*υ, его теплосодержание сρТs:
qпр = υFпрcρTs, (3.29)
где Ts – температура солидуса.
Отношение тепловой мощности, затрачиваемой на проплавление, к полной тепловой мощности дуги называют полным тепловым коэффициентом полезного действия.
ηпр = 
 . (3.30)
. (3.30)
Процесс проплавления сварочной дугой можно подразделить:
1) нагрев основного металла за счет тепла дуги, но при этом в металл идет не все тепло дуги, а лишь часть, которую можно оценить эффективным КПД ηи:
ηи = 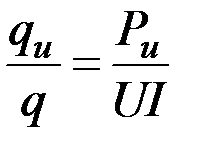 (3.31)
(3.31)
2) проплавление основного металла; при этом расходуется не все тепло, переданное дугой металлу, а лишь его часть, оцениваемая термическим КПД
ηт = 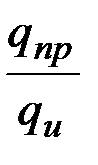 (3.32)
(3.32)
Полный тепловой КПД равен произведению эффективного и термического коэффициентов полезного действия
ηпр = 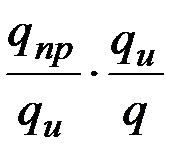 = ηт·ηи (3.33)
= ηт·ηи (3.33)
0.21.7. Нагрев и плавление электродного материала
Электроды делятся на плавящиеся и неплавящиеся.
Плавящиеся электроды:
а) покрытые – имеют конечную длину и неподвижный токоподвод, например штучные электроды ДЭС;
б) голые – имеют условно бесконечную длину и подвижный относительно электрода токоподвод.
У покрытых электродов защита дуги, сварочной ванны и требуемая металлургическая обработка осуществляется за счет материала покрытия – легирующие, ионизирующие, газозащитные компоненты.
У голых электродов защита дуги осуществляется за счет подаваемых в зону дуги газов, активных или инертных.
Рассмотрим второй случай, имеющий место при СПЭ.
Электрод нагревают 2 источника тепла:
1) распределенный по объему источник qт, выделяющий тепло по закону Джоуля-Ленца при прохождении через электрод тока дуги, он имеет возрастающий характер, так как существует саморазогрев электрода проходящим током;
2) сосредоточенный плоский источник тепла – электродная область сварочной дуги qд;

Рис. 3.32. Схема плавления голого электрода:
1 – распределение тепловых потоков qт и qд; 2 – распределение Т
Тепловым потоком вдоль оси электрода, обусловленном теплопроводностью материала электрода пренебрегаем, т.е. считаем, что скорость подачи электродной проволоки Vэ значительно превышает скорость распространения тепла.
Температурное поле от электродной дуги считаем квазистационарным.
Принимаем подвижную систему координат с центром в точке О, расположенной на торцевом сечении электрода, оплавляемой дугой.
Каждая частица материала электрода Vэ в своем движении от точки контакта А до точки О (электродного пятна дуги) нагревается от проходящего тока и от тепла дуги до температуры Тк (капель), которая определяется экспериментально и составляет для стальных электродов Тк = 2300 – 2500°С.
Скорость подачи электрода подбирают опытным путем близкой к скорости плавления электрода, которая определяется величиной тока, напряжением на дуге, длиной вылета и теплофизическими параметрами материала электрода.
0.22. Кристаллизация металла и образование соединения
0.22.1. Общие положения теории кристаллизации
Положение 1. Для начала кристаллизации необходимо наличие центров кристаллизации.
Ими могут быть зародыши твердой фазы, образовавшиеся вследствие переохлаждения жидкости, или частицы примеси.
Положение 2. Зародыши твердой фазы находятся в состоянии динамического равновесия с окружающей жидкостью (т.е. могут растворяться в жидкости и возникать вновь и т.п.). Возникновение твердой фазы сопровождается выделением теплоты кристаллизации, что ведет к повышению температуры в окружающем объеме жидкости и может вызвать расплавление образовавшейся твердой фазы.
Если какой-то из зародышей вследствие благоприятного сочетания флуктуций температуры и градиента температуры достиг радиуса, называемого критическим, то он уже становится устойчивым и приобретает способность к дальнейшему росту:
rкр = 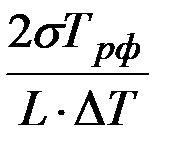 , (3.34)
, (3.34)
где: σ – поверхностная энергия раздела жидкой и твердой фазы
L – скрытая теплота фазового превращения
Трф – температура равновесия фаз
∆Т – величина переохлаждения.
Положение 3. Для непрерывного роста твердой фазы необходимо, чтобы температура межфазной границы была ниже температуры равновесия фаз Трф в течение всего процесса кристаллизации.
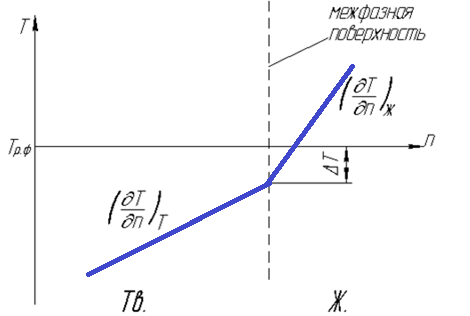
Рис. 3.33. Переохлаждение межфазной границы
В реальных условиях межфазная граница не является идеально плоской, а принимает ступенчатую форму (рис. 3.34).
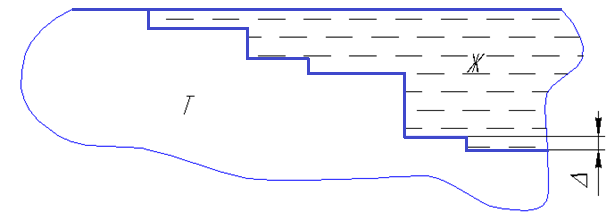
Рис. 3.34. Ступенчатая форма межфазной границы
∆ = от одного атомного слоя до 100 атомных слоев.
Положение 4. Если создать такие условия, когда по мере удаления от фронта кристаллизации в жидкость ее температура будет понижаться (выделяется теплота кристаллизации), то устойчивость межфазовой границы нарушится и возникает дендритная кристаллизация.
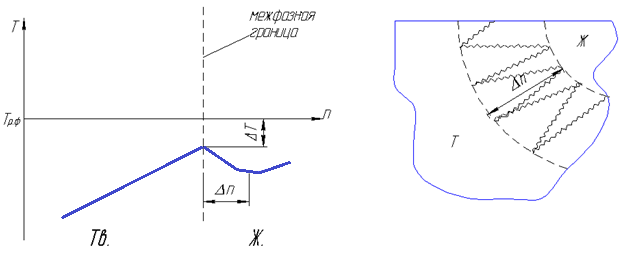
Рис. 3.35. Возникновение дендритов
 < 0 – условие возникновения дендритов.
< 0 – условие возникновения дендритов.
Если какой-либо участок межфазной границы выдвинулся вперед, то он попадает в область повышенного переохлаждения, что вызывает его дальнейший рост и образуется дендрит. Направление роста дендритов соответствует кристаллографическим осям затвердевающего металла.
Положение 5. При кристаллизации сплава, в первую очередь, кристаллизуется чистое вещество основы сплава, перед межфазной границей образуется область повышенной концентрации легирующих элементов и примесей, мешающих доступу новых порций чистого вещества, основы для достройки кристаллов.
Выравнивание концентраций осуществляется путем диффузии легирующих элементов и примесей в твердую фазу и за счет конвекции жидкости.
Если скорость диффузии недостаточна и конвекция не выравнивает концентрацию, то возникает дендритная структура, вызванная концентрационной неоднородностью.
Если какой-либо участок межфазовой границы выдвинулся вперед, то он попадает в область чистого вещества основы сплава и приобретает способность к дальнейшему росту, и образует дендрит.
Между основаниями дендритов остается область, обогащенная легирующими элементами и примесями (либо эвтектика, либо обогащенный твердый раствор). Эта область фиксируется в твердой фазе по границам кристаллов (зерен).
Центры кристаллов обеднены легирующими элементами и примесями: существует межкристаллическая химическая неоднородность.
Кристаллит – кристалл неправильной формы (зерно).
0.22.2. Особенности кристаллизации сварного шва
1. Сварочная ванна условно разделяется на две части: переднюю, где происходит плавление и хвостовую, в которой происходит кристаллизация.
2. Объем жидкого металла колеблется для различных условий сварки от 0,0005 см3 (лазерная сварка) до 200 см3 (электрошлаковая сварка).
3. Происходят непрерывные процессы плавления, течения жидкого металла и его кристаллизация.
4. Градиенты температуры, перпендикулярные фронту кристаллизации, изменяются в больших пределах для различных участков фронта.
5. Несмотря на то, что средняя скорость кристаллизации равна скорости сварки, скорости кристаллизации на отдельных участках фронта кристаллизации существенно различны.
6. Скорости кристаллизации изменяются во времени в зависимости от гидродинамики потока жидкого металла сварочной ванны и условий отвода выделяющейся теплоты кристаллизации. Периоды ускоренного роста сменяются периодами замедления и даже остановок роста кристаллов вследствие выделившейся теплоты кристаллизации.
0.22.3. Первичная структура сварного шва и факторы, влияющие на нее
Для первичной структуры сварного шва характерны дендриты, объединенные в столбчатые кристаллы, рост которых начинается от готовых центров кристаллизации, представляющих собой оплавленные зерна основного металла на границе раздела фаз.
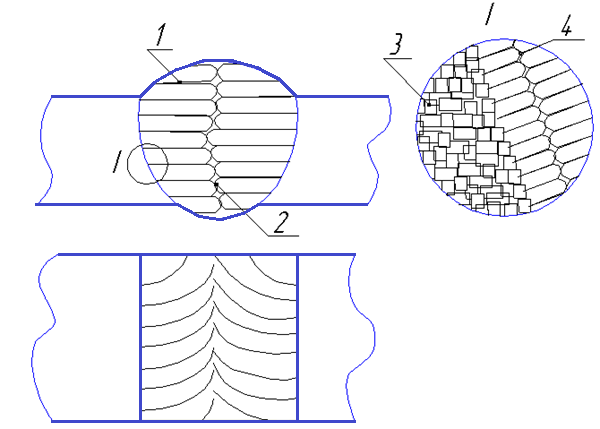
Рис. 3.36. Первичная структура сварного шва:
1 – проекции столбчатых кристаллов; 2 – зона стыковых столбчатых кристаллитов (одно из самых слабых мест сварного шва); 3 – кристаллиты основного металла; 4 – граница
кристаллизационных слоев
Каждый столбчатый кристалл состоит из нескольких дендритов.
Факторы, влияющие на формирование первичной структуры сварного шва.
1. Структура исходного состояния основного металла (зерна основного металла являются центрами кристаллизации, а выросшие на их основе кристаллы шва сохраняют направления кристаллографических осей зерен основного металла).
2. Направления тепловых потоков ≡ направления 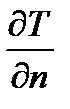 . Кристаллы стремятся расти в направлении теплового потока (в направлении уменьшения
. Кристаллы стремятся расти в направлении теплового потока (в направлении уменьшения 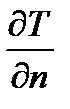 ). Оси растущих кристаллов перпендикулярны изотермической поверхности кристаллизации.
). Оси растущих кристаллов перпендикулярны изотермической поверхности кристаллизации.
3. Длительность пребывания сварочной ванны при высокой температуре (чем выше длительность пребывания, тем больше размеры кристаллитов).
При кристаллизации имеют место две тенденции:
- с одной стороны, кристаллы стремятся расти перпендикулярно изотермической поверхности кристаллизации;
- с другой стороны, условие перпендикулярности нарушается, так как кристаллы стремятся сохранить ориентировку кристаллов основного металла, которые для них были центрами кристаллизации.
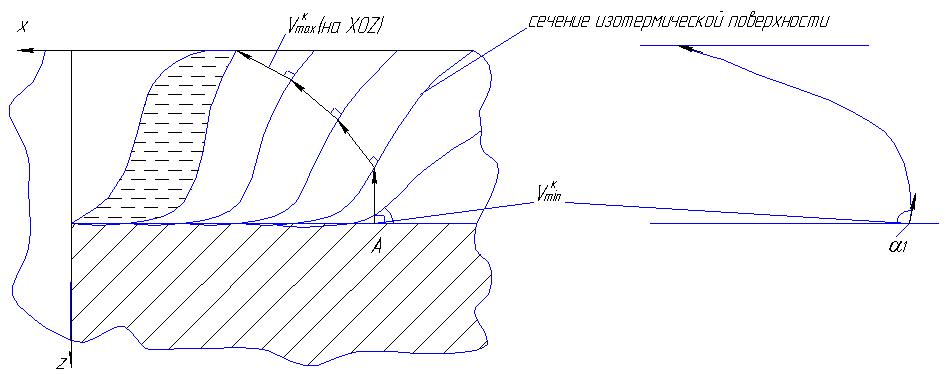
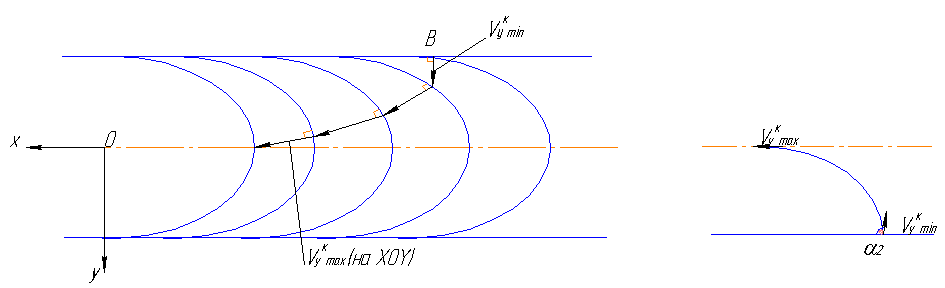
Рис. 3.37. Схема кристаллизации сварочной ванны
0.22.4. Способы регулирования первичной структуры сварного шва
1. Основной способ – воздействие на дугу и на металл сварочной ванны переменного внешнего магнитного поля.
2. Реже применяется механическая вибрация: электрода, присадочного материала, свариваемого изделия.
3. Положительно влияет на измельчение зерна импульсный режим питания сварочной дуги: разделяются процессы плавления и кристаллизации сварочной ванны.
Переменное внешнее магнитное поле вызывает:
а) колебание электрической дуги;
б) вихревое движение жидкого металла сварочной ванны, возникающее под действием электромагнитных сил в объеме ванны.

Рис. 3.38. Воздействие внешнего переменного магнитного поля
на сварочную ванну:
а) создание вихревых токов и электродинамических сил; б) зависимость среднего
размера кристаллита от частоты внешнего магнитного поля
Направление вихревого движения жидкого металла меняется с частотой внешнего магнитного поля. Перемещения жидкого Ме в сварочной ванне вызывает оплавление ранее выросших дендритов, измельчение кристаллитов.
Например, при сварке неплавящимся электродом в среде аргона стали 12Х18Н10Т при применении внешнего переменного магнитного поля, размер кристаллитов уменьшается в 3 – 4 раза (рис. 3.38б).
0.22.5. Химическая неоднородность сварного шва
Даже в случае равновесной кристаллизации слои, кристаллизовавшиеся раньше, обеднены легирующими элементами и примесями, слои, кристаллизовавшиеся позднее, напротив, будут обогащены. Таким образом, возникает химическая неоднородность сплава.
При сплаве кристаллизация всегда протекает неравновесно, что усиливает химическую неоднородность сварного шва, т.к. выравнивание разности концентраций в жидком сплаве не успевает проходить, растворенный элемент в большей степени обогащает те объемы жидкости, которые кристаллизуются позднее. Это обычно междуосные пространства одного дендрита или междендритные пространства.
Такую микроскопическую неоднородность называют внутрикристаллической ликвацией.
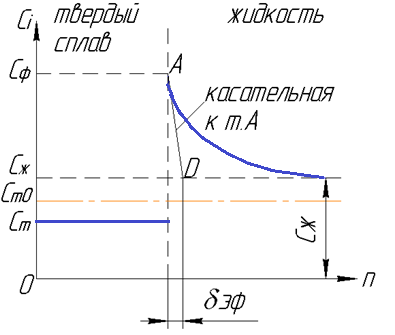
Рис. 3.39. Распределение легирующего элемента у фронта кристаллизации
Сi – концентрация легирующего элемента или примеси; Сто – концентрация легирующего элемента или примеси до сварки; Ст – концентрация легирующего элемента или примеси в ранее закристаллическом объеме; Сф – концентрация легирующего элемента или примеси на межфазовой границе; Сж – концентрация легирующего элемента или примеси в отсавшемся объеме жидкости; δэф – эффективная ширина пограничного слоя δэф≈ 10-3 см.
R = 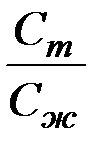 – коэффициент распределения.
– коэффициент распределения.
0.22.6. Меры уменьшения химической неоднородности при сварке
Рассмотрим степень химической неоднородности ε в зависимости от скорости охлаждения ω.
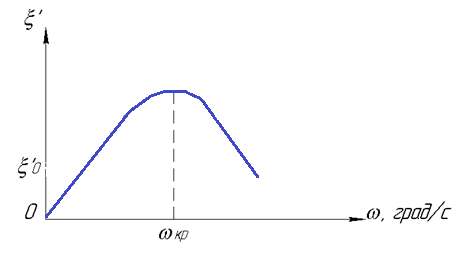
Рис. 3.40. Влияние скорости охлаждения на степень
внутрикристаллической ликвации
Вначале имеет место рост химической неоднородности из-за увеличения неравновесности процесса кристаллизации.
При ω > ωкр степень межкристаллитной химической неоднородности уменьшается по следующим причинам:
а) уменьшаются размеры дендритов и участков микрохимической неоднородности;
б) более равномерно по объему расположены участки химической микронеоднородности.
Основными мерами уменьшения химической неоднородности являются:
1). увеличение скорости охлаждения ωохл > ωкр (рекомендуется для незакаливающихся сталей);
2). введение в сварочную ванну модификаторов в виде поверхностно-активных веществ, или частиц тугоплавких соединений, служащих центрами кристаллизации;
3). возбуждение в кристаллизующемся сплаве колебаний (механических, электромагнитных);
4). создание благоприятных условий для образования высокотемпературных избыточных фаз типа твердого раствора, или типа эвтектик с включением первичных карбидов;
5). повышение химической частоты исходных сварочных материалов (электрошлаковый переплав, вакуумная плавка и т.п.).
ОСНОВЫМЕТАЛЛУРГИЧЕСКИХ ПРОЦЕССОВ ПРИ СВАРКЕ ПЛАВЛЕНИЕМ
0.23. Газовая фаза в зоне сварки
Физико-химические процессы (диссоциация газов, их растворение в жидком металле, химические реакции в газовой среде и при взаимодействии с металлом) оказывают большое влияние на процесс сварки и качество сварного соединения.
Диссоциация газов происходит при высоких температурах с поглощением тепла
Н2 + 432,5 кДж/моль ⇆ 2Н; (4.1)
О2 + 492 кДж/моль ⇆ 2О; (4.2)
N2 + 709 кДж/моль ⇆ 2N – молекула наиболее прочная. (4.3)
Для оценки диссоциации используют понятие степень диссоциации α – отношение диссоциировавших молекул к их первоначальному числу, которую определяют по уравнениям Нернста.
Задаваясь Т при Р = const определяем константу равновесия Кр, а затем и степень диссоциации α.
Важность диссоциации при сварке:
1) газы в атомарном состоянии более химически активны и легко взаимодействуют с расплавленным металлом капель и сварочной ванны;
2) диссоциация газов в области высоких температур дуги с поглощением тепла идет одновременно с обратным процессом вблизи сварочной ванны с выделением тепла. Т.е. существует перенос тепла.
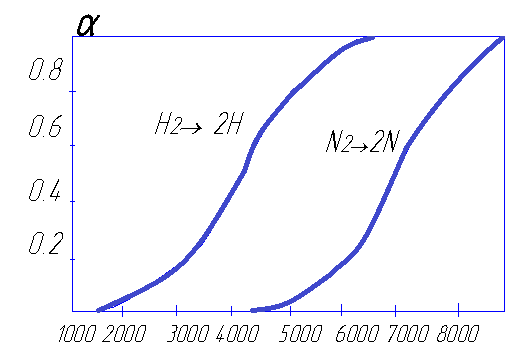
Рис. 4.1. Зависимости степени диссоциации водорода и азота от температуры
Растворение газов в расплавленном металле происходит в каплях и в сварочной ванне, но менее интенсивно, так как:
1) температура ванны ниже температуры капель;
2) отношение поверхности реакции к объему ванны много меньше чем у капель.
Количество растворяющегося газа:
[C]r = a·e-E/kT, (4.4)
где а, k – const;
Е – теплота растворения;
Т – абсолютная температура, К.

Рис. 4.2. Растворимость газов от температуры
Растворимость растет с ростом Т, но при Ткип равна 0.
Стадии растворения:
1) адсорбция атомов газа поверхностью металла;
2) образование растворов и химических соединений в поверхностном слое – хемосорбция;
3) диффузия продуктов хемосорбции вглубь жидкого металла.
Адсорбция и хемосорбция идут мгновенно, а диффузия более замедленно.
0.24. Влияние газов на свойства сталей
0.24.1. Влияние кислорода на свойства стали
Изучение особенностей растворения О, О2 в железе способно раскрыть взаимодействия его со сталью, основой которой является железо.
Железо с кислородом образует три оксида:
2Fe + O2 ↔ 2FeO (закись, содержащая 22,7 % О2) (4.5)
6FeO + O2 ↔ 2Fe3O4 (закись-окись, содержащая 27,64 % О2) (4.6)
4Fe3O4 + O2 ↔ 6Fe2O3 (окись, содержащая 30,06 % О2) (4.7)
Из них только закись FeO растворима в железе и наиболее сильно влияет на его свойства. Остальные оксиды в железе не растворяются, могут присутствовать только в виде включений и легко разлагаются при высоких температурах.
Растворимость кислорода:
при температурах от комнатных до 300° составляет 0,001 %;
при температуре плавления составляет 0,16 %.
Наличие в стали легирующих элементов влияет на растворимость кислорода (С и Si сильно снижают растворимость О2).
Кислород может окислять легирующие элементы:
С + О → СО; (4.8)
Мn + O → MnO; (4.9)
Si + 2O → SiO2. (4.10)
Закись железа может взаимодействовать с легирующими элементами:
FeO + C ↔ CO + Fe; (4.11)
FeO + Mn ↔ Mn + Fe; (4.12)
2Fe O + Si ↔ SiO2 + 2Fe. (4.13)
Кислород в стали ухудшает все свойства: пределы прочности σв и текучести σт, относительное удлинение δ % и ударную вязкость α.
С ростом кислорода:
1) уменьшается стойкость против коррозии;
2) растет склонность к старению;
3) при О2 > 0,08 % возникает хладно и красноломкость;
4) усиливается рост зерен при нагреве;
5) ухудшается обрабатываемость резанием и ковка;
6) понижается магнитная проницаемость и увеличивается электрическое сопротивление.
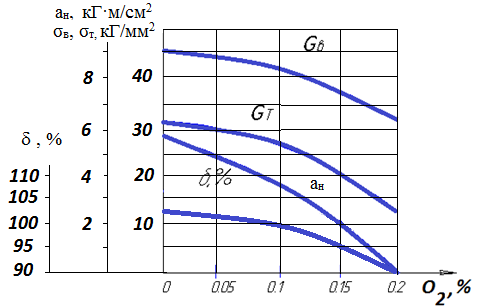
Рис. 4.3. Влияние содержания кислорода на механические свойства м/у стали
0.24.2. Влияние азота на свойства стали
Атомарный азот растворяется в тех металлах, с которыми он может образовывать химические соединения – нитриды. В сталях азот образует нитриды как с железом, так и с большинством примесей. С железом азот дает два нитрида:
4Fe + 1/2N2 ⇆ Fe4N – 11,25 кДж/моль; (4.14)
2 Fe + 1/2N2 ⇆ Fe2N – 16,25 кДж/моль. (4.15)
Нитриды железа образуются в области пониженных температур (700–550оС), при более высоких температурах они диссоциируют.
Азот образует с легирующими элементами нитриды, гораздо более стойкие, чем нитриды железа, особенно нитриды кремния и титана.
Пути насыщения металла азотом:
1) диссоциированный азот непосредственно растворяется в жидком металле, а при понижении температуры образуются нитриды железа;
2) диссоциированный азот образует при высоких температурах стойкие нитриды, которые растворяясь в жидком металле, насыщают его азотом;
3) диссоциированный азот образует при высоких температурах окись азота NO, которая растворяется в каплях. При температурах меньше 1000°С NО выпадает из твердого раствора и диссоциирует, образуя нитриды железа и оксиды.
С увеличением содержания азота:
1) появляется склонность металла к старению;
2) появляется склонность металла к хладно и синеломкости;
3) увеличивается способность к закалке;
4) понижается магнитная проницаемость;
5) увеличивается электросопротивление.
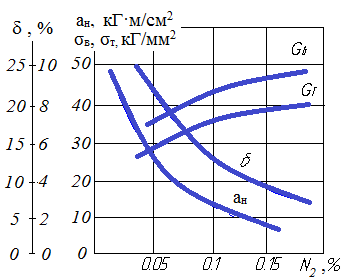
Рис. 4.4. Влияние содержания азота на механические свойства м/у стали
0.24.3. Влияние водорода на свойства стали
Водород может оказывать двоякое действие на металл.
1. Защищает от окисления и насыщения кислородом и азотом; восстанавливает металл из оксидов.
2. Растворяясь в металле, становится причиной пористости и трещин.
Атомарный водород Н растворяется как в твердом, так и особенно сильно в жидком железе. Наиболее значительное насыщение водородом происходит в процессе переноса капель.
Образование в газовой среде соединений ОН и НF, нерастворимых в жидком металле, снижает насыщенность металла водородом.
Находясь в окисленном жидком металле, водород взаимодействуют с кислородом:
2[H] + [H] → H2O ↑, (4.16)
где квадратные скобки означают растворенные в металле элементы;
[H] + [O] → OH ↑ (4.18)
[H]·[O] = const (4.17)
Поэтому наличие в металле кислорода ограничивает концентрацию водорода.
Не успевший выделиться при быстром охлаждении водород задерживается в ветвях дендритов и у поверхностей кристаллов. Здесь атомы воссоединяются в молекулы, парциальное давление атомарного водорода резко снижается, и он продолжает сюда диффундировать. Молекулярный водород создает большие давления, т.к. не растворим в металле, так же как и водяной пар, в который может окислиться водород. В металле возникает объемное напряженное состояние, приводящее к снижению пластических свойств и к хрупкому разрушению.
Особенно опасно наличие водорода в легированных сталях (С, Ni, Mn и др.), увеличивающих его растворимость. Вследствие разновременности полиморфных превращений γ-железа в шве и в основном металле в переходной зоне скапливается водород и возникают трещины.
0.24.4. Влияние окиси углерода на свойства стали
Окись углерода, будучи нерастворимой в жидком металле, прямой опасности не представляет. Наоборот, она способна создать защитную атмосферу у поверхности сварочной ванны.
При взаимодействии углерода с оксидами образующаяся окись углерода приводит к «кипению» металла;
FeO + C ↔ CO↑ + Fe, (4.19)
способствуещему удалению всех посторонних включений. Если в металле шва нет нужных раскислителей (Si, Mn и т.д.), способных подавить «кипение», то может снизиться содержание углерода и образоваться поры.
Карбидообразование железа и других металлов может происходить:
- непосредственно: Ме + С ↔ МеС;
- в атмосфере СО и СО2: Ме + 2СО ↔ МеС + СО2
- в атмосфере углеводородов: Сn Hm + Me ↔ MeC + Cn-1Hm
Карбиды образуют почти все металлы, но они обладают различными свойствами.
1. Карбиды с кубической кристаллической решеткой – наиболее тугоплавкие и устойчивые TiC, ZrC, VC, NbC, T0C, Cr23C6;
2. Карбиды с гексагональной решеткой MoC, W2C, WC, Ni3C, Cr7C2, …;
3. Карбиды с ромбической решеткой Cr3C2, Mo2C, Mn3C, Fe3C.