Качественные реакции
В химии качественные реакции очень важны, с ними тесно связан один из разделов химии - аналитическая химия. Качественные реакции определяют катионы, анионы, порой и целые соединения. Для качественного анализа пригодны не все реакции, а лишь те, которые сопровождаются каким-либо внешним эффектом: выпадением или растворением осадка, изменением окраски анализируемого раствора, выделением газообразных веществ. Такие реакции называют аналитическими.
Аналитическая реакция должна протекать достаточно быстро и полно. При ее выполнении необходимо соблюдать условия, которые определяются свойствами получающегося продукта. Несоблюдение этих условий может привести к неправильным результатам. Одно из условий – среда. Например, осадок AgCl растворим в NH4OH, поэтому он не может быть получен в аммиачной среде.
Другое условие – поддержание необходимой температуры раствора. Большинство аналитических реакций проводят при комнатной температуре или при охлаждении пробирки водой из-под крана. Некоторые реакции требуют нагревания (обнаружение иона NH4+ действием щелочи на исследуемый раствор). Еще одно условие – достаточно высокая концентрация обнаруживаемого иона, если реакция идет в растворе. Здесь необходимо сказать о чувствительности аналитических реакций, которая определяет возможность обнаружения вещества или иона в растворе. Порог чувствительности характеризуют количественно с помощью обнаруживаемого минимума или минимальной концентрации. Обнаруживаемый минимум – это наименьшее количество вещества, которое удается определить с помощью данной реакции. Основным способом повышения чувствительности является концентрирование веществ, которое проводят, упаривая раствор, экстрагируя вещества подходящим растворителем, соосаждая с коллекторами, и другими способами.
Различают специфические и селективные реакции. Селективные, или избирательные, реакции дают сходный внешний эффект с несколькими веществами или ионами. Например, оксалат аммония образует осадки с катионами Са2+, Ва2+, Sr2+. Чем меньше таких ионов, тем более выражена избирательность реакции.
Специфической называют такую реакцию, которая позволяет обнаружить вещество или ион в присутствии других веществ. Специфична реакция йода с крахмалом и некоторые другие. Однако специфических реакций сравнительно немного.
Рассмотрим несколько видов качественных реакций:
Качественные реакции с окрашиванием пламени.
Качественные реакции на катионы щелочных металлов возможно провести только с сухими солями, т.к. практически все соли щелочных металлов растворимы. Обнаружить их можно при внесении небольшого количества соли в пламя горелки. Тот или иной катион окрашивает пламя в соответствующий цвет:
Li+ - темно-розовый; Na+ - желтый; K+, Rb+, Cs+ - фиолетовый;

Качественные реакции с выделением газа.
Можно обнаружить некоторые анионы, добавляя к анализируемой пробе кислоты, если при этом выделяются газы, то по их характеру судят об анионе, входящем в состав вещества. Например, если выделяется H2S, то появляется запах тухлых яиц.
3. Качественные реакции с выпадением осадка.
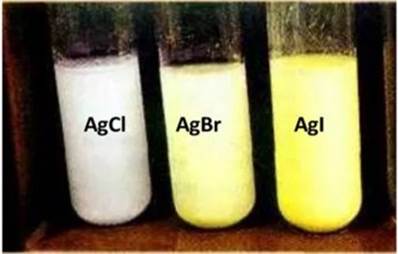
Катионы Ag+ при взаимодействии с растворимыми хлоридами, бромидами и иодидами образуют соответственно осадки определенных цветов: белый – хлорида серебра AgCl, желтоватый – бромида серебра AgBr и желтый – иодида серебра Agl.
4. Качественные реакции с изменением окраски.
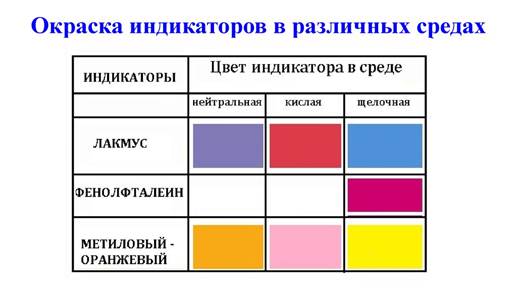
Для качественного обнаружения щелочной или кислой среды часто используется индикаторы — лакмус, фенолфталеин, метиловый оранжевый.
В домашних условиях также можно провести несколько качественных реакций:
1. Качественной реакцией на карбонаты CO32- и гидрокарбонаты HCO3- является их взаимодействие с растворами кислот, при котором выделяется углекислый газ. Процесс сопровождается характерным вскипанием.
Для проведения реакции насыпьте столовую ложку пищевой или кальцинированной соды (NaHCO3, Na2CO3) на блюдце. Сверху тонкой струйкой полейте порошок соды раствором уксусной кислоты (CH3COOH).
NaHCO3 + CH3COOH = CH3COONa + CO2↑ + H2O
Наличие соды в порошковых чистящих и моющих средствах также можно определить по характерному вскипанию при добавлении к ним уксуса.
2. Качественной реакцией на крахмал является появление характерного окрашивания при его взаимодействии с йодом.
Крахмал содержится во многих пищевых продуктах: хлебобулочных изделиях, картофеле, рисе и пр.
Можно капнуть спиртовой раствор йода на кусочек свежего хлеба или в воду, оставшуюся после промывания риса или чищеного картофеля.
Домашнее задание:
1. Где и для чего используются качественные реакции?
2. В какой цвет окрашивают пламя ионы натрия?
3. В какой цвет окраситься вода (нейтральная среда) при добавлении к ней раствора лакмуса?
4. Проведите дома одну из приведенных выше качественных реакций.
5. Укажите, какой цвет появляется при взаимодействии раствора крахмала с йодом.