Для металлов характерно свойство восстановления. Реакции с галогенами и кислородом воздуха протекают с различными скоростями и при различных температурах с разными металлами. Так, щелочные металлы легко окисляются кислородом воздуха и взаимодействуют с простыми веществами, железо и медь взаимодействуют с простыми веществами только при нагревании, золото и платиновые металлы не окисляются вообще. Многие металлы образуют на поверхности оксидную пленку, которая защищает их от дальнейшего окисления.



Менее энергично металлы взаимодействуют с серой:

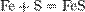
Трудно вступают в реакцию с азотом и фосфором:
 (нитрид магния)
(нитрид магния)
 (фосфид кальция)
(фосфид кальция)
Активные металлы взаимодействуют с водородом:
 (гидрид кальция)
(гидрид кальция)
Взаимодействие с водой:
Активные металлы (щелочные металлы) взаимодействуют с водой при обычных условиях с образованием гидроксидов и выделением водорода:


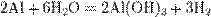
Билет №8
Реакция ионного обмена — одна из видов химической реакции, характеризующаяся выделением в продукты реакции воды,газа или осадка.
Реакцию обмена в растворе принято изображать тремя уравнениями: молекулярным, полным ионным и сокращённым ионным. В ионном уравнении слабые электролиты, газы и малорастворимые вещества изображают молекулярными формулами.
Na2CO3 + H2SO4 → Na2SO4 + CO2↑ +H2O
2Na+ + CO32- + 2H+ + SO42- → 2Na+ + SO42- + CO2↑ + H2O
CO32- + 2H+ → CO2↑ + H2O
Условия необратимости реакций ионного обмена
1. Если образуется осадок (¯) (смотри таблицу растворимости)
Pb(NO3)2 + 2KI ® PbI2¯ + 2KNO3
Pb2+ + 2I- ® PbI2¯
2. Если выделяется газ ()
Na2CO3 + H2SO4 ® Na2SO4 + H2O + CO2
CO32- + 2H+ ® H2O + CO2
3. Если образуется малодиссоциированное вещество (H2O)
Ca(OH)2 + 2HNO3 ® Ca(NO3)2 + 2H2O
H+ + OH- ® H2O
4. Если образуются комплексные соединения (малодиссоциированные комплексные ионы)
CuSO4 • 5H2O + 4NH3 ® [Cu(NH3)4]SO4 + 5H2O
Cu2+ + 4NH3 ® [Cu(NH3)4]2+
В тех случаях, когда нет ионов, которые могут связываться между собой с образованием осадка, газа, малодиссоциированных соединений (H2O) или комплексных ионов реакции обмена обратимы «.
Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Простейшие представители (одноядерные арены):

Многоядерные арены: нафталин С10Н8, антрацен С14Н10 и др.

Термин "ароматические соединения" возник давно в связи с тем, что некоторые представители этого ряда веществ имеют приятный запах. Однако в настоящее время в понятие "ароматичность" вкладывается совершенно иной смысл.
Бензо́л (C6H6, PhH) — органическое химическое соединение, бесцветная жидкость с приятным сладковатымзапахом. Простейший ароматический углеводород. Бензол входит в состав бензина, широко применяется впромышленности, является исходным сырьём для производства лекарств, различных пластмасс, синтетической резины, красителей. Хотя бензол входит в состав сырой нефти, в промышленных масштабах он синтезируется из других её компонентов. Токсичен,канцерогенен.
Физические свойства
Бесцветная жидкость со своеобразным резким запахом
Подобно всем углеводородам бензол горит сильно коптящим пламенем. С воздухом образует взрывоопасные смеси, хорошо смешивается сэфирами, бензином и другими органическими растворителями, с водой образует азеотропную смесь с температурой кипения 69,25 °C (91 % бензола).
Химические свойства
Для бензола характерны реакции замещения — бензол реагирует с алкенами, хлоралканами, галогенами, азотной и серной кислотами. Реакции разрыва бензольного кольца проходят в жёстких условиях (температура, давление).
Взаимодействие с хлором в присутствии катализатора:
С6H6 + Cl2 -(FeCl3)→ С6H5Cl + HCl образуется хлорбензол
Взаимодействие с бромом (чистый):
С6H6 + Br2 -(FeBr3 или AlCl3)→ С6H5Br + HBr образуется бромбензол
Взаимодействие с галогенопроизводными алканов (алкилирование бензола, реакция Фриделя-Крафтса):
С6H6 + С2H5Cl -(AlCl3)→ С6H5С2H5 + HCl образуется этилбензол
С6H6 + HNO3 -(H2SO4)→ С6H5NO2 + H2O
Применение
Значительная часть получаемого бензола используется для синтеза других продуктов:
около 50 % бензола превращают в этилбензол (алкилирование бензола этиленом);
около 25 % бензола превращают в кумол (алкилирование бензола пропиленом);
приблизительно 10—15 % бензола гидрируют в циклогексан;
около 10 % бензола расходуется на производство нитробензола;
2—3 % бензола превращают в линейные алкилбензолы;
приблизительно 1 % бензола используется для синтеза хлорбензола.
Получение H2
Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную серную кислоту:
Zn + H2SO4 → ZnSO4 + H2↑
Взаимодействие кальция с водой:
Ca + 2H2O → Ca(OH)2 + H2↑
Гидролиз гидридов:
NaH + H2O → NaOH + H2↑
Действие щелочей на цинк или алюминий:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
Zn + 2KOH + 2H2O → K2[Zn(OH)4] + H2↑
С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:
2H3O+ + 2e− → H2↑ + 2H2O
Распознование ЛУЧИНА
Получение O2
ислород (O2) в лаборатории получают разложением перманганата калия KMnO4 (марганцовки). Для опыта понадобится пробирка с газоотводной трубкой. В пробирку насыпаем кристаллический перманганат калия. Для сбора кислорода приготовим колбу. При нагревании перманганат калия начинает разлагаться, выделяющийся кислород поступает по газоотводной трубке в колбу. Кислород тяжелее воздуха, поэтому не покидает колбу и постепенно заполняет ее. Тлеющая лучинка вспыхивает в колбе: значит нам удалось собрать кислород.
2 KMnO4 = K2MnO4 + MnO2 + O2 ↑
2Na2O2 + 2CO2 = 2Na2CO3 + O2↑
4KO2 + 2CO2 = 2K2CO3 + 3O2↑
Распознование ЛУЧИНА
Получение co2
Получим углекислый газ (CO2 ) при взаимодействии разбавленной соляной кислоты и карбоната кальция - мрамора.
СаCO3 + 2HCl = CaCl2 + CO2 ↑х +H2O
По трубке углекислый газ CO2 подается в стакан с известковой водой (это раствор гидроксида кальция Ca(OH)2). Небольшое количество поступающего в раствор углекислого газа взаимодействует с водой с образованием слабой угольной кислоты.
CO2 + H2O ↔ H2CO3
H2CO3 + Ca(OH)2 = CaCO3 ↓ + 2H2O