Физико-химические основы процесса.
Термодинамика окисления диоксида серы.
Реакция окисления диоксида серы в триоксид
2SO2 + O2 SO3
обратима и степень окисления газа любого состава строго определяется температурой и парциальными давлениями компонентов реакции[2]:
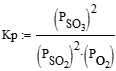

Уравнения для расчета теплового эффекта и константы равновесия реакции для интервала температур 400 – 625 и 650 0С имеют следующий вид:
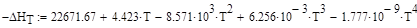
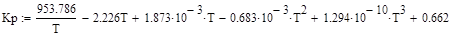
Для технических расчетов может быть использовано уравнение:
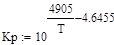
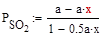

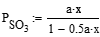

Количество окисленного SO2 характеризуют долей общего содержания диоксида серы (сернистого ангидрида) в газе или в % (к общему первоначальному количеству SO2 в газе). Максимальная степень превращения диоксида серы в триоксид при заданных условиях (температуре, давлении, исходных концентрациях реагирующих компонентов) достигается в условиях равновесия. Для состояния равновесия с учетом уменьшения объема газовой смеси при протекании реакции выражения для парциальных давлений компонентов смеси принимают вид (выражение справедливо при общем давлении 1 атм): где a и b – исходные парциальные давления диоксида серы и кислорода, хр – равновесная степень превращения.
Уравнение, в неявном виде определяющее степень превращения:
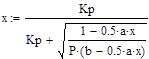
Катализаторы окисления диоксида серы.
В производстве серной кислоты контактным методом окисление SO2 происходит в присутствии катализатора. Для этого газ приводят в соприкосновение с катализатором, находящимся в стационарном или «кипящем» состоянии. Способностью ускорять окисление диоксида серы обладают различные металлы, их сплавы и окислы, некоторые соли, силикаты и многие другие вещества и материалы. Каждый катализатор обеспечивает определенную, характерную для него степень превращения. В заводских условиях выгоднее пользоваться катализаторами, при помощи которых достигается возможно более высокая степень превращения, так как остаточное количество неокисленного SO2 не улавливается в абсорбционном отделении, а удаляется в атмосферу вместе с отходящими газами[3]. Для утилизации выбросов SO2 в настоящее время используются различные технологии, например, технология компании "HALDOR TOPSOE". (Каталитический процесс WSA - производство серной кислоты из влажного газа, позволяющий регенерировать сернистый ангидрид независимо от его концентрации в технологических газах; основные характеристики: полная автоматизация процесса, возможность использования тепла реакции окисления сернистого ангидрида для получения товарного пара и полная экологическая чистота).
Длительное время лучшим катализатором считался платиновый, однако с 1932 г. его вытеснили ванадиевые. До конца 70-х гг. применялся катализатор БАВ (контактная масса, состоящая их бария, алюминия, ванадия). Чистый пятиоксид ванадия обладает слабой каталитической активностью, резко возрастающей в присутствии солей щелочных металлов. Применяется катализатор СВД (сульфо-ванадато-диатомовая контактная масса), изготавливающийся путем смешения кремнеземистого носителя – диатомита с содержанием не более 3% Al2O3, тонко измолотого пятиоксида ванадия и раствора KHSO4, последующего гранулирования и прокаливания гранул.
Стремление повысить активность при низких температурах привело к разработке катализатора СВС и катализатора Института катализа (ныне Институт катализа им. Г. К. Борескова СО РАН). Они производятся с использованием в качестве носителя охлажденного силикагеля при применении гидратированного пятиоксида ванадия по несколько отличающимся между собой технологическим схемам. Применение этих катализаторов при концентрации газа 8 – 9% SO2 позволяет снизить температуру на входе в I катализатора до 405 – 410 0С. Там же были разработаны катализаторы ИК-1-6, МСВ – с малым содержанием ванадия. Сейчас для окисления сернистого ангидрида в серный в производстве серной кислоты применяются катализаторы ИК-1-6М, также разработанные Институтом катализа. (ИК-1-6М - семейство новых катализаторов, являющихся модернизированными аналогами катализатора ИК-1-6; работают в широком диапазоне температур - от 380 до 640 °С в системах одинарного и двойного контактирования, а также в аппаратах нестационарного окисления SO2)[4]. Для переработки газов повышенной концентрации (10 – 11% SO2) был разработан катализатор ТС (термостабильный), более устойчивый к термической инактивации, чем СВД. В качестве носителя используется модифицированный диатомит. Также применяют шариковый износоустойчивый катализатор для работы во взвешенном слое, разработанный в ЛТИ (СПбГТИ (ТУ)). Его получают пропиткой растворами ванадата и сульфата калия шарикового алюмосиликагеля с определенным содержанием Al2O3 и последующей термообработкой, при которой, в зависимости от температуры и содержании вводимого KNO3, создается определенная пористая структура. Для переработки газов с повышенной концентрацией SO2 и под давлением были созданы ванадиевые катализаторы, обладающие повышенной термостабильностью или повышенной температурой зажигания. Существует трубчатый катализатор СВД с пониженным гидравлическим сопротивлением. Иностранные фирмы – поставщики катализаторов для серной кислоты: BASF (ФРГ), Monsanto Environmental Chemical Systems (США), American Cyanamid Co (США), Catalyst and Chemicals Inc (США), Haldor Topsoe (Дания), Saint Gobein and Krebs (Франция), Kemira (Финляндия) и др.
Механизм и кинетика окисления серы [5].
Катализаторы окисления диоксида серы в триоксид имеют различный состав. Так, в СВД установлено присутствие трех соединений: 3K2S2O7*V2O5, 2K2S2O7*V2O5 и K2S2O7*V2O5, разлагающихся при температурах соответственно 315 – 330, 365 – 380 и 405 – 400 0С. Активный компонент ванадиевых катализаторов в температурной области их применения находится в расплавленном состоянии, возникает специфическая особенность в механизме их действия. Катализаторы работают как абсорбционные и процесс окисления протекает внутри слоя активного компонента. В области высоких значений поверхности реакция протекает во всем объеме расплава вследствие его малой величины, со снижением поверхности катализатора толщина пленки расплава увеличивается и скорость реакции лимитируется диффузией газообразных компонентов в объеме расплава.
Схема процесса может быть сформулирована следующим образом:
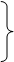 |
1) 2V5+ + O2- + SO2 2V4+ + SO3
2) 2V4+ + 1/2O2 2V5+ + O2- А
В первой стадии достигается равновесие, вторая стадия является медленной и определяет скорость процесса.
В области температур выше 4200С скорость каталитической реакции много больше скорости восстановления катализатора. В связи с этим вероятен механизм, в котором процесс протекает по пути, не связанному с изменением валентного состояния ванадия. Схема такого процесса:
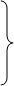 1) V2O5*nSO3 + SO2 V2O5*(n - 1)SO3*SO2 + SO3
1) V2O5*nSO3 + SO2 V2O5*(n - 1)SO3*SO2 + SO3
2) V2O5*(n - 1)SO3*O2 V2O4*nSO3 Б
3) V2O5*(n - 1)SO3*SO2 + O2 + SO2 V2O5*nSO3 + SO3
В случае Б скорость каталитической реакции пропорциональна доле активного компонента в окисленной форме. По этому механизму реакция протекает в присутствии триоксида серы в газовой фазе.
Скорости окисления ванадия (IV) кислородом и каталитической реакции в присутствии SO3 близки и при малых степенях превращения процесс протекает по окислительно-восстановительному механизму, который может быть представлен схемой:
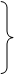 1) V2O4*nSO3 V2O4*(n - 2)SO3 + 2SO2
1) V2O4*nSO3 V2O4*(n - 2)SO3 + 2SO2
2) V2O4*(n - 2)O3 + 1/2O2 V2O5*(n - 2)SO3 В
3) V2O5*(n - 2)SO3 + SO2 + SO3 V2O4*nSO3
Скорость реакции определяет стадия (2).
Таким образом, кинетические закономерности достаточно сложны.
На скорость реакции влияет также внутренняя диффузия. В реальных условиях контактного процесса влияние внешнедиффузионных факторов составляет менее 3%. Диффузионное сопротивление уменьшается с ростом массовой скорости газового потока при высоких парциальных давлениях реагентов, при малых значениях скоростей реакции и размера зерна катализатора.
Влияние давления на процесс окисления диоксида серы.
Повышение давления влияет как на скорость процесса, так и на состояние равновесия. Скорость реакции и выход продукта с повышением давления увеличиваются за счет повышения действующих концентраций SO2 и O2 и увеличения движущей силы процесса. Начальная температура (температура газа на входе в I слой катализатора) понижается с увеличением давления.
Температура газа на входе в I слой:
| Давление, МПа | Концентрация SO2, % | |||
| 0,5 | ||||
| 0,7 | ||||
| 1,0 |
Значения температур, соответствующих равновесной степени превращения 0,998 при давлении в системе 1,0 МПа:
| Сso2, % | |||||
| t, 0C |
Технологическое оформление процесса окисления диоксида серы.
Технологическая схема и аппаратура контактного узла зависит от вида применяемого сырья, способов отвода тепла реакции, производительности установки и других факторов.
На рис. представлена схема контактного узла с одинарным контактированием, включая 4-слойный аппарат с промежуточными теплообменниками. Очищенный и осушенный сернистый газ подается газодувкой, нагревается во внешнем и промежуточных теплообменниках и поступает на I слой контактного аппарата. Пройдя все слои катализатора с промежуточным охлаждением в теплообменниках, прореагировавший газ покидает контактный аппарат, охлаждается во внешних теплообменниках и поступает на абсорбцию образовавшегося SO3. оптимальный температурный режим поддерживается с помощью байпасных газоходов с задвижками на теплообменниках, которые обычно устанавливают последовательно по ходу газа, иногда – параллельно перед двумя последними слоями. Максимальная степень превращения в контактном аппарате 98,0 – 98,5%.
При двойном контактировании после первой стадии катализа из газовой смеси поглощается образовавшийся SO3 и на вторую стадию катализа поступает неокисленная часть исходного SO2. Степень превращения 99,5 – 99,8%.
В современном сернокислотном производстве наиболее широко применяются контактные аппараты с горизонтальными стационарными слоями катализатора и отводом тепла в выносных теплообменниках. Применяются также контактные аппараты с внутренними теплообменниками либо с поддувом воздуха или газа.
При работе по короткой схеме на газах от сжигания серы или сероводорода применяется охлаждение газа между слоями в пароперегревателях, в газовоздушных теплообменниках или поддувом воздуха, что значительно упрощает конструкцию контактного узла.
Для устойчивой работы контактного аппарата необходимо равномерное распределение газа и температур по сечению аппарата, достаточная мощность теплообменников, надежная схема регулирования, простота обслуживании и ремонта и др. Наибольшая равномерность температур и концентраций газа в аппарате достигнута при использовании выносных теплообменников.
Использование аппарата ОТС – с отводом тепла серой позволяет путем использования высокотемпературного теплоносителя увеличить степень конверсии по сравнению с традиционными методами конверсии на 1,5 – 1,8% вследствие снижения градиента температур между стенками трубок и серединой слоя. Рабочая температура охлаждающего агента в ОТС совпадает с температурой зажигания катализатора, что позволяет исключить возможность инактивации катализатора при возрастании скорости газов. При этом в два раза меньше, чем у ПНР, расход металла.
Также используются кассетные аппараты (катализатор помещен в кассеты из проволоки).
По условиям осуществления процесса окисления SO2 и принципу теплоотвода контактные аппараты можно разделить на:
аппараты со стационарными слоями катализатора и промежуточным теплообменом (наиболее широко применяемые);
аппараты со стационарными слоями катализатора и непрерывным теплообменом;
аппараты с кипящими слоями катализатора и непрерывным теплообменом;
аппараты с нестационарным режимом окисления и теплоотвода в слоях катализатора.