Номенклатура.
1 способ: называется по кислотам и спиртам, входящим в их состав.
CH3COOCH3 – метиловый эфир уксусной кислоты. Уксусно-метиловый эфир
C3H7COOC2H5 – этиловый эфир бутановой (масляной) кислоты. Масляно-этиловый эфир.
2 способ: по заместительной номенклатуре: к названию углеводородного радикала добавляется систематическое название карбоновой кислоты, суффикс «овая» кислота замещается на суффикс «оат»
HCOOCH3 -метилформиат
CH3COOCH3 – метилацетат
CH3COOC8H17 — н-октилацетт
( CH3)2CHCH2COOCH2CH2CH(CH3)2 —изоамилизовалерат (изопентилизовалерат) имеет запах яблока.
HCOOCH2C6H5 — бензилформиат; имеет запах жасмина;
HCOOCH2CH2C6H5 — 2-фенилэтилформиат имеет запах хризантем.
Изомерия. Характерна структурная изомерия спиртовых и кислотных радикалов.
ЭCH3COOCH(CH3)2 --физопропилацетат ----
CH3COOC3H7 ---- пропилацетатат
Физические свойства
Сложные эфиры низших и средних гомологов спиртов и кислот - это бесцветные жидкости, легче воды, летучи. Низкомолекулярные эфиры растворимы в воде и органических растворителях. Многие из них обладают специфическим приятным запахом. Например:
- 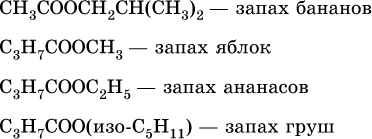 кислоты
кислоты
Способы получения
Термин «эфир» впервые применил к синтетическим веществам Карл Вильгельм Шееле (1742-1786) в 1782 г. Он указал, что исходными веществами для их получения служат карбоновые кислоты и спирты, а в качестве катализатора используется минеральная серная кислота. Прошло более 200 лет, а способ получения сложных эфиров в принципе не изменился.
1.Этерификация — взаимодействие кислот и спиртов в присутствии конц. серной кислоты, например получение этилацетата из уксусной кислоты и этилового спирта:
СН3COOH + C2H5OH ↔ СН3COOC2H5 + H2O
Реакции этерификации обратимы, сдвиг равновесия в сторону образования целевых продуктов достигается удалением одного из продуктов из реакционной смеси (чаще всего — отгонкой более летучих спирта, эфира, кислоты или воды)
2.Взаимодействие ангидридов или галогенангидридов карбоновых кислот со спиртами, например получение этилацетата из уксусного ангидрида и этилового спирта:
(CH3CO)2O + 2 C2H5OH→2 СН3COOC2H5 + H2O
3.Взаимодействие солей кислот с алкилгалогенидами
CH3 COONa + C3H7 Cl →CH3 COO C3H7 + NaCl
4.Присоединение спиртов к алкенам в условиях кислотного катализа
(в присутствии кислот Льюиса):
RCOOH + R'CH=CHR'' → RCOOCHR'CH2R''
СН3COOH + C2H5CH=CHC3H7 →СН3COO CH (C2H5)CH2C3H7
Химические свойства.
1.Гидролиз сложных эфиров - реакция обратная этерификации. Протекает в кислой (обратимо) или щелочной (необратимо) среде.
В результате кислотного гидролиза бензилформиата образуются муравьиная кислота и бензиловый спирт.
HCOOCH2C6H5 + H2O ↔HCOOH +H OCH2C6H5
В результате щелочного гидролиза образуются спирт и соль карбоновой кислоты.
2.Восстановление. Сложные эфиры чаще восстанавливают в соответствующие первичные спирты, реже в альдегиды или простые эфиры. Обычно для восстановления используют алюмогидрид лития:
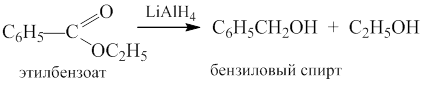
3. Образование амидов кислот под действием аммиака.
CH3COOC2H5+ HNH2 → CH3CO NH2 + HOC2H5
Амид уксусной кислоты этанол
Сложные эфиры глицерина. Жиры (триациалглицериды) – сложные эфиры глицерина и высших карбоновых кислот.
Наибольшее значение имеют сложные эфиры жирных (высших) карбоновых кислот. Для высших карбоновых кислот – характерны следующие основные особенности: имеют неразветвленную структуру с четным числом атомов углерода, чаще всего встречаются кислоты состава С16, С18 и С20;
ненасыщенные кислоты, как правило, содержат двойную связь в положении 9;если двойных связей несколько, то они разделены группой СН2;
двойные связи в ненасыщенных кислотах имеют цис-конфигурацию.
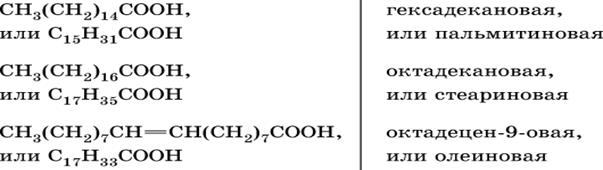
Общая формула жиров
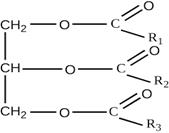
Глицерин, как многоатомный спирт образует полные и неполные эфиры: моноацилглицерины, диацилглицерины, триацилглицерины.
В зависимости от состава сложные эфиры могут быть простыми (содержат остатки одинаковых кислот) и смешанными (содержат остатки разных кислот). Например, смешанный жир, содержит остатки пальмитиновой, стеариновой и олеиновой кислот:

Природные жиры не являются индивидуальными соединениями, а представляют собой разнообразную смесь глицеридов: смесь полных сложных эфиров глицерина и высших карбоновых кислот, а также до 5% свободных жирных кислот, моно - диацилглицеринов и других веществ.
Строение жиров было установлено в начале XIX века французским химиком Шеврелем на основании их гидролиза. В 1854 году Бертло подтвердил синтезом жира из глицерина и смеси кислот:
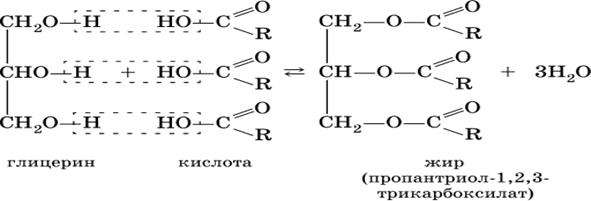
Номенклатура. 1. Способ. Названия жиров образованы из названий кислотных остатков и слова глицерина
| Кислота | Название | Кислотный остаток |
| C15 H31 COOH | пальмитиновая | Пальмитоил |
| C17 H35 COOH | Стеариновая | Стеароил |
| C17 H33 COOH | Олеиновая | Олеоил |
| C17 H31 COOH | Линолевая | Линолоил |
| C17 H29 COOH | линоленовая | линоленоил |
Например: 1,2,3 –трипальмитоил глицерина (трипальмитин)
3-пальмитоил-1,2- дистеароил глицерина.
Физические свойства.
Триацилглицериды, содержащие преимущественно остатки ненасыщенных кислот, при обычных условиях являются жидкостями, насыщенных кислот – твердыми веществами. Животные жиры содержат в основном триацилглицериды с остатками насыщенных кислот и поэтому имеют твердую консистенцию. Растительные масла включают в основном остатки ненасыщенных кислот и являются жидкостями.Жиры легче воды, в воде не растворяются, хорошо растворимы в органических растворителях. Как и любая смесь не имеют четкой температуры плавления. Основная биологическая функция триацилглицеридов – запасные вещества животных и растений.
Химические свойства.
Химические свойства триацилглицеридов определяются наличием сложноэфирной и непредельных связей.
Как сложные эфиры триацилглицериды гидролизуются под действием кислот, ферментов и щелочей: 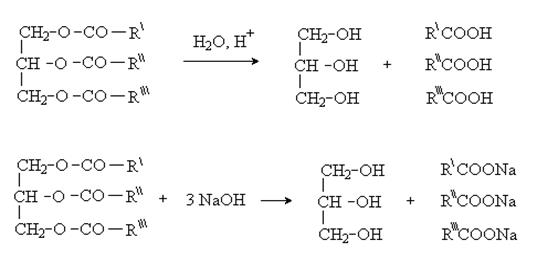
При кислотном гидролизе жиров освобождаются кислоты и появляется неприятный запах и вкус.
При щелочном гидролизе (омылении) жиров образуются соли жирных кислот (мыла-стеарат и пальмитат натрия). Их молекулы дифильны (содержат полярную “голову” и неполярный “хвост”), что обуславливает их повехностно-активные свойства и моющее действие.
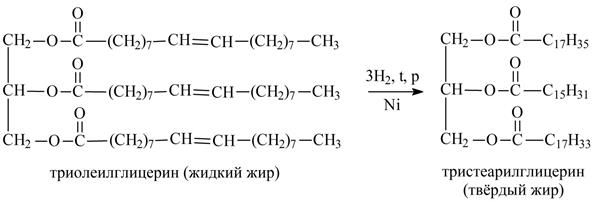
2.Гидрогенизация жиров – каталитическое гидрирование растительных масел, в результате которого водород насыщает двойные связи, и жидкие масла превращаются в твердые жиры (маргарин). В процессе гидрогенизации происходит также изомеризация – перемещение двойных связей (при этом из полиненасыщенных кислот образуются кислоты с реакционноспособными, в том числе и в реакциях окисления, сопряженными двойными связями) и изменение их стереохимической конфигурации (цис в транс), а также частичное расщепление сложноэфирных связей. Существует мнение, что при этом образуются вещества небезопасные для организма.
Окисление (прогоркание жиров).
Триацилглицериды, содержащие остатки ненасыщенных кислот под действием кислорода воздуха и света окисляются по месту двойной связи. Это приводит к разрыву связи и образованию в качестве продуктов окисления смеси альдегидов и карбоновых кислот с более короткой цепью. Появление таких веществ обуславливает неприятный запах и горький вкус жиров.
CH3-(CH2)4-CH= CH-CH2-CH=CH-(CH2)7-COOH →
CH3-(CH2)4-COH + HOC-CH2-COH +HOC-(CH2)7-COOH→
Смесь альдегидов
CH3-(CH2)4-COOH + HOOC-CH2-COOH +HOOC- (CH2)7 –COOH
Гексановая к-та пропандиовая нонандиовая к-та
Окислительные процессы замедляются при уменьшении доступа воздуха и в темноте. Поэтому лекарства на жировой основе хранят в темноте и в прохладном месте, в плотно закрытой таре.
Применение.
В конце XIX — начале ХХ века было синтезировано и испытано фармакологами множество сложных эфиров. Они стали основой таких лекарственных средств, как салол, валидол и др. Как местнораздражающее и обезболивающее средство широко использовался метилсалицилат, в настоящее время практически вытесненный более эффективными средствами.
МАСЛО КАКАО Buturum Cacao – суппозиторная основа. Т плав.= 32-360С. Треть всех жиров, содержащихся в масле какао приходится, на долю стеариновой кислоты, которая не приводит к повышению уровня холестерина. Другая треть на долю мононенасыщенной олеиновой к-ты, которая уменьшает содержание холестерина. Масло какао имеет заживляющее и тонизирующее действие, так как содержит: метилксантины, кофеин, танин. Используется при лечении ожогов, кашля, простудных заболеваний.
МАСЛО КАСТОРОВОЕ Oleum Ricini – смесь триглицеридов линолевой, олеиновой ирицинолевой (одноосновная ненасыщенная оксикислота C17H32(OH)COOH) - внутрь, как слабительное, смягчения кожи, удаления перхоти, в состав линимента бальзамического по Вишневскому.
МАСЛО ЛЬНЯНОЕ – наружно при поражениях кожи,
РАСТИТЕЛЬНЫЕ ЖИРЫ(персиковое и др.) – растворители,
ЛИНЕТОЛ - наружно при ожогах и лучевых поражениях кожи, внутрь для профилактики и лечении атеросклероза.
Составить конспект и ответить на вопросы:
1. Напишите реакцию образования амида из этилового эфира α-метилвалериановой кислоты.
2. Напишите реакцию восстановления маслянопропилового эфира.
3. Какими кислотами образован приведенный компонент жира? Какова его консистенция и почему? Назовите его.
СН2О-СО-С17Н33
│
СНО-СО-С17Н31
│
СН2О-СО-С17Н29
4. Напишите схему реакции окисления линолевой кислоты. Назовите полученные продукты.
5. Напишите реакцию гидролиза триацилглицерина
СН2О-СО-С15Н31
│
СНО-СО-С17Н33
│
СН2О-СО-С17Н35
раствором гидроксида натрия и назовите полученные продукты.