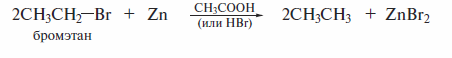Предельные углеводороды
Глава «Алканы» является первой во всех курсах органической химии. Для этого имеются объективные причины, среди которых особо следует выделить следующие. Алканы, находящиеся в природе в составе природного газа, нефти, среди продуктов биологического разложения растительных остатков, являются одним из основных сырьевых источников органического синтеза. Трансформация алканов введением в их молекулы разнообразных функциональных групп и последующие превращения дают химикам возможность получать самые различные органические соединения.
Кроме того (и это также подчеркивает важность алканов как ключевого класса органических соединений), названия алканов лежат в основе номенклатуры органических соединений, поскольку их фрагменты присутствуют в большинстве органических молекул.
Номенклатура и изомерия
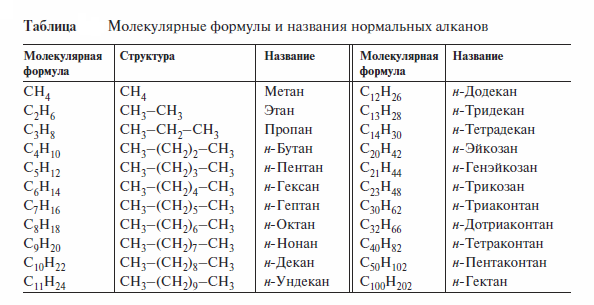
Ациклические углеводороды линейного или разветвленного строения, содержащие только простые связи и образующие гомологический ряд обшей формулы CnH2n + 2 называют алканами. В таблице даны формулы и названия некоторых неразветвленных (нормальных) алканов (название любого предельного углеводорода характеризуется окончанием «ан»).
Молекулы нормальных алканов, перечисленных в табл., имеют линейное строение и содержат только первичные и вторичные атомы углерода.
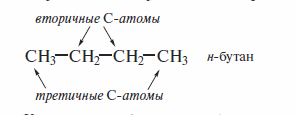
Как видно из формулы н-бутана, первичный атом углерода имеет лишь один соседний С-атом, а вторичный — два соседних атома углерода.
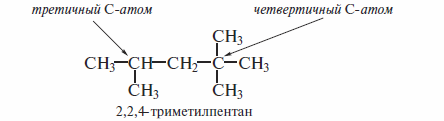
Молекулы и зоалканов содержат, кроме первичных и вторичных, еще и третичные и (или) четвертичные атомы углерода. Третичный атом углерода связан с тремя С-атомами, а четвертичный — с четырьмя атомами углерода.
|
|
Ниже даны примеры названий по номенклатуре ИЮПАК ряда разветвленных алканов.
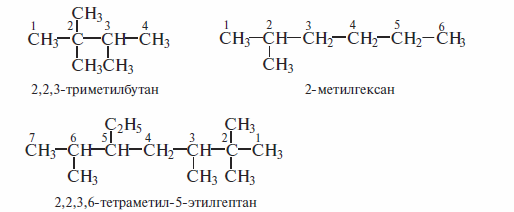
На примере даже средних (С5—С8) алканов видно, что традиционные (полные) структурные формулы весьма громоздки при изображении сложных молекул. В настоящее время предложено несколько упрощенных модификаций структурных формул.
В сжатой структурной формуле обозначение некоторых или всех кова-лентных связей опускают, а идентичные группы, связанные с каким-либо из атомов, записывают в скобках, указывая число этих групп. При этом обычно принято писать заместители, стоящие при углеродном атоме, справа от этого атома.
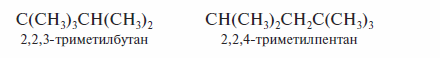
Еще большим упрощением является формула углеродного остова, в которой в виде символов записывают только атомы, отличные отуглерода иводорода (атомы водорода в составе функциональных групп также изображают).
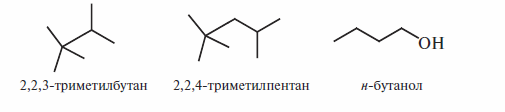
Источники алканов
Природный газ и нефть в настоящее время являются основными источниками алканов в промышленности.
Природный газ особенно богат метаном (до 98%). Газообразные алканы встречаются также в местах нефтяных отложений (попутный газ). Содержание метана в попутном газе достигает 75—85%. В заметных количествах в попутном газе присутствуют также этан и пропан.
Нефть представляет собой жидкую смесь нескольких сотен углеводородов, половина из которых — алканы и циклоалканы.
Методы синтеза
Восстановление галогеналканов
В некоторых случаях восстановление галогеналканов действием цинка в водной минеральной или уксусной кислоте является удобным лабораторным способом получения алканов: