2. Нитрование азотной кислотой в среде инертного органического растворителя позволяет:
- Уменьшить окислительное действие азотной кислотой за счет того, что растворитель подбирают таким образом, чтобы в нем растворялись исходные вещества, и не растворялся продукт реакции.
- Регулировать концентрацию нитроний-катиона, а, следовательно, и скорость реакции полярностью и количеством растворителя. Чем полярнее растворитель, тем быстрее идет реакция.
- Катализировать процесс добавлением небольших количеств сильных кислот. Например, добавка 0,001 моль/л H2SO4 увеличивает скорость нитрования бензола в нитрометане в 2 раза, а 0,01 – в 30 раз.
Необходимо также учитывать что:
- Соли азотной кислоты (например, KNO3) замедляют нитрование (аналогично тому, как соли серной кислоты замедляют сульфирование).
- Многие растворители, явно не реагирующие с азотной кислотой, образуют с последней комплексные соединения, например, диэтиловый эфир, диоксан, дихлорэтан, метиленхлорид. Четыреххлористый углерод и хлороформ с азотной кислотой практически не взаимодействуют.
Скорость реакции, протекающей в кинетической области в полярных средах, где концентрация нитроний-катиона высока, пропорциональна как концентрации субстрата, так и концентрации реагента. Однако в инертном растворителе в случае реакционноспособных соединений лимитирующей стадией является образование нитроний-катиона и скорость реакции не зависит от концентрации нитруемого вещества. Для малоактивных соединений в этих же условиях определяющей скорость стадией будет опять же взаимодействие субстрата с нитроний-катионом.
Нитрование концентрированной азотной кислотой с азеотропной отгонкой воды из реакционной массы идет при температуре кипения азеотропной смеси и постоянной концентрации электрофила, т. к. образующаяся в процессе реакции вода удаляется. Нитрование проводится минимально необходимым количеством азотной кислоты.
VI. Нитрование смесью азотной и уксусной кислот
Достоинства метода: 1) низкая окислительная активность реагентов, 2) легко регулируется нитрующая активность реагентов, поэтому можно нитровать активированные арены, 3) нитрование в среде уксусной кислоты более селективно, чем в среде серной кислоты, и позволяет увеличить выход нитросоединения, не повышая температуру реакции.
Этим методом нитруют активные арены: производные бензола (например, фенол, гидроксибензальдегид, салициловую кислоту), производные нафталина (гидроксинафтойную кислоту), антрацен и другие.

Ароматические амины, для предотвращения побочных реакций по аминогруппе,нитруют в присутствии уксусного ангидрида, при этом сначала проходит ацилирование аминогруппы, а затем нитрование ацетанилида. Для предотвращения нитрозирования примесь азотистой кислоты снимают мочевиной:
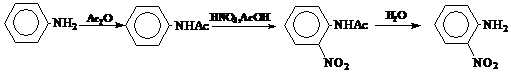

При получении нитроанилина анилин обрабатывают смесью уксусной кислоты и уксусного ангидрида, а затем к полученному раствору ацетанилида добавляют смесь концентрированной азотной кислоты и мочевины в ледяной уксусной кислоте. После выдержки при комнатной температуре технический продукт осаждают разбавлением нитромассы водой при 0°С. Выход технического нитропродукта около 90%. Разделение о - и п -нитроанилина основано на различной растворимости и различной скорости омыления о - и п -нитроацетанилидов.
Если при нитровании ацетанилида серно-азотной нитрующей смесью образуется главным образом п -нитроацетанилид, то при нитровании в среде уксусной кислоты в качестве основного продукта образуется о -нитроацетанилид.
7. Нитрование смесью концентрированной азотной кислоты с уксусным ангидридом
Метод применяют для нитрования активных аренов, в том числе и ацидофобных соединений, применяют чаще, чем нитрование в уксусной кислоте.
Нитрующие частицы образуются при взаимодействии уксусного ангидрида с концентрированной азотной кислотой. При этом реакция катализируется добавлением каталитических количеств серной кислоты:

Нитрующими частицами являются (в порядке возрастания активности):
а)ацетилнитрат, который способен к электрофильной атаке за счет поляризации молекулы; б) протонированная форма ацетилнитрата; в) нитроний-катион (мало).
 ;
;  ; NO2+
; NO2+
Вместо уксусного ангидрида в некоторых случаях используются ангидриды других кислот, например, бензойной.
Степень превращения азотной кислоты в ацетилнитрат зависит от температуры. При 20°С превращение происходит на 75% (в конц. HNO3 1% нитроний - катиона), но при –10°С ацетилнитрат не образуется.
Достоинства метода: 1) высокая концентрация нитрующих частиц; 2) возможность нитрования малоустойчивые и ацидофобные соединения; 3) высокий выход; 4) замещение идет селективно, преимущественно в о-положение.
Основным недостатком является опасность процесса. Несоблюдение режима смешения азотной кислоты и уксусного ангидрида приводит к образованию не только ацетилнитрата, но и ряда побочных продуктов, обладающих взрывчатыми свойствами, в том числе тетранитрометана. Известны случаи, когда ацетилнитрат взрывался не только при нагревании, но и на холоду.
Метод используют:
- При нитровании мезо-3,4-дифенилгексана (получение курареподобного препарата парамиона):

- При нитровании "пиридона" в синтезе витамина В6 (в реактор загружают уксусный ангидрид и засыпают расчетное количество "пиридона" и мочевины, а затем медленно при 45°С добавляют нитрующую смесь из азотной кислоты и уксусного ангидрида):

- При нитровании пятичленных гетероциклов с одним гетероатомом и их производных.
Фуран, пиррол и индол, которые в средах с сильными кислотами расщепляются и образуют смолы, нитруются ацетилнитратом с высоким выходом при температуре до 5°С. Аналогично нитруется тиофен:


Фуран с ацетилнитратом образует продукт 1,4-присоединения:

Нитрование фурфурола (в производстве фурациллина, фуразолидона и др.) осуществляют по схеме:
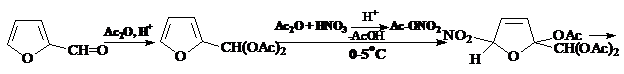

- Процесс нитрования фурфурола осуществляется одновременным прибавлением субстрата и смеси азотной и серной кислот к охлажденному уксусному ангидриду (без предварительного приготовления раствора ацетилнитрата). Реакцию проводят в среде уксусного ангидрида, который берется в избытке, и используется для защиты альдегидной группы фурфуролаот окисления.
Реакция протекает весьма быстро, в основном, во время смешивания компонентов. Вначале образуется фурфуролдиацетат, который затем нитруется образовавшимся ацетилнитратом.
Прибавление нитрующей смеси и фурфурола ведется при четком соблюдении температурного режима в реакторе (температура не должна превышать 5°С). Оба компонента добавляются одновременно и в строгой пропорции: на 1 л нитрующей смеси 1,3-1,5 л фурфурола. Регулирование дозировки осуществляется автоматически.
При повышении температуры в реакционной массе автоматика отключает подачу сырья и сигнализирует о нарушении режима. После снижения температуры в реакторе до 0°С дозатор автоматически включается.
- После завершения реакции нитрования реакционную смесь разбавляют водой, при этом уксусный ангидрид превращается в уксусную кислоту:

- Деацетоксилирование 5-нитро-2-ацетокси-2,5-дигидрофурфуролди-ацетата проводят частичной нейтрализацией реакционной массы (до рН 4¸4,5) 25%-ным раствором едкого натра при температуре 15¸35°С и выдерживают при температуре 50-55°С 1 ч. Затем реакционную массу охлаждают до 15-20°С, выпавший осадок 5-нитрофурфуролдиацетата отфуговывают и промывают на центрифуге холодной водой.
Этот способ получения 5-нитрофурфуролдиацетата позволил:
- существенно повысить безопасность технологического процесса;
- сократить расход дорогостоящего сырья; количество сточных вод
- облегчить обслуживание реакторов нитрования;
- Нитрование аренов солями азотной кислоты в уксусном ангидриде (реакция Менке) - метод является разновидностью предыдущего, но более безопасен и селективен.
Нитровать можно разными солями, но наибольшая скорость наблюдается при использовании смеси нитратов меди (II) и железа (III). Реакция идет при невысоких температурах, без осмоления, с высокой селективностью. Например, из анилина при действии нитрата меди в среде уксусного ангидрида образуется только о-нитроацетанилид, а при действии нитрата лития – только п-нитроацетанилид.
Описано нитрование пиридона при температуре 70-80°С смесью уксусного ангидрида и нитрата железа (III).


Прибавление ледяной уксусной кислоты способствует более спокойному течению реакции. Во многих случаях уксусный ангидрид можно полностью заменить уксусной кислотой. Например, из фенола при действии нитрата меди и ледяной уксусной кислоты образуется только о-нитрофенол.