ХИМИЧЕСКИЙ ЭКВИВАЛЕНТ
Методические указания
по дисциплине «Химия»
для бакалавров по направлениям:
"Строительство", "Стандартизация и метрология", "Товароведение", "Технология художественной обработки материалов", "Техносферная безопасность", "Эксплуатация транспортно-технических машин и комплексов", "Технология транспортных процессов" всех профилей дневного и заочного отделений
Ростов - на - Дону
УДК 541.2
Химический эквивалент: методические указания по дисциплине «Химия» для бакалавров.– Ростов н/Д: Рост. гос. строит. ун-т, 2012. – 16 с.
Изложены сведения по определению эквивалентных масс простых и сложных соединений. Описана методика определения эквивалентной массы магния по объему вытесненного водорода.
Предназначены для бакалавров 1-го курса, обучающихся по направлениям "Строительство", "Стандартизация и метрология", "Товароведение", "Технология художественной обработки материалов", "Техносферная безопасность", "Эксплуатация транспортно-технических машин и комплексов", "Технология транспортных процессов" всех профилей дневного и заочного отделений.
Электронная версия находится в библиотеке, ауд. 224.
УДК 541.2
Составитель доц. М.А. Таутиева
Редактор Н.Е. Гладких
Темплан 2012 г., поз. 76
__________________________________________________________________
Подписано в печать 6.12.11
Формат 60x84/16. Бумага белая. Ризограф.
Уч.-изд.л. 0,7. Тираж 100 экз. Заказ
__________________________________________________________________
Редакционно-издательский центр
Ростовского государственного строительного университета
344022, Ростов-на-Дону, ул. Социалистическая, 162
© Ростовский государственный
строительный университет, 2012
Правила техники безопасности
При выполнении лабораторной работы
«Определение химического эквивалента»
Все мероприятия по технике безопасности при проведении лабораторной работы сводятся к правильной работе с химическими реактивами.
1. Перед началом лабораторных работ каждый студент должен ознакомиться с правилами техники безопасности и строго их выполнять.
2. Без разрешения преподавателя нельзя проводить никаких опытов, не предусмотренных планом работы.
3. Во время работы не следует набирать кислоту при помощи пипетки, для этого рекомендуется использовать мерный цилиндр на 10 мл.
4. Присоединяя пробирку к прибору, соблюдать осторожность во избежание порезов.
Правила оформления лабораторной работы
1. Отчёт о выполнении лабораторной работы записывается в специальной лабораторной тетради, объём которой должен быть достаточным для оформления всех работ, включённых в настоящий практикум по общей химии. Запрещается вести записи на отдельных листках и черновых тетрадях.
2. В лабораторной тетради записываются следующие данные:
а) дата;
б) номер и название работы;
в) название эксперимента;
г) схема и рисунок основного прибора;
д) химические формулы и расчеты эксперимента;
ж) наблюдение в ходе проведения опыта (интенсивность процесса, условия его проведения, сопутствующие его явления; выделение газа и т.д.);
з) выводы (таблицы, итоговые обобщения).
3. Всё оформление работы проводится во время занятий, по окончании которых студент предъявляет лабораторную тетрадь преподавателю на проверку.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Химический эквивалент представляет собой одну из важнейших характеристик химического элемента. Экспериментально установлено, что различные вещества реагируют друг с другом в определенных количественных соотношениях. Так, содержание водорода в воде составляет 11,11%, кислорода – 88,89 %. Это означает, что они реагируют между собой в массовом соотношении 1: 8, а в молярном соотношении 2: 1. Эти количества равноценны (эквивалентны) по отношению друг к другу.
Эквивалентом элемента (Э) называют такое его количество, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях. Например, в соединении водорода с кислородом – воде (Н2О) – на 1 моль атомов приходится, как видно из формулы соединения, 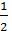 моля атомов кислорода. Следовательно, эквивалент кислорода равен
моля атомов кислорода. Следовательно, эквивалент кислорода равен  моля атомов кислорода. В соединении водорода с азотом NH3 – на 1 моль атомов водорода приходится
моля атомов кислорода. В соединении водорода с азотом NH3 – на 1 моль атомов водорода приходится  моля атомов азота, следовательно, эквивалент азота в этом соединении равен
моля атомов азота, следовательно, эквивалент азота в этом соединении равен  моля атомов азота.
моля атомов азота.
При определении эквивалента элемента необязательно исходить из его соединения с водородом. Эквивалент можно вычислить по составу соединения данного элемента с любым другим, эквивалент которого известен.
При расчетах используется эквивалентная масса Мэ – масса одного эквивалента. Она имеет размерность г/экв. В приведенных выше соединениях (Н2О, NH3) эквивалентные массы будут
Мэ (Н) = 1 г/экв, Мэ (О) = 16: 2 = 8 г/экв, Мэ (N) = 14: 3 = 4,67 г/экв.
Поскольку эквивалент измеряется в молях, то часто используется размерность г/моль.
Эквивалентная масса элемента связана с мольной (атомной) массой элемента. Она равна мольной (атомной) массе, деленной на валентность элемента в данном химическом соединении.
Мэ (элемента) =  .
.
Эквивалентная масса может быть переменной величиной, так как зависит от валентности элемента в различных соединениях. Например, эквивалентная масса серы в разных соединениях:
а) сероводороде H2S Мэ (S) = 32: 2 = 16 г/экв;
б) оксиде серы (IV) SO2 Мэ (S) = 32: 4 = 8 г/экв;
в) оксиде серы (VI) SO3 Мэ (S)= 32: 6 = 5,3 г/экв.
Понятие об эквивалентах и эквивалентной массе распространяется и на сложные соединения (оксиды, кислоты, основания, соли). Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода или с одним эквивалентом любого другого элемента.
Эквивалентная масса сложного вещества может иметь различные значения в зависимости от характера реакции, в которую вступает данное вещество, и от того, какой продукт при этом образуется.
Эквивалентная масса кислоты Мэ (кислоты) равна молярной массе кислоты, деленной на основность кислоты (число атомов водорода, замещенных в данной реакции на металл).
Мэ (кислоты) =  .
.
Например, эквивалентная масса кислоты в реакции
H2SO4 + KOH = KHSO4 + H2O;
Мэ (Н2SO4) =  = 98 г/экв,
= 98 г/экв,
а в реакции
H2SO4 + Mg = MgSO4
эквивалентная масса той же кислоты вдвое меньше, так как в этой реакции замещено два катиона водорода:
Мэ (H2SO4) =  = 49 г/экв.
= 49 г/экв.
Эквивалентная масса основания Мэ (основания) равна молярной массе основания, деленной на кислотность этого основания (число гидроксогрупп, замещенных на кислотный остаток).
Мэ (основания) = 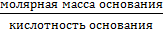 .
.
Например, эквивалентная масса основания Mg(OH)2 в реакции Mg(OH)2 + HСl = MgOHCl + H2O;
Мэ (Мg(OH)2) =  = 58 г/экв,
= 58 г/экв,
а в реакции
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
эквивалентная масса того же основания в два раза меньше
Мэ (Мg(OH)2) =  = 29 г/экв.
= 29 г/экв.
Эквивалентная масса соли Мэ (соли) равна молярной массе соли, деленной на произведение валентности металла (ВМе) на число его атомов (n).
Мэ(соли) =  .
.
Например,
Мэ (Na2SO4) =  = 71 г/экв.
= 71 г/экв.
Эквивалентная масса оксида равна молярной массе оксида, деленной на произведение валентности элемента (Вэл) на число его атомов (n).
Мэ (оксида) =  .
.
Например,
Мэ (Al2O3) =  = 17 г/экв.
= 17 г/экв.
Молярную массу эквивалента любого сложного соединения можно определить по сумме эквивалентных масс составляющих его частиц. Например:
а) молярная масса гидроксида натрия равна сумме молярных масс эквивалентов металла и гидроксогруппы, т.е.
Мэ (основания) = Мэ (металла) + Мэ (гидроксогруппы);
Мэ (NaOH) = Mэ (Na+) + Mэ (OH-) = 23 + 17 = 40 г/экв;
б) эквивалентная масса кислоты равна сумме эквивалентных масс водорода и кислотных остатков
Мэ (кислоты) = Мэ (Н+) + Мэ (кислотного остатка);
Мэ (H2SO4) = Мэ (Н+) + Мэ (S  ) = 1 + 48 = 49 г/экв;
) = 1 + 48 = 49 г/экв;
в) эквивалентная масса соли равна сумме эквивалентных масс металла и кислотного остатка
Мэ (соли) = Мэ (металла) + Мэ (кислотного остатка);
Мэ (Al2(SO4)3) = Мэ (Al3+) + Mэ (S  ) =
) = 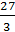 +
+  = 57 г/экв;
= 57 г/экв;
г) эквивалентная масса оксида равна сумме эквивалентных масс кислорода и элемента
М э (оксида) = Мэ (элемента ) + Мэ (кислорода);
Мэ (МgO) = Mэ (Mg2+) + Mэ (О2-) =  +
+  = 20 г/экв.
= 20 г/экв.
Закон эквивалентов (Рихтер, 1792 г.)
Химические элементы (сложные соединения) соединяются или замещают друг друга в весовом соотношении, равном отношению их эквивалентных масс
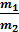 =
= 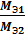 или
или  =
=  ,
,
где m1 и m2 – массы реагирующих веществ (г, кг, %).
Если одно из веществ находится в газообразном состоянии, закон эквивалентов записывается следующим образом:
 =
=  ,
,
где m1 и Мэ1 – масса и эквивалентная масса твердого или жидкого вещества; V2 и Vэ2 – объем и молярный объем эквивалента газообразного вещества;
Vэ – молярный объем эквивалента газа (эквивалентный объем) при нормальных условиях. Как известно, моль любого газа при нормальных условиях занимает объем 22,4 л. Так как масса моля водорода равна 2 г, а масса эквивалента – 1 г, то эквивалентный объем водорода будет в два раза меньше молярного, т.е. Vэ (Н) = 22,4: 2 = 11,2 л/экв.
Молярная масса кислорода 32 г/ моль соответствует объему 22,4 л. Т.к. эквивалентная масса кислорода – 8 г/экв, то его эквивалентный объем
Vэ (О) = 22,4: 4 = 5,6 л/экв;
Vэ =  .
.
Примеры решения задач
Пример 1. Элемент образует гидрид, где его массовая доля 75%. Определите эквивалентную массу элемента.
Решение. Эквивалентом элемента называется такое его количество, которое соединяется с одним молем атомов водорода или замещает его в химических реакциях. Массу одного моля эквивалента элемента называют молярной массой эквивалента. Эта задача решается на основе закона эквивалентов, согласно которому химические элементы (сложные вещества) соединяются между собой или замещают друг друга в количествах, пропорциональных их молярным массам эквивалентов.
Вычислим массовую долю водорода в гидриде
w (Э) = 100% - 75% = 25%.
Согласно закону эквивалентов m(Эл) / m(H) =MЭ(Эл) / MЭ(H). При образовании 100 г гидрида 25 г водорода соединяются с 75 г элемента. Исходя из этого
MЭ(Эл) = 1 г/моль ´ 75 г / 25 г = 3 г/моль.
Пример 2. При сгорании 15 г металла образуется 28,32 г оксида металла. Вычислите эквивалентную массу металла.
Решение. Эквивалентная масса кислорода MЭ (О) = 8 г/моль. Масса кислорода в оксиде m (O) = 28,32 - 15,00 = 13,32 г. Тогда согласно закону эквивалентов:
MЭ(Ме) = МЭ(О) ´ m(Me) / m (O) = 8 г/моль ´ 15 г / 13,32 г = 9 г/моль.
Пример 3. Рассчитайте молярную массу эквивалента металла, если 1,168 г его вытеснили из кислоты 438 мл водорода, измеренного при 17оС и давлении 98642 Па.
Решение. Приведем объем вытесненного водорода к нормальным условиям, воспользовавшись объединенным газовым уравнением
 =
=  ,
,
V0 = P ´ V ´ Т0 / P0 ´ Т = 98642 ´ 438 ´ 273 / 1,013 ´ 10 5 ´ 298 = 401,5 мл.
Эквивалентный объем водорода VЭ (H2) = 11,2 л/моль при нормальных условиях, поэтому
m(Me) / V (H2) = MЭ (Ме) / VЭ (H2);
MЭ (Me) = 1,168 г ´ 11,2 л/моль / 0,4015 л = 32,58 г/моль.
Пример 4. На нейтрализацию 0,471 г фосфористой кислоты израсходовано 0,644 г KOH. Вычислите молярную массу эквивалента кислоты.
Решение. Эквивалентная масса КОН равна ее молярной массе, так как основание содержит одну гидроксогруппу и составит MЭ (КОН) =56 г/моль. Тогда согласно закону эквивалентов:
m (кислоты) / m (КОН) = MЭ (кислоты) / MЭ (КОН);
MЭ (кислоты) = 56 г/моль ´ 0,471 г / 0, 644 г = 40, 96 г/моль.