Давайте вспомним (устно)
Даны вещества:
А) метан б)ацетилен в)этанол г)уксусная кислота д)бутадиен -1,3 е)глицерин
Задания:
1)У какого из веществ две двойные связи?
2)Назовите вещество, относящееся к классу спиртов.
3)У какого из веществ 2 и 3связи?
4)Общая формула класса веществ, к которому относят данное вещество СnH2n-2.
Актуализация знаний.
На прошлом урокемы изучалиодноосновные карбоновые кислоты.
Рассмотрим многоосновные карбоновые кислоты, отметим особенности строения и области применения. Что значит многоосновные? Это значит, что у этих кислот несколько групп –СООН. Например, у обычной уксусной – всего одна. Но может быть и 2, и 3.
Лимонная кислота: НООС-СН2-СОН-СН2-СООН
Молочная кислота: СН3-СНОН- СООН
Щавелевая кислота: НООС- СООН
Высшие карбоновые кислоты:
С15Н31СООН- пальметиновая кислота
С17Н35СООН- стеориновая кислота
Мыла- соли С17Н35СООК, С17Н35СООNа
Смотрим видео: https://www.youtube.com/watch?v=DhOs9mkpUR0
Сложные эфиры — это продукт взаимодействия спирта с кислородсодержащей кислотой.
Процесс получения сложных эфиров носит название реакции этерификации. Эта реакция с использованием общих формул описывается уравнением
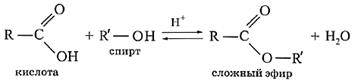 (уравнение записываем)
(уравнение записываем)
Обратите внимание на то, как строится название сложного эфира. Оно состоит из четырёх слов, указывающих на название углеводородного радикала и исходной кислоты. Например, продукт взаимодействия муравьиной кислоты с метиловым спиртом — метиловый эфир муравьиной кислоты
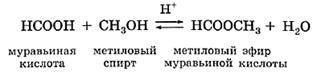 (реакцию записываем)
(реакцию записываем)
Сложные эфиры широко распространены в природе. Неповторимый аромат цветов и фруктов часто обусловлен присутствием веществ именно этого класса. Сложные эфиры с большой молекулярной массой представляют собой твёрдые вещества — воски. Пчелиный воск — это смесь сложных эфиров, образованных карбоновыми кислотами и спиртами с длинными углеводородными цепями.
Синтетические сложные эфиры используют в пищевой промышленности в качестве добавок для придания фруктовых запахов напиткам и кондитерским изделиям. Благодаря хорошей растворяющей способности сложные эфиры входят в состав растворителей лаков и красок.
Теперь вспомним о жирах. Они вам известны? Растительное и оливковое масло, сало….
Люди стали использовать жиры в повседневной жизни значительно раньше, чем задумались об их химическом строении. Животные и растительные жиры — важные компоненты пищи. Жиры необходимы для построения клеточных мембран и как источник энергии, поскольку калорийность жиров в 2 раза выше, чем других питательных веществ — углеводов и белков. У позвоночных животных жиры откладываются в жировой ткани, сосредоточенной в основном в подкожной жировой клетчатке и сальнике. В растениях жиры содержатся в сравнительно небольших количествах, за исключением семян масличных растений, в которых содержание жиров может быть более 50%.
Жирыпредставляют собой сложные эфиры трёхатомного спирта глицерина и высших карбоновых кислот.
Общую формулу жиров можно представить в следующем виде:
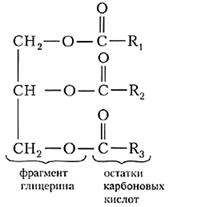 (записываем формулу)
(записываем формулу)
Сравните состав стеариновой (С17Н35СООН) и олеиновой (С17Н33СООН) кислот. У стеариновой кислоты углеводородный радикал отвечает формуле СnН2n+1, т. е. является предельным. Следовательно, стеариновая кислота относится к предельным карбоновым кислотам. В углеводородном радикале олеиновой кислоты на два атома водорода меньше, поскольку в нём содержится одна двойная углерод-углеродная связь. Олеиновая кислота относится к непредельным карбоновым кислотам.
Жиры животного происхождения имеют твёрдую консистенцию (есть и исключения, например жидкий рыбий жир). В состав молекул твёрдых жиров входят остатки предельных кислот. Растительные жиры, которые часто называют растительными маслами, образованы остатками непредельных кислот, имеют жидкую консистенцию (исключение — твёрдое пальмовое масло). Кстати, название олеиновой кислоты произошло от латинского слова oleum — масло.
Жиры гидрофобны, т.е. нерастворимы в воде (вспомните, как плавает масло в воде!), но хорошо растворяются в органических растворителях: этиловом спирте, гексане, тетрахлорметане.
Жиры проявляют все характерные для сложных эфиров химические свойства. Главное из них — это гидролиз. Молекулы воды атакуют связи между кислотным остатком и фрагментом глицерина, в результате чего происходит распад молекулы жира
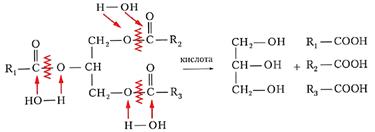 (записываем реакцию)
(записываем реакцию)
Домашнее задание: читаем параграф 29, 30. На стр.145 письменно отвечаем на вопросы №2, 3, 5.