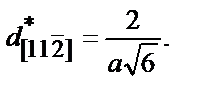Известно, что кристаллическим структурам свойственна тенденция к образованию плотных и плотнейших упаковок как структур, обладающих минимальной свободной энергией.
При рассмотрении моделей плотных и плотнейших упаковок материальные частицы отождествляют с жесткими несминаемыми шарами, притягивающимися друг к другу. Шары, касаясь, заполняют большую часть объема, однако междуними образуются пустые пространства, которые называются пустотами.
 Рис.3.4. Плотнейшая упаковка атомов в плоскости
Рис.3.4. Плотнейшая упаковка атомов в плоскости
|
Представим себе, что в пространстве весь объем заполнен плотнейшимобразом упакованными слоями атомов. Если обозначить через А первый слой атомов (рис.3.5, а), то второй такой же атомный слой В (обозначимцентры тяжести его атомов серыми кружками) плотно ляжет на первый, если его атомы попадут в лунки между атомами первого слоя А (см. рис.3.5, а). Оказывается, что третий слой атомов C (обозначим центры тяжести его атомов черными кружками) может быть уложен на второй двояким образом. Если шары третьего слоя уложить так, что их центры тяжести придутся над центрами тяжести шаров первого слоя (рис.3.5, б), то получится гексагональная плотнейшая упаковка (ГПУ). Поэтому чередование атомных слоев в пространстве можно записать в виде алгоритма
 Рис.3.5. Плотнейшие упаковки ГПУ и ГЦК
Рис.3.5. Плотнейшие упаковки ГПУ и ГЦК
|
АВАВАВ ¼, т.е. атомы третьего слоя повторяют положение атомов первого слоя.
Во втором варианте упаковки третий слой атомов С (рис.3.5, в) займет положение в пространстве, отличное от положенияпервого слоя А и второго слоя В: его центры окажутсянад центрами лунок первого слоя (отмечены белыми кружками), незаполненных атомами второго слоя. В этом случае алгоритм чередования атомных слоев в пространстве имеет вид АВСАВС ¼, т.е. положение первого слоя повторяется атомами четвертого слоя. Такая упаковка называется гранецентрированной кубической (ГЦК).
В обеих плотнейших упаковках коэффициент компактности h составляет 0,74, т.е. атомы занимают около 3/4 объема. Во всех остальных упаковках и структурах коэффициенткомпактности h < 0,74. Координационные числа для решеток ГЦК и ГПУ максимальны из возможных, одинаковы и равны 12 (обозначаются как K12 и Г12 соответственно) (рис.3.5, г,д), что нетрудно представить себе из описанного выше метода получения плотнейших упаковок: каждый атом окружен шестью атомами в своем слое, тремя снизу и тремя сверху.
 Рис.3.6. Тетраэдрические (а) и октаэдрические (б) пустоты
Рис.3.6. Тетраэдрические (а) и октаэдрические (б) пустоты
|
В элементарной ячейке ГЦК центры тетраэдрических пустот находятся в точках с координатами |[1/4,1/4,1/4]| и |[3/4,3/4,3/4]|, которые располагаются по две на каждой пространственной диагонали куба; всего их 8. Центры октаэдрических пустот расположены в середине каждого ребра (внутри элементарной ячейки оказывается 1/4 часть объема от каждой такой пустоты) и в центре куба. Всего в ячейке  октаэдрические пустоты.
октаэдрические пустоты.
Ячейка ГПУ может быть представлена в виде ромбической призмы, у которой атомы находятся в вершинах и один атом расположен над центром одного из правильных треугольников основания на 1/2 высоты призмы. Число атомов в ячейке складывается из долей атомов, лежащих внутри нее:
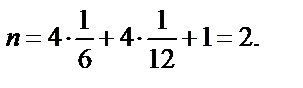
Октаэдрических пустот в ГПУ упаковке две. Тетраэдрических пустот в ГПУ четыре (в два раза больше, чем число атомов) (см. рис.3.8). При этом удобно пользоваться представлением решетки в виде гексагональнойпризмы.
Идея плотнейших упаковок оказалась удобной для описания сложных кристаллических структур.
 Рис.3.7. Положение пустот в ГЦК плотнейшей упаковке:
а - октаэдрических; б - тетраэдрических
Рис.3.7. Положение пустот в ГЦК плотнейшей упаковке:
а - октаэдрических; б - тетраэдрических
 Рис.3.8. Положение пустот в ГПУ плотнейшей упаковке: а - октаэдрических; б - тетраэдрических
Рис.3.8. Положение пустот в ГПУ плотнейшей упаковке: а - октаэдрических; б - тетраэдрических
|
3.2. Кристаллохимический анализ типичных
структур металлов
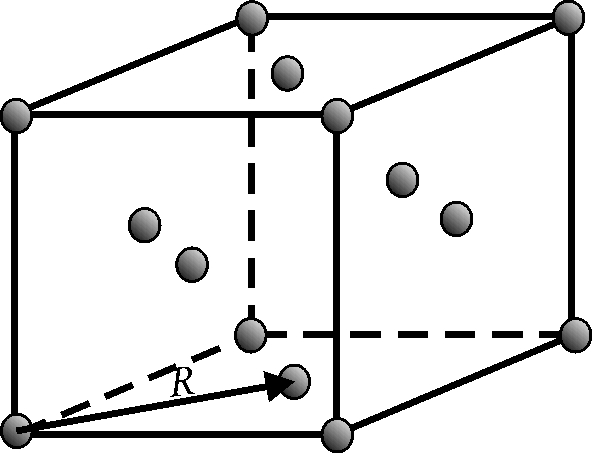 Рис.3.9. Структурный тип меди (ГЦК решетка)
Рис.3.9. Структурный тип меди (ГЦК решетка)
|
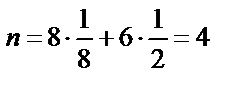
К 12
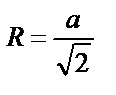
۟h = 0,74
Наиболее плотноупакованная плоскость - (111), наиболее плотноупакованное направление - [110].
 Рис.3.10. Структурный тип вольфрама (ОЦК решетка)
Рис.3.10. Структурный тип вольфрама (ОЦК решетка)
|

К 8
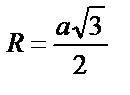
h = 0,68
Самая плотноупакованная плоскость - (110), самое плотноупакованное направление - [111].
Структурный тип магния. В структурном типе магния кристаллизуются металлы: кадмий, бериллий, цинк, кобальт, β-титан, рений и некоторые другие. Структура совпадает с плотнейшей упаковкой ГПУ, все пустоты свободны (рис.3.11). Для металлов, кристаллизующихся в этом структурном типе, характерна анизотропия свойств вдоль осей X, Y, U и вдоль оси Z.
 Рис.3.11. Структурный тип магния
Рис.3.11. Структурный тип магния
|
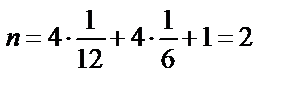
Г 12

h = 0,74
Наиболее плотноупакованная плоскость - (0001), наиболее плотноупакованное направление - 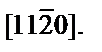
Пример решения варианта контрольной работы
1. Указать элемент, кристаллизующийся в структурном типе магния: Na, Zn, Pt.
2. Определить коэффициент заполнения пространства в решетке Ag.
3. Определить ретикулярную плотность плоскости 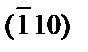 в решетке Mo.
в решетке Mo.
4. Определить ретикулярную плотность направления  в решетке Au.
в решетке Au.
5. Решить кристаллохимическую задачу.
Решение
Задание 1. В структурном типе магния кристаллизуется Zn.
Задание 2. Коэффициент заполнения пространства определяется из соотношения
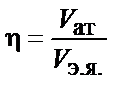 ,
,
где V ат - объем, который занимают атомы в элементарной ячейке; V э.я. - объем элементарной ячейки. Объем атомов, принадлежащих элементарной ячейке, рассчитывается по формуле:
 ,
,
где 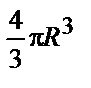 - объем одного атома, n - число атомов в элементарной ячейке Ag, R - радиус атома Ag. Объем элементарной ячейки серебра, имеющего ГЦК решетку, равен параметру решетки a в кубе:
- объем одного атома, n - число атомов в элементарной ячейке Ag, R - радиус атома Ag. Объем элементарной ячейки серебра, имеющего ГЦК решетку, равен параметру решетки a в кубе:
V э.я. = a 3 .
Для решетки ГЦК самое плотноупакованное направление - [110], 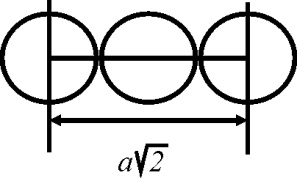 вдоль этого направления атомы соприкасаются. Из соотношения
вдоль этого направления атомы соприкасаются. Из соотношения  определяем радиус атома:
определяем радиус атома: 
Тогда
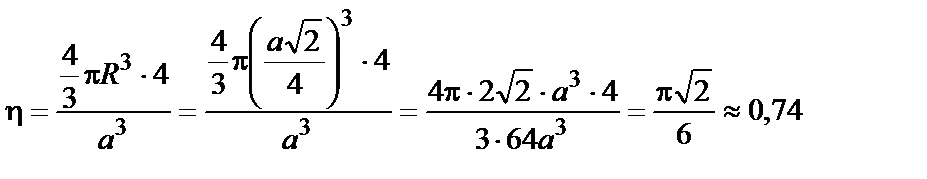 .
.
Ответ: h » 0,74.
Задание 3. Кристаллическая структура Mo - ОЦК:

Тогда 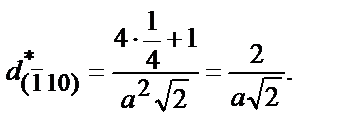
Ответ: 
Задание 4. Кристаллическая структура Au - ГЦК:
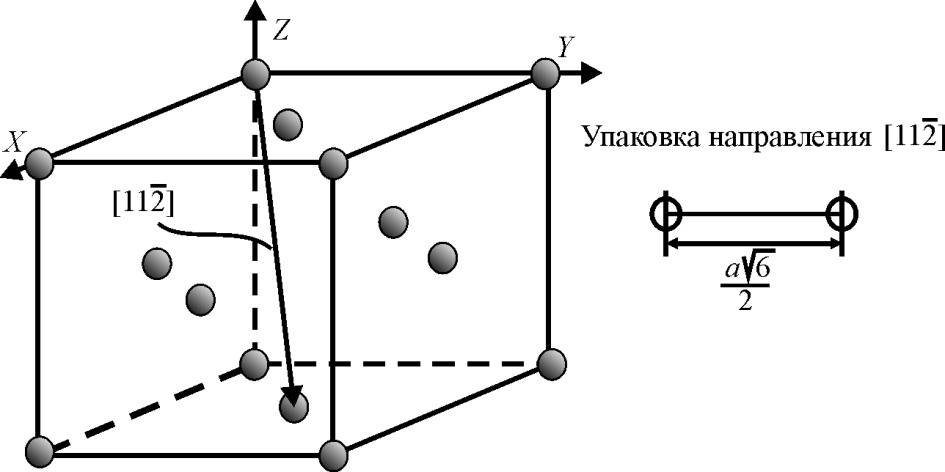
Тогда 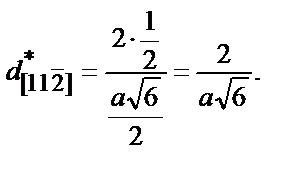
Ответ: