Используя графическую кластеризацию аппроксимации и проекции однородного многообразия (UMAP) 23, алгоритм одноклеточного распознавания типов клеток (SingleR) 24 и ручную аннотацию на основе канонических маркеров генов, мы идентифицировали 22 типа или подтипа клеток и выполнили анализ дифференциальной экспрессии. среди всех типов клеток (рис. 3b и дополнительная таблица S8). Клетки (клеточные транскриптомы) из образцов до (синий) и после (оранжевый) вакцинации были четко разделены в представлении UMAP для обеих когорт, что означало, что иммунологические характеристики сильно изменились почти во всех обнаруженных типах иммунных клеток и постоянно у всех добровольцев (Рис. 3c). Среди 11 пар (до и после) образцов PBMC 10 пар секвенировали вместе, а одну пару секвенировали отдельно в другой партии. Распределения UMAP были очень похожими независимо от разных партий, что свидетельствует о минимальных эффектах партии при секвенировании (дополнительный рисунок S1b). Две независимые серии секвенирования выявили аналогичные изменения до и после вакцинации, предполагая, что изменения реальны, тогда как при использовании метода коррекции эффекта партии (Harmony 25) (дополнительный рис. S1c – e)) приведет к чрезмерной фильтрации и устранению реальных изменений, вызванных вакцинацией. Более того, кластеризация образцов на основе коэффициента корреляции Пирсона транскриптомов показала, что образцы из двух когорт (A и B) хорошо перемешались друг с другом как до, так и после вакцинации, тогда как изменения, вызванные вакцинацией, можно было четко наблюдать (рис. 3d).. Поэтому для увеличения статистической мощности мы объединили две когорты для последующего анализа.
|
|
Чтобы выявить различия в составах типов клеток до и после вакцинации, мы рассчитали относительные проценты всех типов клеток в PBMC каждого человека на основе данных scRNA-seq (фиг. 3e). Мы наблюдали снижение содержания регуляторных Т- лимфоцитов CD4 + (CD4.Treg), CD8 + Т-клеток (CD8.T) и пролиферирующих клеток CD8 + (CD8.Tprolif) после вакцинации (рис. 3e). Снижение содержания γδ-Т-клеток (gd.T.Vd2) также было значительным (рис. 3e). Напротив, вакцинация увеличивала содержание CD14 +классических моноцитов (Mono.C) (рис. 3e), что согласуется с клиническими лабораторными измерениями (рис. 3f).). Общее содержание лимфоцитов, которое включает все CD4 + Т-клетки, все CD8 + Т-клетки, В-клетки и NK-клетки, существенно не изменилось до и после вакцинации, что также было подтверждено клиническими лабораторными измерениями (рис. 3g). Мы собрали опубликованный набор данных от 196 пациентов, инфицированных COVID-19, и контрольной группы 7, и проанализировали наши данные вместе с этим набором данных. Результат показал, что вызванные вакцинацией изменения клеточного содержания всех пяти различных подтипов иммунных клеток также изменились в тех же направлениях у пациентов с COVID-19 по сравнению с контрольной группой, за исключением пролиферирующих CD8 + Т-клеток (дополнительный рисунок S2).
Чтобы изучить подробные изменения экспрессии генов, вызванные вакцинацией, мы объединили отдельные образцы в псевдогрупповые образцы и использовали тест парных образцов для идентификации дифференциально экспрессируемых генов (DEG) (рис. 3h и дополнительная таблица S9). Значительно активизированные гены были вовлечены в «передачу сигналов TNFα через NF-κB», «воспалительные реакции» и «взаимодействие цитокин-цитокиновый рецептор», «передачу сигналов IL6-JAK STAT3», «коагуляцию», «гипоксию», о которых сообщалось для COVID-19, в то время как пути, связанные с клеточным циклом, были подавлены (рис. 3i). Эти результаты подтверждают мнение о том, что вакцинация имитирует инфекцию 6, 7, 8, 9, 10, 11., 12.
|
|
Характерные изменения экспрессии генов, специфичных для подтипов иммунных клеток, отражают изменения в клинических лабораториях
До выяснения функциональной гетерогенности и изменений экспрессии генов, специфичных для конкретных типов клеток, между образцами до и после вакцинации мы сгруппировали клетки по 11 основным типам: (1) CD4 + Т-клетки в наивном состоянии, (2) CD8 в наивном состоянии. + Т-клетки, (3) CD4 + хелперные Т-клетки (включая CD4.T, CD4.Treg и CD4.Tprolif), (4) CD8 + цитотоксические Т-клетки (включая CD8.T, CD8B.T и CD8.Tprolif), (5) MAIT, (6) γδ-Т-клетки, (7) NK-клетки (включая NK, пролиферативные NK), (8) B / плазмобластные клетки (включая B-клетки и плазмобласты), (9) моноциты / дендритные клетки (включая классические моно, промежуточные моно, неклассические моно, миелоидный DC1, миелоидный DC2 и плазмацитоидный DC), (10) концевые эффекторные Т-клетки CD4 + и (11) CD8+терминальные эффекторные Т-клетки. Следуя одиннадцати категориям основных типов клеток, мы выполнили сравнения на уровне выборки путем агрегирования экспрессии генов по основным типам клеток в пределах каждого донора, а затем выполнили анализ дифференциальной экспрессии с использованием muscat 26. Мы идентифицировали дифференциально экспрессируемые гены (DEG) среди всех основных типов клеток (рис. 4a и дополнительная таблица S10) и провели функциональный анализ генов (рис. 4b).). Повторяя результаты клинических измерений, гены, относящиеся к «гомеостазу холестерина», «коагуляции» и «воспалительному ответу» (CXCL8, CD14, IL6 и TNFRSF1B), «передаче сигналов TNFα через NF-κB» (NFKB1, NFKB2, NFKBIE, TNFAIP3, и TNFSF9) и «гипоксия» (HIF1A) были активированы. Кроме того, гены, связанные с «передачей сигналов TGFβ», «IL2-STAT5» (IFNGR1, MAPKAPK2 и CASP3) и «передачей сигналов IL6-JAK-STAT3», также были активированы (фиг. 4c). Чтобы визуализировать, какие типы клеток были обогащены этими сигнатурами, мы выполнили оценку генного модуля и отобразили оценки в координатах UMAP, а также сгруппированные прямоугольные диаграммы (рис. 4c и дополнительная таблица S11.). Интересно, что гены «воспалительного ответа» были высоко экспрессированы в моноцитах и после вакцинации еще больше увеличивались (рис. 4c), что позволяет предположить, что моноциты были одним из основных типов клеток, участвующих в воспалительных ответах после вакцинации. Напротив, гены, связанные с «гликолизом», «метаболизмом желчных кислот» и «ответом на интерферон I типа (IFN-α / β)», были подавлены, что согласуется с нашими клиническими данными и патофизиологией COVID-19 13 (рис. 4d.).
|
|
Рис. 4: Подтип-специфическая дифференциальная экспрессия генов и анализ избыточной репрезентативности набора генов, отображающий общие изменения экспрессии генов среди различных типов иммунных клеток после вакцинации.
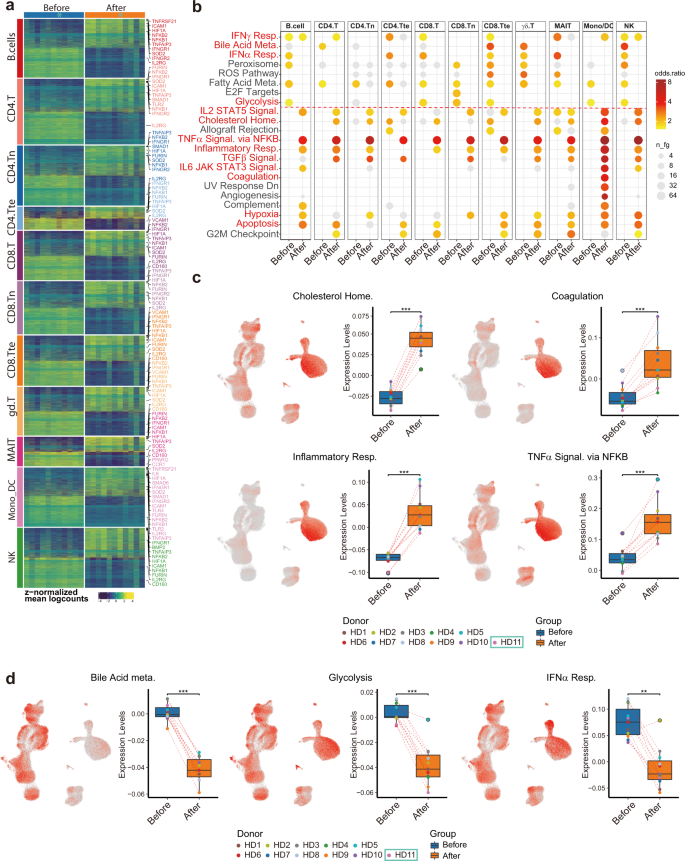
а 11 основных иммунные клетки типа специфических DegS, идентифицированных псевдо-объемных данных, полученных комбинациями образцов до и после вакцинации. Были включены гены с logFC> 0,5 и настройкой P <0,05. b Анализ репрезентативности наборов генов HALLMARK из MSigDB среди 11 основных типов клеток продемонстрировал общие изменения в наборах генов, представляющие измененные иммунологические состояния до и после вакцинации. c, d Визуализация UMAP, окрашенная средними показателями (уровнями) экспрессии на основе дифференциального пути обогащения. График в виде прямоугольников, изображающий распределение показателей экспрессии до и после вакцинации.