Изучение влияния концентрации на скорость очистки проводилось на той же лабораторной установке приведенной на рисунке 3.1. Результаты исследований приведены в таблице 3.2
Таблица 3.2 – Результаты исследований влияния концентраций кислот на процесс очистки поверхностей от накипи при температуре окружающей среды
| Реагент | Концен-трация кислоты, % | Объем реагента, см3 | Температура, ºС | Время реагирования, мин | Масса образца до очистки, г | Масса образца после очистки, г | Потери при очистке,% |
| HNO3 | 2,164 | 21,5 | 0,1917 | 0,1917 | |||
| 4,14 | 21,5 | 0,3050 | 0,3050 | ||||
| 9,43 | 21,5 | 0,3184 | 0,3184 | ||||
| HCl | 2,16 | 21,5 | 0,3342 | 0,3342 | |||
| 4,6 | 21,5 | 0,1616 | 0,1616 | ||||
| 5,61 | 21,5 | 0,2168 | 0,2168 | ||||
| H3PO4 | 3,63 | 21,5 | 0,1684 | 0,1684 | |||
| 7,5 | 21,5 | 0,1873 | 0,1873 | ||||
| 11,538 | 21,5 | 0,1917 | 0,1917 |
Потери при очистке рассчитаем по формуле приведенной выше.
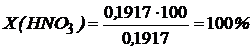
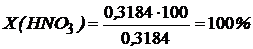
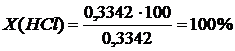
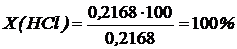
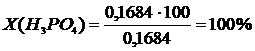
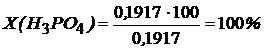
На основании полученных экспериментальных данных я сделала вывод: для очистки в промышленных условиях для наиболее эффективной очистки, при обычной температуре, целесообразно применять раствор азотной кислоты, а для домашнего использования - раствор соляной кислоты в виду того, что она менее токсична, чем азотная. Поэтому процесс очистки при повышении температуры изучим для раствора соляной кислоты.
Изучение процесса очистки при повышенной температуре для соляной кислоты проводилось на установке изображенной на рисунке 3.1. Для поддержания повышенной температуры она была помещена в термостат с электронагревом. Результаты исследований представлены в таблице 3.3.
Таблица 3.3 – Результаты исследований влияния температуры на процесс очистки поверхности от накипи в среде соляной кислоты
| Объем реагента, | Температура, ºС | Время реагирования, | Масса образца до очистки, г | Масса образца после очистки, г | Потери при очистке,% |
| 21,5 | 0,1616 | 0,1616 | |||
| 0,3623 | 0,3623 | ||||
| 0,3277 | 0,3277 |
Потери при очистке вычислим по формуле приведенной выше:
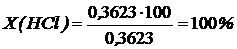
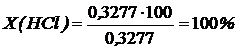
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
КИНЕТИЧЕСКИЕ ЗАВИСИМОСТИ
Для построения графика кинетической зависимости построим график зависимости скорости очистки, в зависимости от концентрации кислоты. Для этого скорость очистки выразим как массу вещества перешедшего за одну минуту. Для чего массу вещества перешедшую в раствор разделим на время за которое она перешла. График зависимостей примет вид (рис.4.1.- 4.3).
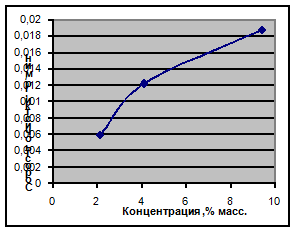
Рис. 4.1 – Зависимость скорости очистки от концентрации азотной кислоты.
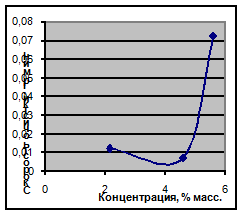
Рис. 4.2 – Зависимость скорости очистки от концентрации соляной кислоты.
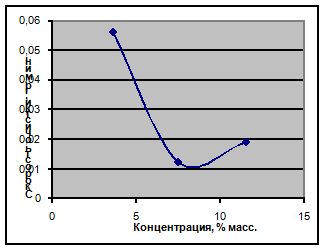
Рис. 4.2 – Зависимость скорости очистки от концентрации ортофосфорной кислоты.
Анализируя графики зависимостей можно сделать такие выводы: увеличение концентрации азотной кислоты будет способствовать увеличению скорости растворения накипи. В зависимости скорости растворения для соляной кислоты имееет место минимум в области приблизительно 4 % массовых. Увеличение концентрации выше 4 % способствует увеличению скорости растворения. Для фосфорной кислоты наблюдается обратная зависимость, когда с ростом концентрации кислоты скорость очистки снижается, это может объясняется тем, что при взаимодействии солей кальция с ортофосфорной кислотой происходит образование фосфатов кальция, которые образуют на поверхности нерастворимую плёнку.