Через определенное время, которое может составлять от нескольких секунд до нескольких лет, активность катализатора уменьшается до уровня, который делает продолжение работы экономически нецелесообразным. Может уменьшиться и его селективность. В таких случаях загруженный катализатор нужно регенерировать или заменить. Регенерацию катализатора осуществляют в том же каталитическом реакторе посредством пуска смеси другого состава или же катализатор выгружают и регенерацию производят где-либо в другом месте.
При обратимом отравлении для регенерации достаточно удаления яда из исходного сырья. В некоторых случаях требуется дополнительная обработка катализатора. Например, если Ni -катализатор дезактивируется добавками кислорода, его восстанавливают водородом, что приводит к восстановлению его активности, близкой к первоначальной.
Никель, необратимо отравленный серой, при обработке водяным паром или кислородом переводит серу в еще более трудно удаляемый сульфат. На практике эти катализаторы не регенерируют. Нанесенные катализаторы после спекания также не регенерируют.
Катализаторы, содержащие Pt, Pd, Rh и другие, удаляют из реактора для извлечения дорогого благородного металла.
Для регенерации закоксованного катализатора крекинга поток реакционной смеси через катализатор прекращают и катализатор нагревают в окислительной атмосфере, так что происходит окисление или «сгорание» кокса.
Основная задача при регенерации закоксованного катализатора - уменьшение роста температуры, вызванного экзотермической реакцией окисления кокса в СО и СО2. Нежелательный подъем температуры при регенерации может привести к спеканию катализатора. Одним из возможных решений является применение малых концентраций кислорода в начальных стадиях регенерации.
Исследование кинетики сгорания отложенного кокса показало, что СО и СО,, являются первичными продуктами сгорания углерода. Отношение СО/СО2 почти не зависит от того, в какой форме находится углерод; оно составляет 0.3-0.9 и растет с температурой процесса. Общая скорость сгорания углерода в закоксованном катализаторе определяется или кинетикой окисления С в порах гранулы, или диффузией кислорода в порах катализатора, а также одновременно кинетикой реакции и диффузией через поры. При увеличении температуры происходит переход от кинетической области сгорания кокса через переходную к диффузионной. Для катализаторов крекинга с размером частиц ~4 мм кинетическая область наблюдается до 475°С, диффузионная область начинается при температурах выше 625 °С. При низких температурах кислород имеет доступ ко всем местам выделения кокса по всему объему зерна. При высоких температурах процесс лимитируется диффузией кислорода сквозь поры.
Необходимо отметить, что при регенерации происходит не только выжигание кокса, но и изменение самого катализатора под действием окислительной среды. Катализатор при регенерации может менять структуру, химический состав, пористость и удельную поверхность.
Если дезактивация происходит вследствие осаждения металла из примесей в сырье, простая процедура окисления не годится. В этом случае катализатор выгружают из реактора и подвергают полной переработке.
В зависимости от природы отравляющих катализатор веществ или от причины потери активности разрабатываются методы регенерации катализаторов в промышленных условиях.
Регенерация контактных масс столь же специфична, как и их отравление.
В каждом случае выявляют причину снижения активности и изменения селективности катализатора и разрабатывают методы его регенерации.
Из возможных путей восстановления активности контактных масс наиболее существенными являются следующие:
. летучий яд может быть удален с поверхности катализатора током чистого газа, жидкости или повышением температуры.
. при химическом взаимодействии яд может перейти в нетоксичную, слабо адсорбированную форму.
. промывка катализаторов жидкими растворителями.
. обработка смесью газов, которые являются восстановителями или окислителями.
Пример. Катализаторы, потерявшие активность вследствие блокировки поверхности при коксообразовании, регенерируются путем выжигания кокса кислородом воздуха при 550-700оС.
От оксидов ванадия и никеля катализатор можно освободить растворением их в водных растворах неорганических кислот.
Промоторы
Промоторы - это вещества, которые сами не обладают каталитическими свойствами или мало активны, но при добавлении их к катализатору даже в небольшом количестве, увеличивают активность катализатора.
Промоторы в твердые катализаторы вводят в момент их синтеза.
Эффективность действия промотора зависит, прежде всего, от их количества. При оптимальном соотношении катализатора и промотора соблюдается максимальная активность. Повышенное количество промотора сверх оптимального могут приводить к снижению активности катализатора.
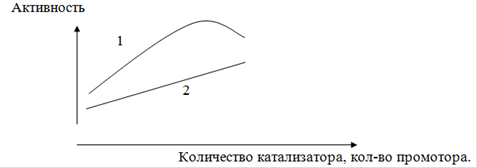
Рис. Зависимость активности катализатора от количества промотора. 1 - кривая активности катализатора.2 - кривая активности промотора.
Промоторы делятся на 2 группы:
- Текстурные, которые оказывают физическое воздействие в каталитической системе.
- Структурные, которые оказывают химическое воздействие в каталитической системе.
Текстурные промоторы присутствуют в катализаторе, как правило, в виде мелких частиц и оказывают тормозящее действие на спекание активной фазы.
Эффективность действия текстурного промотора напрямую связана с его дисперсностью, которая должна быть значительно выше, чем у собственно катализатора.
Пример: мелкие частицы Al вводят в железный катализатор синтеза аммиака, количество 0,5 - 1,5%; оксид хрома в катализатор синтеза ментола на основе оксида Zn 0,5 - 4% - предотвращает спекание.
Текстурные промоторы не изменяют энергию активности реакции.
Структурные промоторы изменяют химический состав катализатора. Механизм их действия очень сложен, и воздействие может идти следующими путями:
. промоторы могут ускорять образование промежуточных соединений.
. они могут создавать дефекты в кристаллической решетке.
. они могут изменять электронную структуру катализатора, т.е. облегчать присоединение или отрыв электронов.
. они существенно меняют энергию активации.
Модификаторами называются такие вещества, которые при добавлении к катализатору меняют его активность по полиэкстремальной зависимости.
Активаторами называют вещества, которые вводят в реакционную смесь и которые изменяют активность катализатора. Они могут быть астехиометрическими и стехиометрическими компонентами.
Астехиометрические участвуют в химическом процессе в составе реакционной среды, но после окончания реакции выделяются в неизменном виде.
Стехиометрические сами участвуют в каталитическом процессе, изменяют скорость реакции и сами участвуют в химическом превращении.
Смешанные катализаторы - в них практически все компоненты находятся в соизмеримых количествах, и являются активными в отношении данной реакции.
Составляющие смешанных катализаторов в процессе их приготовления могут реагировать между собой с образованием нового, более активного соединения (железо-молибденовый катализатор окисления метанола в формальдегид). В процессе приготовления образует молибдат железа - когда соотношение оксидов молибдена и железа равно 1,5:1, катализатор имеет определенную активность. При изменении соотношения получаем систему с избытком оксида или Fe, или Мо, и активность катализатора резко падает. Тоже самое происходит в железомедном катализаторе окисления серы, он состоит из соединений типа: CuFeO2, CuFeO4, что обеспечивает повышение активности, по сравнению с чистыми оксидами железа и меди.