1. К 1 мл мочи прибавляют 1 мл реактива, состоящего из 80 мл 10 %-го раствора серной кислоты и 20 мл 5 %-го раствора хлорида железа (III). При наличии аминазина и других производных фенотиазина в моче раствор приобретает розовато-лиловую окраску.
2. К 1 мл мочи прибавляют 1 мл реактива ФПН. Появление розовой окраски указывает на наличие аминазина или других производных фенотиазина в моче.
Приготовление реактива ФПН (см. Приложение 1, реактив 45).
Обнаружение аминазина
Реакция с концентрированной серной кислотой. Аминазин с концентрированной серной кислотой дает пурпурно-красную окраску.
Реакция с концентрированной азотной кислотой. При взаимодействии аминазина с концентрированной азотной кислотой возникает пурпурно-фиолетовая окраска.
Реакция с концентрированной соляной кислотой. Аминазин с концентрированной соляной кислотой дает розовато-фиолетовую, переходящую в красно-фиолетовую окраску.
Реакция с реактивом Марки. Аминазин под влиянием реактива Марки приобретает пурпурную окраску.
Реакция с реактивом Манделина. Аминазин с этим реактивом дает зеленую окраску, переходящую в пурпурную.
Обнаружение аминазина методом хроматографии. На хроматографическую пластинку наносят исследуемый раствор и раствор «свидетель» (спиртовой раствор аминазина). Пластинку подсушивают на воздухе, а затем вносят в камеру для хроматографирования, насыщенную парами системы растворителей (смесь бензола, диоксана и аммиака 75: 20:5). После того как жидкость поднимется на 13 см выше линии старта, пластинку вынимают из камеры высушивают на воздухе и опрыскивают реактивом Марки или свежеприготовленной смесью концентрированной азотной кислоты и этилового спирта (1:9). При наличии аминазина пятна на пластинке приобретают розово-фиолетовую окраску.
Приготовление хроматографических пластинок (см. Приложение 2, способ 7).
Обнаружение аминазина по УФ- и ИК-спектрам. Аминазин в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 255 и 307 нм. Сульфоксид аминазина, являющийся метаболитом этого препарата, в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 239, 274, 300 и 341 нм.
В ИК-области спектра основание аминазина (диск с бромидом калия) имеет основные пики при 1561, 1455, 1402, 1240, 747 см -1.
Задача 2. В клинико-токсикологическую лабораторию Центра лечения отравлений поступили объекты (кровь, моча) гр. В. Предполагается отравление анальгином. Представить формулу вещества, описать физико-химические свойства. Выбрать объекты и описать изолирование. Предложить схему ХТА.
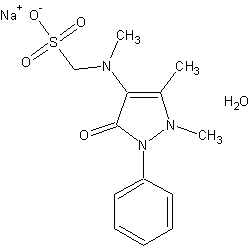
натрия 2,3-диметил-1-фенил-4-метиламинопиразолон-5-N-метансульфоната гидрат.
Анальгин – ненаркотический анальгетик.
Эмпирическая формула – C13 H16 O4 N3 SNa·H2 O – белый, слегка желтоватый кристаллический порошок, легко растворим в воде (1:1,5), трудно в спирте. Водный раствор прозрачен и нейтрален на лакмус. При стоянии желтеет, не утрачивая активности.
Анальгин – лучший препарат среди соединений пиразолонового ряда. Превосходит все анальгетики пиразолонового ряда. Малотоксичен. Анальгин входит в состав многих препаратов.
Для изолирования анальгина (и его метаболитов) из крови использовали метод экстракции органическим растворителем. Стандартный раствор анальгина готовили из порошка с содержанием анальгина 99,4% путем растворения в 0,1М хлористоводородной кислоте. Раствор разделяли на 2 части. Одну часть помещали в ампулу, запаивали, нагревали 30 минут на кипящей водяной бане. На спектрофотометре Cary 50 при 258нм строили калибровочный график. Раствор сравнения - 0,1М хлористоводородная кислота. Толщина слоя 1см.
Основная сложность при исследовании объектов судебно-химического анализа заключается в быстром метаболизме препарата. Основные метаболиты: 4-метиламинофеназон, 4-аминофеназон, 4-формиламинофеназон, 4-ацетиламинофеназон. Максимальное число метаболитов обнаруживается в моче.
Качественные реакции:
1. с р-ром FeCl3: антипирин – красное окр-е, амидопирин – фиол-е, исчезающее при избытке р-ва, анальгин – синее à крас à исчез.
2. с азотистой к-той: антипирин – зеленое окр-е, амидопирин – фиол-е.
3. Анальгин + резорцин – при нагревании – роз-е окр-е. (Ауриновый краситель)
Задача 3. В судебно-химическое отделение поступили объекты (печень с желчным пузырем, почка, желудок, кровь, моча) трупа гр. А. Диагноз – отравление неизвестным лекарственным веществом. Предложить схему ХТА.
· В результате ХТА обнаружен пахикарпин в печени, почке, крови и моче.
Пахикарпин – алкалоид, производное пиперидина.

Пахикарпин не кумулируется в организме. Уже через 6 ч после приема пахикарпина его можно обнаружить в неизмененном виде в моче. За сутки пахикарпин почти полностью выводится из организма.
Пахикарпин - основание растворяется в воде. Растворимость увеличивается с повышением температуры: при 25° растворяется 0,819%, при 35° - 0,936%, лри 50°-1,17%. Хорошо растворяется в общеупотребительных органических растворителях. Перегоняется с водяным паром.
Для изолирования пахикарпина из биологического материала при химико-токсикологических исследованиях применяют извлечение подкисленным спиртом или подкисленной водой.
В. П. Крамаренко и С. У. Закалик изучали возможность изолирования пахикарпина из биологического материала водой, подкисленной до рН-2,5 серной кислотой. В качестве органических растворителей для экстрагирования алкалоида сравнивали изоамиловый спирт, хлороформ, дихлорэтан и бензол. В случае экстрагирования хлороформом и изоамиловым спиртом им удавалось определить 80-90% пахикарпина, содержащегося в водном растворе. Максимум экстрагирования достигается при рН-9,8-10,8.
Н. И. Вестфаль разработала быстрый метод изолирования пахикарпина электродиализом, а В. В. Михно - электрофорезом. Метод электродиализа позволяет обнаружить 1-2 мг пахикарпина в 100 г биологического материала.