Результатом исследования пластовых проб газа и нефти является в первую очередь их компонентный состав (т.е. количественный состав), зная который можно рассчитать практически все физико-химические свойства нефти и газа, используемые в расчетах по технологии добычи.
Количества вещества n - характеризует число структурных элементов в данном веществе (атомов, молекул, других частиц). Единицей количества вещества в системе СИ является 1 моль. 1 моль - это такое количество вещества, в котором содержится столько же структурных элементов, сколько атомов в 12 г изотопа углерода-12. Согласно закону Авогадро, 1 кмоль любого газа занимает при нормальных условиях объем 22,414 м3, называемый нормальным молекулярным объемом. Соответственно стандартный молекулярный объем равен 24,05 м3.
Компонентный состав нефтяного газа может быть выражен в молекулярных, массовых долях и процентах. Молекулярная доля компонента в смеси газов при нормальных условиях практически точно совпадает с объемной долей этого компонента. Если задан объемный состав газа (смеси), то его можно пересчитать в массовый состав по формуле:
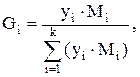 (1)
(1)
где Gi - массовая доля (доли единицы или проценты) компонента i в смеси; yi - объемная (молекулярная) доля компонента в смеси; Мi - молекулярная масса i-ого компонента; k - число компонентов.
При этом, если объемный состав задан в процентах, то его можно принять за 100 молей. Тогда доля каждого компонента в процентах будет выражать число его молей.
Если состав задан в массовых долях или массовых процентах, то его можно пересчитать в объемные доли или проценты по уравнению:
 (2)
(2)
где Ni = Gi / Mi - число молей i - го компонента в смеси.
Если массовый состав смеси выражен в процентах, то его удобно принять за 100 кг и для определения числа молей каждого компонента необходимо его массу (численно равную процентному содержанию в смеси) разделить на его молекулярную массу. Часто при расчетах необходимо знать среднюю молекулярную массу, а также плотность (и относительную по воздуху) плотность попутного и нефтяного газа. Средняя молекулярная масса газа по данным его объемного (молекулярного) состава равна:
 (3)
(3)
если объемная доля yi задана в процентах,
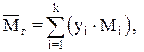 (4)
(4)
если объемная доля yi задана в долях единицы.
Средняя молекулярная масса газа по данным его массового состава рассчитывается по формулам:
 , (5)
, (5)
если массовая доля Gi задана в процентах,
 , (6)
, (6)
если массовая доля Gi задана в долях единицы.
Средняя плотность газа по вычисленной средней молекулярной массе при нормальных условиях равна:
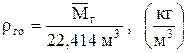 ; (7)
; (7)
при стандартных условиях соответственно
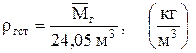 . (8)
. (8)
Относительная плотность газа по воздуху определяется как
 , (9)
, (9)
где 1,293 кг/м3 - плотность воздуха при нормальных условиях; 1,205 кг/м3 - плотность воздуха при стандартных условиях.
В таблице 1 приведены некоторые физические параметры компонентов природных газов, часто используемые при технических расчетах.
Таблица 1 Физико-химические свойства компонентов природных газов
| Параметры | СН4 | С2Н6 | С3Н8 | i-С4Н10 | n-С4Н10 | i-С3Н12 |
| Молекулярная масса | 16,043 | 30,070 | 44,097 | 58,124 | 58,124 | 72,151 |
| Газовая постоянная, Дж/(кг·К) | 523,3 | 288,8 | 217,7 | 188,4 | 188,4 | 159,1 |
| Температура кипения при нормальном давлении, °С | - 161,3 | - 88,6 | - 42,2 | - 10,1 | - 0,5 | +28,0 |
| Критические: | ||||||
| температура, °К | 190,7 | 306,2 | 369,8 | 407,2 | 425,2 | 461,0 |
| абсолютное давление, МПа | 4,7 | 4,9 | 4,3 | 3,7 | 3,8 | 3,3 |
| коэффициент сжимаемости | 0,290 | 0,285 | 0,277 | 0,283 | 0,274 | 0,268 |
| плотность, кг/м3 | 2,0 | 210,0 | 225,5 | 232,5 | 225,8 | - |
| Плотность при нормальных условиях, кг/м3 | 0,717 | 1,344 | 1,967 | 2,598 | 2,598 | 3,220 |
| Относительная плотность по воздуху | 0,5545 | 1,038 | 1,523 | 2,007 | 2,007 | 2,488 |
| Динамическая вязкость при нормальных условиях, мПа·с | 0,0103 | 0,0083 | 0,0075 | 0,0069 | 0,0069 | 0,0062 |
| Удельная теплоемкость при нормальных условиях, Дж/(кг·К): | ||||||
| при постоянном давлении Ср | 2219,0 | 1729,1 | 1574,2 | 1494,7 | 1494,7 | 1452,8 |
| при постоянном объеме Сv | 1695,7 | 1440,3 | 1356,5 | 1306,3 | 1306,3 | 1293,7 |
Продолжение таблицы 1
| Отношение теплоемкостей при 273 °К Ср/Сv | 1,309 | 1,200 | 1,160 | 1,144 | 1,144 | 1,123 |
| Теплопроводность при 273 ºК, Вт/(м·К) | 0,0300 | 0,0180 | 0,0148 | 0,0135 | 0,0135 | 0,0128 |
| Параметры | n-С5Н12 | С6Н14 | СО2 | Н2S | N2 | Н2О |
| Молекулярная масса | 72,151 | 88,178 | 44,011 | 34,082 | 28,016 | 18,016 |
| Газовая постоянная, Дж/(кг·К) | 159,1 | 138,0 | 192,6 | 259,5 | 297,3 | 502,5 |
| Температура кипения при нормальном давлении, °С | + 36,2 | + 69,0 | - 78,5 | - 61,0 | - 195,8 | + 100,0 |
| Критические: | ||||||
| температура, °К | 470,4 | 508,0 | 304,2 | 373,6 | 126,2 | 647,1 |
| абсолютное давление, МПа | 3,4 | 3,1 | 7,4 | 9,0 | 3,4 | 22,1 |
| коэффициент сжимаемости | 0,269 | 0,264 | 0,274 | 0,268 | 0,291 | 0,230 |
| плотность, кг/м3 | 232,0 | - | 468,0 | - | 310,6 | - |
| Плотность при нормальных условиях, кг/м3 | 3,220 | 3,880 | 1,977 | 1,539 | 1,251 | 0,805 |
| Относительная плотность по воздуху | 2,488 | 2,972 | 1,520 | 1,191 | 0,970 | 0,622 |
| Динамическая вязкость при нормальных условиях, мПа·с | 0,0062 | 0,0059 | 0,0138 | 0,0117 | 0,0166 | 0,0128 |
| Удельная теплоемкость при нормальных условиях, Дж/(кг·К): | ||||||
| при постоянном давлении Ср | 1452,8 | 1410,0 | 845,7 | 1063,4 | 1042,5 | 2009,7 |
| при постоянном объеме Сv | 1293,7 | 1272,0 | 653,1 | 803,9 | 745,2 | 1507,2 |
| Отношение теплоемкостей при 273 °К Ср/Сv | 1,123 | 1,108 | 1,295 | 1,323 | 1,399 | 1,333 |
| Теплопроводность при 273 ºК, Вт/(м·К) | 0,0128 | - | 0,0137 | 0,0119 | 0,0238 | - |