ЛАБОРАТОРНЫЕ РАБОТЫ
БОЛЬШОГО ПРАКТИКУМА
ПО ФИЗИОЛОГИИ ЧЕЛОВЕКА
И ЖИВОТНЫХ
Раздел — Электрофизиология
Часть 1. Физиология возбудимых структур
Нижний Новгород 2007
УДК 591.1
Лабораторные работы большого практикума по физиологии человека и животных. Раздел — Электрофизиология. Часть 1. Физиология возбудимых структур. Периферические нервы/Составители: В. Н. Крылов, Л. В. Ошевенский. Н. Новгород: ИНГУ, 1998. 45с.
Составители:
профессор, док. биол. наук В. Н. Крылов.
доцент, канд. биол. наук Л. В. Ошевенский.
Рецензент:
доцент, канд. биол. наук В. Г. Ретивин.
Методическое руководство предназначено для студентов старших курсов, проходящих практические занятия в рамках общего курса "Физиология человека и животных". Практические работы, включенные в данную методическую разработку, затрагивают раздел электрофизиологии, в частности, физиологию возбудимых структур (периферические нервы).
© Нижегородский государственный университет им. Н. И. Лобачевского, 1998
Биологическая мембрана
Композитная структура образующая наружную оболочку всех животных клеток, а также участвующая в формировании внутриклеточных органелл – называется биологической мембраной.
Биологические мембраны формируют замкнутые структуры и обеспечивают разделение внешней и внутренней среды. При этом мембраны выполняют барьерную функцию, препятствуя свободной диффузии веществ, регулируя процесс переноса веществ и соответственно их концентрацию.
Мембраны формируют внутриклеточную среду, и обеспечивают высокую сбалансированность протекания метаболических процессов.
Помимо граничной функции мембраны, обеспечивают: 1) внешнюю рецепцию физических и химических эффекторов поверхностными молекулами и преобразованием информации регуляторными мембранными белками; 2) обладают высокой ферментативной активностью за счет встроенных молекул ферментов; 3) обеспечивают транспорт электронов и фосфорилирование в цепи дыхания; 4) ферментативные процессы синтеза секретируемых продуктов; 5) преобразования внешних стимулов в электрические сигналы; 6) проведение биоэлектрических импульсов; 7) высвобождение синоптических нейромедиаторов.
Состав мембран
На (рис 1) представлена трехмерная схема модели биологической мембраны, которая наиболее наглядно демонстрирует ее морфо – функциональные свойства.
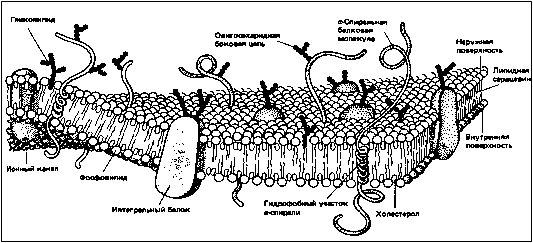
Рис1 Трехмерная схема жидко – мозаичной модели мембраны Сингра – Николсона.
Матрикс мембраны представлен липидами, это фосфоглицериды (фосфатидилэтаноламин, фосфатидилхолин) и сфинголипиды (сффингомиелин). Эти соединения амфифильны т. е. имеют полярные головки и неполярные хвосты.
Группировки образующие полярные головку, гидрофобны (имеют сродство к воде), а неполярные хвостовые группы гидрофобны (не растворимы в воде).
Двойственная природа мембранных липидов образует бислой и позволяет организовать пограничные разделы в водных растворох, что служыт основой организации клеток и клеточных структур. Внутренний гидрофобный участок бислоя обеспечивает интеграцию в мембрану неполярных веществ и участков других образующих мембрану группировок.
Так для повышения вязкости мембран в состав гидрофобного участка бислоя встроены молекулы стерола что повышает жесткость мембраны и снижает ее текучесть, что является основой разнообразия и постоянства формы клеток и их органелл.
Мембраные белки, это элементы формирующие функциональные свойства мембран. Ферментативную активность определяют флавопротеины и цитохромы белки веутренней мембраны митохондрий, АТФазы, участвующие в активном транспорте, аденилаткиназа, которая катализирует превращение АТФ в цАМФ.
Белки не обладающие ферментативной активностью образуют ионные каналы, являются рецепторами связывающие гормоны, нейромедиаторы и другие эффекторы.
Белки мембран часто создают комплексные связи с липидами образуя липопротеины, что расширяет их функциональные свойства.
Одним из наиболее важным свойством биологической мембраны является ее проницаемость, точнее сказать полупроницаемость или перенос веществ через мембрану.
Пассивный, не энергозависимый перенос веществ через мембрану осуществляется в основном тремя путями, определяется физико-химическими свойствами растворенных веществ и растворителя.
Вещества, находящиеся в водной фазе по одну сторону мембраны, растворяются в липидном слое мембраны, диффундируют и переходят в водную фазу с противоположной стороны мембраны.
Растворенные вещества диффундируют через заполненные водой поры.
Молекулы вещества связываются с молекулами-переносчиками встроенными в липидный слой мембраны, и диффундируют в водную фазу с противоположной стороны мембраны из молекулы-переносчика.
Ионные мембранные каналы.
Мембранные каналы образованы белками, погруженными в мембрану, где образуют заполненные водой поры. Через канал диффундируют малые молекулы. Они движутся по градиенту концентрации. Движение молекул по каналу определяется как их размерами так и зарядом. Мембранные каналы обладают относительной избирательностью по отношению к типу молекул, которые через них проходят. Существуют, например, калиевые и кальциевые каналы, каждый из которых непроницаем практически для любого иона, кроме специфического. Такая селективность обусловлена зарядом или структурой стенки канала.
Калиевый канал
Калевый ионный канал имеет свой индивидуальный энергетический профиль, при чем этот профиль динамически изменяется при транспорте иона, что регулирует производительность канала при взаимодействии со средой. На (рис2) представлена схема калиевого канала, где четыре отрицательных заряда зафиксированы на стенке канала. При чем предполагается, что конформация канального белка осциллирует и тем самым облегчается связывание транспортируемого иона и прохождение его через канал.
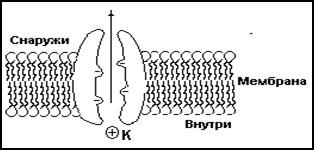
Рис 2 Схема белка образующего калиевый канал, погруженный в бислой плазматической мембраны.
Потенциал - зависимый патриевый канал
Ионные каналы другого типа обеспечивают транспорт ионов при наличии эффекторного воздействия. К таким каналам относятся потенциал - зависимые натриевые каналы, участвующие в генерации и распространении потенциала действия в нервной системе и рецептор - зависимые каналы синапсов.
На (рис 2, 3, 4) представлена схема потенциал - зависимого натриевого канала и его состояние при возбуждении.
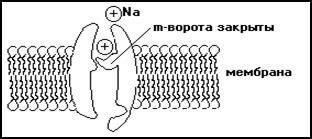
Рис. 3 Схема белка образующего натриевый канал в состоянии покоя
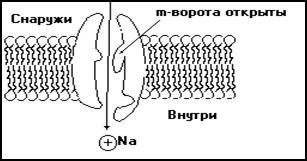
Рис.4 Схема белка образующего натриевый канал при возбуждении – деполяризация мембраны
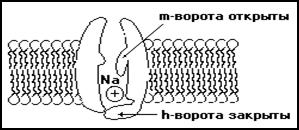
Рис.5 Схема белка образующего натриевый канал при возбуждении – деполяризация – реполяризация мембраны
Натриевые каналы активируются (т. е. открываются и пропускают ионы) в ответ на деполяризацию мембраны, при этом они проявляют высоко избирательную проницаемость для Li+ и Na+ по сравнению с другими ионами. Такое свойство обусловлено особой структурой каналов, благодаря которой они играют роль избирательных (селективных) фильтров. Поскольку в норме ионы лития в организме практически отсутствуют, весь ток, проходящий через эти каналы, переносится ионами Na +; ионы же Са2+ и К+ через них почти не проходят.
Процессы, приводящие к открыванию или закрыванию каналов, описывают воротными механизмами.
В покое натриевый канал механически перекрыт некой заряженной структурой (рис.3). При деполяризации мембраны конформация этой структуры изменяется, и канал открывается (рис.4). Главный аргумент в пользу того, что в мембране действительно происходят подобные механические конформационные перестройки, - это регистрация так называемых воротных токов, возникающих при открывании и закрывании натриевых каналов. Эти очень слабые токи можно обнаружить, если активировать натриевые каналы, предварительно заблокировав их с помощью фармакологических препаратов с тем, чтобы через них не мог протекать мощный ионный ток. Полагают, что воротные токи связаны с перемещением заряженных группировок, приводящим к открыванию активационных ворот (m-ворот) при активации каналов.
Здесь может возникнуть вопрос, каким же образом деполяризация мембраны приводит к открыванию потенциал - зависимых каналов? Представим себе типичную возбудимую клетку в состоянии покоя. Ее мембранный потенциал составляет — 75 мВ. Деполяризация на 50 мВ (т. е. до — 25 мВ) обычно приводит к активации большей части натриевых каналов, расположенных в мембране. Эти каналы представляют собой молекулы белка, вкрапленные в мембранный липидный бислой толщиной порядка 5 нм. Значит, при деполяризации на 50 мВ в этом бислое (а следовательно, и в расположенных в нем воротных белках) возникает изменение напряжения 10~3 В на 10 ~8 см, т.е. 100000 В/см. Неудивительно, что заряженные группировки белков-каналов «чувствуют» такие изменения напряженности поля и отвечают на них конформационными перестройками каких-то участков белковых молекул.
Считают, что эти конформационные перестройки и лежат в основе воротных процессов, управляющих электровозбудимыми каналами.
При длительной деполяризации натриевые каналы инактивируются. Инактивация развивается в мембране автоматически, и степень ее зависит от мембранного потенциала и времени. Постоянная времени инактивации составляет менее 2 мс. Инактивацию можно подавить, введя в цитоплазму протеолитические ферменты. Это позволяет думать, что в инактивации принимает участие некая белковая структура, расположенная у внутреннего входа натриевого канала - инактивационных ворот (h-ворот). h-Ворота закрываются через несколько миллисекунд после открывания m-ворот (рис.5). По-видимому, закрывание h-ворот зависит от пребывания m-ворот в открытом состоянии.
Тетродотоксин (ТТХ) - вещество, выделенное из внутренних органов иглобрюха (рыбы, обитающей у берегов Японии), способен внедряться в натриевые каналы и блокировать их. Опыты, проведенные на различных видах нервов, показали, что натриевые каналы на участке мембраны аксона площадью 1 мкм2 связывают менее 100 молекул ТТХ. При этом полностью подавляется увеличение натриевой проводимости, возникающее в норме при деполяризации.
Кинетические особенности блокирования каналов свидетельствуют о том, что каждая молекула ТТХ связывается с одним натриевым каналом. Значит, число каналов на 1 мкм2 мембраны составляет менее 100. Если бы все эти каналы открывались одновременно, то площадь их сечения должна была бы составлять менее 1 50000 от поверхности мембраны, если считать, что диаметр канала составляет порядка 0,5 нм. То, что на долю канала приходится столь малая часть поверхности мембраны, вполне согласуется с моделями клеточных оболочек Даниелли и Сингера.
Согласно этим моделям, низкая проницаемость мембраны для полярных молекул обусловлена тем, что большую ее часть занимает сплошной липидный бислой. Чрезвычайно малая площадь канала объясняет также и то, почему при тех значительных изменениях проводимости,
которые наблюдаются при возбуждении мембран, не происходит каких-либо существенных изменений емкости мембраны.
В 1980г. Фредерик Сигворс и Эрвин Неер с помощью так называемого метода локальной фиксации (patch-clamp) смогли зарегистрировать ток через одиночный натриевый канал, активированный с помощью деполяризации.
Для этого они использовали микропипетку диаметром 0,5 мкм, в кончик которой втягивали участок мембраны для создания тесного контакта между пипеткой и мембраной. Оказалось, что токи через одиночные каналы подчиняются закону «все или ничего», имеют прямоугольную форму (это свидетельствует об очень быстром открывании и закрывании каналов) и одинаковы по величине для разных каналов. При этом длительность пребывания каналов в открытом состоянии варьирует случайным образом и довольно широко. Среднее время нахождения канала в открытом состоянии составляет менее 1 мс и зависит от мембранного потенциала: при смещении деполяризующего потенциала в положительную сторону это время уменьшается. В то же время проводимость одиночных натриевых каналов слабо зависит от напряжения и равна примерно 10 пСм (что соответствует сопротивлению 1011 Ом). Используя закон Ома, постоянную Фарадея и число Авогадро, находим, что при Vм — ENa = -100 мВ (примерно такова электродвижущая сила для Na+ в начале развития ПД) активированные натриевые каналы пропускают примерно 6000 ионов натрия за 1 мс.
Число каналов, открытых в каждый момент времени, зависит от мембранного потенциала, а также от времени, поскольку от времени зависят процессы, приводящие к активации и инактивации каналов.
Таким образом, суммарные, зависящие от потенциала и времени изменения натриевой проводимости мембраны порождаются воротными процессами в тысячах натриевых каналов, каждый из которых в ответ на деполяризацию открывается и закрывается в соответствии с определенными
вероятностными закономерностями