Содержание
1. Патология коры надпочечников. Гиперкортизолизм.............................................2
2. Альдостеронизм.........................................................................................................5
3. Адреногенитальный синдром...................................................................................7
4. Острая и хроническая недостаточность коры надпочечников...............................10
5. Патология щитовидной железы................................................................................13
Патология коры надпочечников
В клинике патология надпочечников проявляется в виде ряда важнейших синдромов:
ГИПОФУНКЦИЯ:
Острая и хроническая, первичная или вторичная недостаточность над- почечников (кортикостероидная недостаточность);
ГИПЕРФУНКЦИЯ:
1. Тотальная (болезнь Иценко-Кушинга);
2. Частичная:
а) альдостеронизм;
б) гиперкортизолизм;
в) адреногенитальный синдром;
г) гиперфункция мозгового вещества.
Гиперкортизолизм
Гиперпродукция глюкокортикоидов может иметь: центральное, регуляторное происхождение, связанное с избытком АКТГ, выражающееся в первичной гиперфункции коры надпочечников.
Кроме того, встречаются эктопические очаги продукции подобных АКТГ веществ в злокачественных опухолях различных органов.
Центральный гиперкортицизм представлен болезнью Иценко-Кушинга, возникающей при базофильной аденоме гипофиза или избыточной продукции гипоталамусом кортиколиберина. Усиленное образование АКТГ приводит к чрезмерной стимуляции пучковой и сетчатой зон надпочечников и их двусторонней гиперплазии. Основные проявления болезни Иценко— Кушинга связаны с гиперпродукцией глюкокортикоидов.
Симптоматика болезни весьма разнообразна, так как связана с избыточностью многочисленных эффектов глюкокортикоидов. а отчасти — и других гормонов коры надпочечников. Из неспецифических признаков больных беспокоят общее недомогание, слабость, повышенная утомляемость, головная боль, боли в ногах, спине, сонливость, жажда. Весьма характерен внешний вид больного — круглое, «лунообразное», багрово-красное лицо, умеренный гипертрихоз (у женщин), диспластическое ожирение с преимущественным отложением жира в области лица, шеи, верхней половины туловища при непропорционально худых конечностях. Весьма характерны атрофические западающие багрово-красные или фиолетовые полосы растяжения (стрии) на коже живота, плеч, молочных желез, внутренней поверхности бедер. Часто выявляется остеопороз, нередко приводящий к патологическим переломам позвонков, шейки бедра и др. «Стрии» и костные изменения связывают с белково-катаболическим и антианаболическим действием избытка глюкокортикоидов.
Как правило, значительно страдает сердечно-сосудистая система. Развивается стойкая высокая артериальная гипертензия с вторичными нарушениями, свойственными данному виду патологии: расстройством мозгового кровообращения, ретинопатией, сморщенной почкой, перегрузочной формой сердечной недостаточности. В генезе кардиальных нарушений существенное значение может иметь так называемая электролитно-стероидная кардиопатия, связанная с электролитными сдвигами в миокарде, увеличением внутриклеточного натрия и уменьшением калия.
Таким образом, перегрузочная форма сердечной недостаточности сочетается с миокардиальной. Наряду с указанными проявлениями при болезни Иценко— Кушинга часто наблюдается снижение устойчивости к инфекционным заболеваниям, гнойничковым поражениям кожи, инфекциям мочевыводящих путей и др. Это связано с иммунодепрессивным действием избытка глюкокортикостероидов. Как правило, при болезни Иценко—Кушинга наблюдается гипергликемия и нередко — сахарный диабет. В основе данных нарушений лежат гиперглике-мизирующее и «контринсулярные» свойства глюкокортикостероидов.
В периферической крови обнаруживаются лимфопения, эозинопения, эритроцитоз. Нередко возникают различные нарушения в половой сфере, неврологическом и нервно-психическом статусе. Первично гландулярная (периферическая) форма гиперкортицизма, как было указано выше, может быть вызвана кортикостеромой — гормонально-активной опухолью коры надпочечников, исходящей из пучковой зоны и продуцирующей кортизол, или злокачественной (раковой) опухолью. Название этого варианта гиперкортицизма иногда не дифференцируют от центральной, гипоталамо-гипофизарной формы заболевания. Однако в связи с явными различиями в этиологии, патогенезе, некоторых решающих диагностических признаках и терапевтических подходах в настоящее время признается целесообразным использовать понятие и термин «болезнь Иценко—Кушинга» применительно к центральным, гипоталамо-гипофизарным формам гиперкортицизма, а периферическую, первично-гландулярную форму обозначать термином «синдром Иценко— Кушинга».
Внешние проявления синдрома Иценко—Кушинга весьма сходны с симптоматологией болезни Иценко — Кушинга. Принципиальное различие заключается в том, что для болезни Иценко —Кушинга характерно сочетание гиперкортицизма с высоким уровнем АКТГ; при синдроме Иценко— Кушинга продукция АКТГ по механизму обратной связи подавлена первичным избытком глюкокортикостероидов и уровень АКТГ в крови понижен.
Принципиальным отличием синдрома и болезни Иценко—Кушинга является также то, что во втором случае обнаруживается двусторонняя диффузная гиперплазия надпочечников, а при синдроме Иценко — Кушинга (аденоме или карциноме) — одностороннее увеличение с атрофией другого надпочечника, вызванной избытком глюкокортикостероидов, продуцируемых опухолью.
Своеобразная форма гиперкортицизма, не связанная с нарушением гормонообразования в коре надпочечников, иногда встречается при поражениях печени (циррозах и др.). В нормальных условиях большая часть образовавшегося в надпочечниках кортизола (до 80%) образует в крови комплекс со специфическим кортико-стероидсвязывающим глобулином — транскортином, до 10% кортизола связано с альбуминами и не более 10 % кортизола плазмы находится в свободном состоянии и проявляет свою биологическую активность. При поражении печеночных клеток синтез транс-кортина нарушается, что может привести к увеличению свободной фракции кортизола в крови и возникновению так называемого кушингизма — симптомокомплекса, сходного с синдромом Ипенко — Кушинга, хотя обычно менее ярко выраженным.
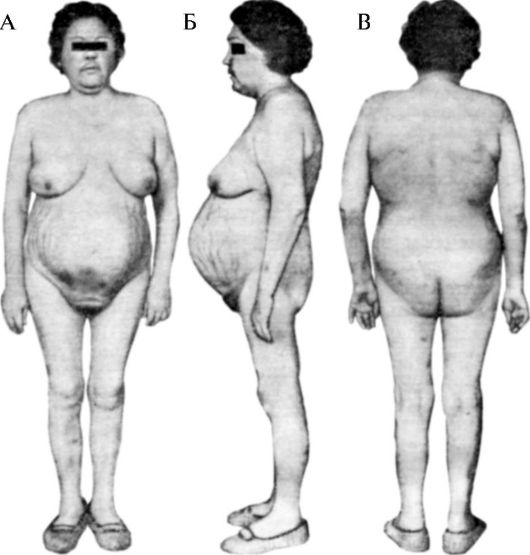
Рис.1. Больная с синдромом Иценко-Кушинга. Выглядит значительно старше своего возраста (30 лет). Перераспределение подкожной жировой клетчатки: отложение жира на животе (А, Б), истончение конечностей (А, Б, В), скошенность ягодиц (В), лунообразное лицо (Г).
Альдостеронизм
Различают две формы избыточной секреции альдостерона: первичный и вторичный гиперальдостеронизм.
Причиной первичного гиперальдостеронизма (синдром Конна) обычно является гормонально-активная опухоль, происходящая из клубочковой зоны — альдостерома. Проявления первичного гиперальдостеронизма сводятся к трем основным группам симптомов: сердечно-сосудистым, почечным, нервно-мышечным. Основными причинами этих нарушений служат почечная задержка натрия и потеря калия. Накопление натрия в клетках стенок сосудов приводит к их гипергидратации, сужению просвета, увеличению периферического сопротивления и повышению артериального давления. Артериальной гипертензии способствует также увеличение чувствительности сократительных элементов сосудистых стенок к действию прессорных аминов.
В результате гипертензии часто встречаются (особенно у детей) изменения глазного дна, приводящие к нарушению зрения вплоть до слепоты. Нередко наблюдаются нарушения ритма сердца, характерные для гипокалиемии изменения ЭКГ. В начальной стадии болезни суточный диурез понижен. Позднее олигурия сменяется стойкой полиурией, которая обусловлена дегенерацией эпителия почечных канальцев и снижением их чувствительности к АДГ. Как правило, существуют нарушения в нервно-мышечной системе — мышечная слабость, парестезии, судороги; иногда вялые параличи.
Вторичный гиперальдостеронизм может возникать при некоторых физиологических состояниях: сильном физическом напряжении, менструации, беременности и лактации, высокой внешней температуре с интенсивным потоотделением и др.
Патологический гиперальдостеронизм возникает при острой кровопотере, различных формах сердечной недостаточности, нефрозе с выраженной протеинурией и гипопротеинемией. В этих случаях усиленная продукция альдостерона связана с активацией ренин-ангиотензиновой системы в ответ на гиповолемию. Активация данной системы возникает и при заболеваниях почек, сопровождающихся их ишемией. Повышение уровня альдостерона при заболеваниях печени (в основном — циррозе) связано с тем, что этот гормон, как и многие другие, метаболизируется в основном в печени. Вторичный гиперальдостеронизм также проявляется задержкой натрия, артериальной гипертензией, гипергидратацией и некоторыми другими симптомами, свойственными первичному гиперальдостеронизму. Однако при этом в отличие от синдрома Конна в крови наблюдается высокий уровень ренина и ангиотензина; развиваются отеки, что связано с особенностями этиологии и патогенеза этих двух видов гиперальдостеронизма.
Адреногенитальный синдром
Адреногенитальный (кортикогенитальный) синдром (КГС). Данный вид расстройств функций коры надпочечников встречается в двух основных формах: врожденной вирилизирующей гиперплазии коры надпочечников и гормонально-активной опухоли — ан-дростеромы (андробластомы).
Врожденная форма кортико-генитального синдрома связана с нарушениями синтеза гормонов в коре надпочечников, в результате в кровь поступает избыточное количество стероидов с андрогенными свойствами. Основные проявления патологии обусловлены вирилизирующим и анаболическим действием данных гормонов. В этиологии врожденного кортико-генитального синдрома главную роль играет наследственность. Развитию данного заболевания могут способствовать также различные неблагоприятные факторы во время беременности матери (токсикоз, применение гормональных препаратов и др.).
В основе врожденного кортико-генитального синдрома лежит дефицит ферментов 21-гидроксилазы, 11-гидроксилазы и, возможно, 3-дегидрогеназы, участвующих в многоэтапном синтезе кортикостероидов.
Различают три клинические формы заболевания:
- простая вирилизирующая (от лат. virilis — мужской, свойственный мужчине; син.: андрогенизируюшая, маскулинизирующая) форма (наиболее частая);
- вирилизм с гипотоническим синдромом (сольтеряющая форма);
- вирилизм с гипертензивным синдромом (встречается редко).
Считается, что две первые формы связаны с дефицитом 21-гидроксилазы, а третья форма — с дефицитом 11-р-гидроксилазы. Во всех случаях нарушается синтез кортизола, кортикостерона и альдостерона, что сопровождается накоплением андрогенных предшественников и увеличением образования гипофизарного АКТГ. Последнее обусловлено по механизму обратной связи дефицитом кортизола: в то же время андрогены не обладают тормозящим влиянием на синтез АКТГ. Избыток АКТГ дополнительно стимулирует сетчатую зону, усиливая образование андрогенов и вызывая гиперплазию надпочечников. Из-за дефицита необходимых для синтеза кортизола ферментов стимулирующее влияние AKTT на пучковую зону и синтез кортизола реализоваться при этом не может.
Проявления кортико-генитального синдрома наиболее ярко выражены у женщин и в большинстве случаев обнаруживаются сразу после рождения (хотя встречаются и случаи значительно более позднего проявления признаков болезни).
Как правило, дети с этим заболеванием рождаются крупными в результате анаболического действия андрогенов. Если гиперпродукция андрогенов возникла на раннем этапе развития плода, изменения наружных половых органов у девочек выражены настолько резко, что бывает трудно установить пол новорожденного (женский псевдогермафродитизм). В случаях, когда избыток андрогенов проявляется только после рождения, наружные половые органы имеют нормальный вид и их изменение происходит постепенно по мере нарастания дисфункции надпочечников. Ранним признаком вирилизации у девочек является также появляющееся в возрасте 2 — 5 лет, а иногда и раньше, ненормальное, избыточное оволосение — гипертрихоз (или гирсутизм), рост волос на лобке, в подмышечных впадинах, на лице, спине, конечностях. В более поздние сроки избыток андрогенов сказывается и на строении тела девочек. В связи с усилением анаболизма вначале отмечается быстрый рост, однако в результате преждевременного окостенения эпифизов трубчатых костей рост вскоре прекращается и в конечном итоге обычно наблюдается низкорослость. Характерны чрезмерное развитие скелетной мускулатуры и большая физическая сила. При отсутствии или неэффективности лечения андрогенизация прогрессирует и девочки приобретают еще более мужеподобный вид, усиливается рост волос на лице (усы, борода) и теле, грубеет голос. Молочные железы не развиваются, менструации не наступают. У взрослых женщин также наблюдаются аменорея, атрофия матки и молочных желез, телосложение приближается к мужскому типу, часто появляется облысение. Имеются также определенные отклонения в поведенческих особенностях.
Мальчики с врожденной гиперплазией надпочечников обычно рождаются с нормальной дифференциацией наружных половых органов. В дальнейшем происходит раннее ложное половое созревание по изосексуальному типу: явно преждевременно развиваются вторичные половые признаки и наружные половые органы (макрогенитосомия). В то же время из-за торможения избытком андрогенов образования гипофизарных гонадотропинов половые железы остаются недоразвитыми и сперматогенез может полностью отсутствовать. Весьма характерен внешний вид больных: низкий рост, короткие нижние конечности и сильно развитая мускулатура (так называемый «ребенок-геркулес»).
При гипотензивной (сольтеряющей) форме кортико-генитального синдрома в связи с резким уменьшением продукции альдостерона наряду с описанными выше характерными признаками заболевания наблюдаются серьезные нарушения электролитного баланса: потеря натрия, гиперкалиемия, гипогидратация и, как следствие, артериальная гипотензия. Нередко развиваются кризы с судорогами и расстройствами гемодинамики вплоть до коллапса, иногда — со смертельным исходом.
Кортико-генитальный синдром с гипертензивным синдромом характеризуется значительным избытком дезоксикортикостерона, что ведет к стойкому повышению артериального давления. Имеются также отчетливые признаки вирилизации вплоть до псевдогермафродитизма у девочек и макро-генитосомии у мальчиков.
Нередко встречаются стертые формы кортико-генитального синдрома, проявляющиеся нерезко выраженными симптомами гиперпродукции андрогенов: умеренным гипертрихозом, нарушением менструального цикла и др.
Приобретенная форма КГС вызывается гормонально-активной опухолью — андростеромой, происходящей из сетчатой зоны надпочечников и продуцирующей большое количество андрогенов. Опухоль может носить доброкачественный или злокачественный характер и развиваться в любом возрасте.
Проявления заболевания у женщин весьма характерны и совпадают с врожденным кортико-генитальным синдромом. При раннем возникновении опухоли у мальчиков также имеются характерные признаки данного заболевания. У взрослых мужчин с нормально развитыми вторичными половыми признаками при возникновении андростеромы бывает трудно выявить прогрессирование вирилизма, в связи с чем заболевание часто своевременно не диагностируется. В отличие от врожденного кортико-генитального синдрома при андростероме обычно нет значительного повышения содержания АКТГ в плазме, но резко увеличено выделение с мочой 17-кетостероидов.

