Тема 5. Промышленный катализ (4 часа)
Каталитические процессы в настоящее время составляют основу химической технологии. Причем область их применения расширяется: около 90 % новых производств, освоенных за последние годы химической промышленностью, основаны на взаимодействии, протекающем в присутствии катализаторов.
В промышленности 90 % процессов являются каталитическими. ВВП США на 30 % определяется каталитическими технологиями, являющимися локомотивом экономически развитых стран.
КАТАЛИЗ (термин введен в 1835 г) – это изменение скорости реакции при воздействии веществ- катализаторов, которые участвуют в реакции, но не входят в состав продуктов.
Применение катализаторов облегчает практическое осуществление многих химических реакций; скорость некоторых из них увеличивается в тысячи и даже миллионы раз. Очень многие промышленные процессы удалось осуществить только благодаря применению катализаторов.
К числу каталитических процессов относятся важнейшие крупнотоннажные производства, например, такие как получение водорода, аммиака, серной и азотной кислот и многих других важнейших химических продуктов. Особенно велико и разнообразно применение катализа в технологии органических веществ и в производстве высокомолекулярных соединений.
Катализаторами могут быть вещества, находящиеся в любом из трех агрегатных состояний. К твердым катализаторам можно отнести металлы и их оксиды, например, железо Fe при синтезе аммиака, платину Pt при окислении аммиака, оксид ванадия V2O5 при окислении SO2, Al2O3 при крекинге нефтепродуктов и др.
Жидкими катализаторами служат обычно кислоты и основания, например, серная кислота H2SO4 и фосфорная кислота Н3РО4 применяются при алкилировании ароматических углеводородов, при изомеризации н-бутилена в изобутилен и др.
Примером газообразных катализаторов может служить BF3 в процессах полимеризации некоторых углеводородов.
Каталитические процессы можно разделить на две группы: гомогенные и гетерогенные.
· При гомогенном катализе катализатор и реагенты находятся в одной фазе в молекулярно дисперсном состоянии.
В гомогенно-каталитических реакциях скорость процесса зависит от концентрации не только реагирующих веществ, но и катализатора.
Основным недостатком гомогенного катализа является трудность выделения катализатора из конечной продукционной смеси, в результате чего часть катализатора теряется, а целевой продукт загрязняется. Однако в последнее время ведутся обширные исследования в области высокоактивных катализаторов гомогенного катализа, которые, присутствуя в малых дозах, вызывают цепные реакции. Поскольку количество вводимого катализатора невелико, после реакции он не извлекается из реакционной смеси, а остается в целевом продукте, не снижая качества получаемого целевого продукта.
Большой интерес к гомогенному катализу объясняется главным образом тем, что при подборе соответствующих катализаторов интенсивность гомогенных процессов очень высока. Это объясняется тем, что гомогенные реакции протекают на микроуровне (на уровне отдельных молекул), когда вероятность столкновения молекул реагирующих веществ с молекулами катализатора весьма значительная.
· При гетерогенном катализе катализатор образует самостоятельную фазу, отделенную границей раздела от фазы, в которой находятся реагенты. При этом катализатор не ускоряет диффузионных процессов и оказывает влияние только на скорость процессов протекающих в кинетических. областях.
В особую группу выделены микрогетерогенные и ферментативные каталитические процессы. Микрогетерогенный катализ происходит в жидкой фазе с участием коллоидных частиц металлов в качестве катализаторов. Ферментативный катализ наблюдается в биологических системах с участием сложных комплексов (часто белковой природы), называемых ферментами.
Общее представление о катализе
Каталитические реакции подчиняются общим законам химии и термодинамики, но имеют при этом свои особенности, так как в них всегда участвует один дополнительный компонент – катализатор. Действие катализаторов принципиально отличается от действия других факторов, способствующих интенсификации химических реакций, например, температуры, давления, радиационного воздействия и др. Повышение температуры может ускорять реакцию вследствие увеличения энергетического уровня реагирующих молекул, т.е. их активации за счет вводимого извне тепла. При этом изменяется внутренняя энергия системы и смещается положение равновесия.
Катализаторы – это вещества, которые многократно вступая в промежуточное взаимодействие с участниками реакции, изменяют её механизм и увеличивают скорость реакции. Они восстанавливают свой химический состав после каждого цикла промежуточных взаимодействии.
Для равновесных химических реакций катализатор (kat) не смещает положения равновесия, он лишь уменьшает время его достижения τ, равно ускоряя как прямую так и обратную реакцию.
Катализатор ускоряет хим. реакцию за счет изменения механизма реакции. Существует несколько теорий, объясняющих механизм действия катализаторов, из которых наиболее распространенной теорией, служащей основой современных представлений о катализе, является теория промежуточных соединений. Согласно этой теории, медленную реакцию между исходными веществами можно заменить двумя или несколькими более быстрыми реакциями с участием катализатора, который образует с исходными веществами промежуточные непрочные соединения. Ускоряющее действие катализатора состоит в понижении энергии активации реакций образующихся промежуточных соединений, что оказывает очень сильное влияние на скорость реакции, поскольку в уравнение Аррениуса
 энергия активации Е входит в показатель степени.
энергия активации Е входит в показатель степени.
Пусть протекает одностадийная реакция с энергией активации Eo
 A+B R
A+B R
 |
 Eo 1 2
Eo 1 2
E2
E1

 Ι E3 ΙΙ
Ι E3 ΙΙ

ход реакции
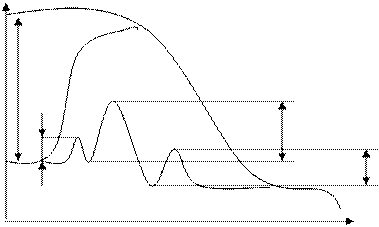
Энергетические диаграммы каталитической и не каталитической реакций:
Ι – энергетический уровень исходных реагентов
ΙΙ – энергетический уровень продуктов реакций
1 – путь каталитической реакции
2 – путь реакции без катализаторов
Ход реакции на энергетической диаграмме изображен кривой 2. В присутствии катализатора механизм реакции изменяется, она протекает через несколько последовательных стадий (кривая 1).
Первой стадией может быть образование промежуточного активированного комплекса Akat:
A+kat= Akat (1 стадия)
катализатор
Затем активированный комплекс реагирует со вторым реагентом В с образованием комплекса катализатора и продукта R:
Akat+B=Rkat (2 стадия)
Последней стадией является разложение комплекса Rkat c образование продукта R и высвобождением катализатора для нового каталитического цикла:
Rkat=R+kat (3 стадия)
 Каждая из этих последовательных стадий характеризуется своими значениями энергии активации E1,E2,E3 (кр.1), но, как правило, высота каждого из этих потенциальных барьеров ниже энергии активации Eo. Т.о. в присутствии kat реакция протекает по энергетически более выгодному пути, что позволяет проводить процесс с большей скоростью. Исходное (Ι) и конечное (ΙΙ) энергетические состояния реакционной системы в присутствии катализатора и без него остаются одинаковыми. кат-р не м/т изменить состояние химического равновесия, которое не зависит от пути реакции. Роль катализатора состоит в изменении скорости достижения состояния равновесия. Некоторые химические реакции без катализаторов практически неосуществимы, например, из за слишком большой энергии активации. Для преодоления высокого энергетического барьера можно повысить кинетическую энергию молекул, т.е. увеличить температуру. Но для многих обратимых экзотермических реакций (∆Н<0) повышение температуры приводит к смещению равновесия в обратную сторону и делает реакцию ТД неразрешенной. В таких случаях применение катализатора необходимо. Катализатор снижает Еакт реакции и позволяет тем самым проводить ее при существенно более низких температурах. Чрезвычайно важна роль катализаторов в осуществлении сложных реакций, т.к. катализаторы обладают способностью избирательно влиять на скорость только какой-то одной нужной реакции (крекинг нефтепродуктов – получение высококачественных бензинов)
Каждая из этих последовательных стадий характеризуется своими значениями энергии активации E1,E2,E3 (кр.1), но, как правило, высота каждого из этих потенциальных барьеров ниже энергии активации Eo. Т.о. в присутствии kat реакция протекает по энергетически более выгодному пути, что позволяет проводить процесс с большей скоростью. Исходное (Ι) и конечное (ΙΙ) энергетические состояния реакционной системы в присутствии катализатора и без него остаются одинаковыми. кат-р не м/т изменить состояние химического равновесия, которое не зависит от пути реакции. Роль катализатора состоит в изменении скорости достижения состояния равновесия. Некоторые химические реакции без катализаторов практически неосуществимы, например, из за слишком большой энергии активации. Для преодоления высокого энергетического барьера можно повысить кинетическую энергию молекул, т.е. увеличить температуру. Но для многих обратимых экзотермических реакций (∆Н<0) повышение температуры приводит к смещению равновесия в обратную сторону и делает реакцию ТД неразрешенной. В таких случаях применение катализатора необходимо. Катализатор снижает Еакт реакции и позволяет тем самым проводить ее при существенно более низких температурах. Чрезвычайно важна роль катализаторов в осуществлении сложных реакций, т.к. катализаторы обладают способностью избирательно влиять на скорость только какой-то одной нужной реакции (крекинг нефтепродуктов – получение высококачественных бензинов)