Согласно эмпирически установленному закону теплопроводности Фурье плотность теплового потока q пропорциональна градиенту температуры:
 вт/м2
вт/м2
Это означает, что тепловой поток направлен из области высоких температур в область низких температур.
Согласно кинетической теории идеального газа, состоящего из абсолютно упругих сфер коэффициент теплопроводности равен [8]

М – молекулярный вес газа,
R – 8314,4 Дж/кмоль * 0,
Т – температура, К,
σ – диаметр молекулы М,
Na – число Авагадро, 6,023*1026 шт./кмоль,
CV – удельная изохорная массовая теплоемкость, Дж/кг*0К,  ;
;
 , Ср – изобарная удельная теплоемкость, Дж/кг*0К.
, Ср – изобарная удельная теплоемкость, Дж/кг*0К.
Учет эффектов реального газа с помощью интеграла столкновений Ωλ дает:
 ;
;
Приведенный интеграл столкновений зависит только от приведенной температуры Т*, которая отпределяется как:
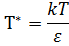
Температурная зависимость Ωλ показана на рис. 1п.
| 0,5 |
| Т* |
| Ωλ |
Рис.1.п. – Температурная зависимость Ωλ и Ω.
| 0,5 |
| Т* |
| Ωλ |
Таблица 1п.
| Газ | σ*109, м | ε/k, 0K | Газ | σ*109, м | ε/k, 0K | Газ | σ*109, м | ε/k, 0K |
| H | 0,205 | C2H6 | 0,432 | воздух | 0,371 | 78,6 | ||
| O | 0,275 | C3H8 | 0,498 | A2 | 0,354 | 93,3 | ||
| H2 | 0,292 | C2H2 | 0,403 | Hl | 0,255 | 10,22 | ||
| O2 | 0,346 | C2H4 | 0,416 | H2O2 | 0,42 | 389,3 | ||
| N2 | 0,362 | nC4H10 | 0,469 | OH | 0,314 | 79,8 | ||
| H2O | 0,26 | C4H10 | 0,528 | NO | 0,349 | 116,7 | ||
| CO | 0,365 | C6H6 | 0,535 | 412,3 | N2O | 0,383 | 232,4 | |
| CO2 | 0,376 | C6H12 | 0,618 | CH3OH | 0,363 | |||
| CH4 | 0,375 | C6H14 | 0,595 | 399,3 | C | 0,3385 | 30,6 |
Пример:
Определить λ воздуха при температуре Т=293 0К.
1.  кг/кмоль
кг/кмоль
2.  ,
,  (Рис. 1.п.), σ=3,711*10-10 м.
(Рис. 1.п.), σ=3,711*10-10 м.
3.  вт/м*град.
вт/м*град.
Теплоемкость  Дж/кг*град.
Дж/кг*град.
В таблице 2.п. данные справочные данные по некоторым характеристикам для воздуха в зависимости от температуры При Р=1 атм.
Таблица 2.п.
| Т, 0К | ρ, кг/м3 | Ср, кДж/кг 0К | М*107, Па*с | V*106, м2/с | λ*103, вт/м 0К | ϰ*105, м2/с | Р2 |
| 3,5562 | 1,032 | 71,1 | 2,0 | 9,34 | 2,54 | 0,786 | |
| 2,3364 | 1,012 | 103,4 | 4,426 | 13,8 | 5,84 | 0,758 | |
| 1,7458 | 1,007 | 132,5 | 7,59 | 18,1 | 10,3 | 0,737 | |
| 1,3947 | 1,006 | 159,6 | 11,44 | 22,3 | 15,9 | 0,72 | |
| 1,1614 | 1,007 | 184,6 | 15,89 | 26,3 | 22,5 | 0,707 | |
| 0,8711 | 1,014 | 230,1 | 26,41 | 33,8 | 38,3 | 0,69 | |
| 0,7740 | 1,021 | 250,7 | 32,39 | 37,3 | 47,2 | 0,686 | |
| 0,6964 | 1,03 | 270,1 | 38,79 | 40,7 | 56,7 | 0,684 | |
| 0,6329 | 1,04 | 288,4 | 45,57 | 43,9 | 66,7 | 0,683 | |
| 0,5804 | 1,051 | 305,8 | 52,69 | 46,9 | 76,9 | 0,685 | |
| 0,5356 | 1,063 | 322,5 | 60,21 | 49,7 | 87,3 | 0,69 | |
| 0,4975 | 1,075 | 338,8 | 68,1 | 52,4 | 0,695 | ||
| 0,4643 | 1,087 | 354,6 | 76,37 | 54,9 | 0,702 | ||
| 0,4354 | 1,099 | 369,8 | 84,93 | 57,3 | 0,709 | ||
| 0,3868 | 1,121 | 398,1 | 102,9 | 0,72 | |||
| 0,3482 | 1,141 | 424,4 | 121,9 | 66,7 | 0,726 | ||
| 0,3166 | 1,159 | 141,8 | 71,5 | 0,728 | |||
| 0,2902 | 1,175 | 162,9 | 76,3 | 0,703 | |||
| 0,2679 | 1,189 | 185,1 | 0,719 | ||||
| 0,2488 | 1,207 | 0,703 | |||||
| 0,2322 | 1,23 | 0,685 | |||||
| 0,2177 | 1,248 | 0,688 | |||||
| 0,2049 | 1,267 | 0,685 | |||||
| 0,1935 | 1,286 | 0,683 | |||||
| 0,1741 | 1,337 | 0,672 | |||||
| 0,1582 | 1,417 | 0,655 | |||||
| 0,1448 | 1,558 | 0,630 | |||||
| 0,1389 | 1,665 | 0,613 | |||||
| 0,1135 | 2,726 | 0,536 |
Видно, что коэффициент теплопроводности зависит от температуры за счет множителя Т1/2 и зависимости СV от температуры. Коэффициент теплопроводности не зависит от давления.
Для смеси газов коэффициент теплопроводности можно вычислить по коэффициентам теплопроводности λi и мольным долям xi индивидуальных компонентов i с точностью 10 - 20%, используя имперический закон:

Если требуется более высокая точность (5-10%), необходимо использовать более сложные формулы.
Например:

Где Фik зависят от коэффициентов вязкости μi и молекулярных весов Mi компонентов:

Теплопроводность твердых материалов и жидкостей следует брать из справочной литературы [1.п,2.п.]
Теплоемкость газов
Теплоемкость газов зависит от строения молекул и от температуры. По закону о распределении по степеням свободы молярная теплоемкость одноатомных газов равна:
 Дж/моль0 = 2,98 кал/моль0
Дж/моль0 = 2,98 кал/моль0
Поскольку для одноатомных газов существуют только поступательные степени свободы, которые всегда реализуются, то теплоемкость их не зависит от температуры.
По закону Майера:
 Дж/моль 0 = 4,967 кал/моль0
Дж/моль 0 = 4,967 кал/моль0
Массовые удельные теплоемкости определяются делением на молекулярный вес:

Газы состоящие из 2-х и более молекул имеют вращательные и колебательные степени свободы, которые возбуждаются по мере возрастания температуры. Эта зависимость выражается соотношением:
 или
или 
Таблица 3.п. дает сведения и зависимости Ср(Т) для различных газов.
Таблица 3.п.
| Вещество | Ср (298) Дж/моль0 | а | b*103 | C*106 | C1*10-5 | Дисперсия |
| СН4(г) | 35,71 | 14,32 | 74,66 | -17,43 | - | 298-1500 |
| С2Н2 | 43,93 | 26,44 | 66,65 | -26,48 | - | 298-1000 |
| С2Н4 | 43,56 | 11,32 | 122,01 | -37,90 | - | 298-1500 |
| С2Н6 | 52,64 | 5,75 | 175,11 | -57,85 | - | 298-1500 |
| С3Н8 | 73,51 | 1,72 | 270,75 | -94,48 | - | 298-1500 |
| С4Н10 | 97,45 | 18,23 | 303,56 | -92,65 | - | 298-1500 |
| С7Н16(ж) | 138,91 | - | - | - | - | - |
| С7Н16(г) | 165,98 | -215,56 | - | 298-1000 | ||
| С8Н18(ж) | 254,14 | - | - | - | - | - |
| С8Н18(г) | 188,87 | 11,84 | 666,51 | -244,93 | - | 298-1000 |
| Н2 | 28,83 | 27,98 | 3,26 | - | 0,5 | 298-3000 |
| N2 | 29,12 | 27,88 | 4,27 | - | - | 298-2500 |
| O2 | 29,37 | 31,46 | 3,39 | - | -3,77 | 298-3000 |
| СO | 29,14 | 28,41 | 4,1 | - | -0,46 | 298-2500 |
| СO2 | 37,11 | 44,14 | 9,04 | - | -8,54 | 298-2500 |
| Н2 O(ж) | 75,3 | 39,02 | 76,64 | - | 11,96 | 298-380 |
| Н2 O(г) | 33,61 | 10,71 | - | 0,33 | 258-2500 | |
| Н2 O2(г) | 42,39 | 52,3 | 11,88 | - | -11,88 | 298-1500 |
Вязкость газов
Вязкость газов определяется как и теплопроводность на основании кинетической теории идеальных газов. Так что имеется связь между коэффициентом вязкости μ и коэффициентом теплопроводности.

Здесь μ – [П*сек] коэффициент динамической вязкости; Ср – удельная изобарная теплоемкость, [Дж/кг0]; R = 8314,4 Дж/кмоль0, М – молекулярный вес, кг/моль.
Кроме динамической вязкости часть используется коэффициент кинематической вязкости ν, [м2/сек].

Где ρ – плотность газа, кг/м3.
Пример: Определить коэффициенты кинематической и динамической вязкости воздуха при 293 0К.
Ср= 1006 Дж/кг0, λ=0,0263 Вт/м0, М=28,84 кг/кмоль.

Вязкость капельных жидкостей определяется в основном экспериментально и её значения приводятся в справочниках [9-10].
Таблица 4.п. Вязкость воды в интервале температур 5-1000С.
| t, 0С | μ*103, Па*сек. | t, 0С | μ*103, Па*сек. |
| 1,5193 | 0,5044 | ||
| 1,3073 | 0,467 | ||
| 1,1383 | 0,4339 | ||
| 1,002 | 0, 4046 | ||
| 0,8902 | 0,3785 | ||
| 0,7973 | 0,3551 | ||
| 0,7191 | 0,3341 | ||
| 0,6527 | 0,3150 | ||
| 0,5961 | 0,2978 | ||
| 0,5471 | 0,2821 |
Таблица 5.п.
| Вещество | 0 0С | 10 0С | 20 0С | 25 0С | 30 0С | 40 0С | 50 0С | 60 0С |
| Ацетон | 0,397 | 0,361 | 0,325 | 0,310 | 0,296 | 0,271 | 0,249 | 0,228 |
| Бензол | 0,910 | 0,755 | 0,652 | 0,600 | 0,559 | 0,503 | 0,436 | 0,389 |
| Гексан | 0,381 | 0,343 | 0,307 | 0,294 | 0,29 | 0,253 | 0,248 | 0,222 |
| Гептан | - | - | 0,414 | 0,39 | 0,373 | 0,338 | 0,308 | 0,281 |
| Глицерин | 12,1*103 | 3,95*103 | 1,49*103 | 0,95*103 | 0,63*103 | |||
| Метанол | 0,817 | 0,69 | 0,597 | 0,547 | 0,510 | 0,450 | 0,396 | 0,350 |
| Октан | 0,714 | 0,622 | 0,546 | 0,514 | 0,486 | 0,435 | 0,392 | 0,356 |
| Сероуглерод | 0,433 | 0,396 | 0,365 | 0,352 | 0,341 | 0,319 | 0,297 | - |
| Толуол | 0,77 | 0,667 | 0,584 | 0,552 | 0,517 | 0,489 | 0,425 | 0,387 |
| Циклогексан | - | - | 0,970 | 0,898 | 0,822 | 0,708 | 0,640 | 0,538 |
| Этанол | 1,773 | 1,466 | 1,200 | 1,096 | 1,003 | 0,834 | 0,702 | 0,592 |
При определении числа Нусельта (Nu), необходимо знание числа Прандтля ( )
)
Для газов это число не сильно отличается от единицы и слабо зависит от температуры.
Для жидкостей число Pr заметно большеединицы и определять его можно по выражениям  , учитывая зависимость коэффициентов переноса от температуры.
, учитывая зависимость коэффициентов переноса от температуры.
Для газов число Прандтля можно оценить, если известно значение теплоемкости по зависимости [11]

Пример: определить число Pr для метана при температуре T=10000К.
Теплоемкость  ;
;
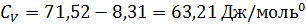 ;
;
 ;
;
 .
.
Таблица 10.п. Теплопроводность, теплоемкость и плотность твердых тел.
| Вещество | Плотность, кг/м3 | Теплопроводность, Вт/м0 | Теплоемкость, Дж/кг0 |
| Бетон (сухой) | 0,84 | ||
| Асфальт | 0,7 | ||
| Железобетон | 1,55 | ||
| Глина | 0,6 | ||
| Сосна – | 0,42 | ||
| Сосна | | 0,14 | ||
| Кирпич | 0,77 | ||
| Стекло | 0,96 | 0,16 | |
| Сталь (мягкая) |